Механизм иммунной реакции. Клеточные факторы неспецифической защиты
Читайте также
Основными элементами иммунной системы организма являются белые клетки крови – лимфоциты, существующие в двух формах. Обе формы происходят из клеток-предшественников в костном мозге, т.н. стволовых клеток. Незрелые лимфоциты покидают костный мозг и попадают в кровяное русло. Некоторые из них направляются к тимусу (вилочковой железе), расположенному у основания шеи, где происходит их созревание. Прошедшие через тимус лимфоциты известны как Т-лимфоциты, или Т-клетки (Т от «тимус»). В экспериментах на цыплятах было показано, что другая часть незрелых лимфоцитов закрепляется и созревает в сумке Фабрициуса – лимфоидном органе около клоаки. Такие лимфоциты известны как В-лимфоциты, или В-клетки (B от bursa – сумка). У человека и других млекопитающих В-клетки созревают в лимфатических узлах и лимфоидной ткани всего организма, эквивалентных сумке Фабрициуса у птиц.
Оба типа зрелых лимфоцитов имеют на своей поверхности рецепторы, которые могут «узнавать» специфический антиген и связываться с ним. Контакт В-клеточных рецепторов со специфическим антигеном и связывание определенного его количества стимулируют рост этих клеток и последующее многократное деление; в результате образуются многочисленные клетки двух разновидностей: плазматические и «клетки памяти». Плазматические клетки синтезируют антитела, выделяющиеся в кровоток. Клетки памяти являются копиями исходных В-клеток; они отличаются большой продолжительностью жизни, и их накопление обеспечивает возможность быстрого иммунного ответа в случае повторного попадания в организм данного антигена.
Что касается Т-клеток, то при связывании их рецепторами значительного количества определенного антигена они начинают секретировать группу веществ, называемых лимфокинами. Некоторые лимфокины вызывают обычные признаки воспаления: покраснение участков кожи, местное повышение температуры и отек за счет увеличения кровотока и просачивания плазмы крови в ткани. Другие лимфокины привлекают фагоцитирующие макрофаги – клетки, которые могут захватывать и поглощать антиген (вместе со структурой, например бактериальной клеткой, на поверхности которой он находится). В отличие от Т- и В-клеток эти макрофаги не обладают специфичностью и атакуют широкий спектр разных антигенов. Еще одна группа лимфокинов способствует разрушению инфицированных клеток. Наконец, ряд лимфокинов стимулирует добавочное количество Т-клеток к делению, что обеспечивает быстрое возрастание числа клеток, которые отвечают на тот же антиген и выделяют еще больше лимфокинов.
Антитела, вырабатываемые В-клетками и поступающие в кровь и другие жидкости организма, относят к факторам гуморального иммунитета (от лат. humor – жидкость). Защита организма, осуществляемая с помощью Т-клеток, называется клеточным иммунитетом, так как в ее основе лежит взаимодействие отдельных клеток с антигенами. Т-клетки не только активируют другие клетки путем выделения лимфокинов, но и атакуют антигены с помощью содержащих антитела структур на поверхности клетки.
Антиген может индуцировать оба типа иммунного ответа. Более того, в организме происходит определенное взаимодействие между Т- и В-клетками, причем Т-клетки осуществляют контроль над В-клетками. Т-клетки могут подавлять B-клеточный ответ на безвредные для организма чужеродные вещества или, наоборот, побуждать В-клетки вырабатывать антитела в ответ на вредные вещества с антигенными свойствами. Повреждение или недостаточность данной контролирующей системы может проявляться в виде аллергических реакций на вещества, обычно безопасные для организма.
Этапы иммунной реакции
Иммунную реакцию от начала до завершения можно разделить на три этапа:
Распознавание антигена;
формирование эффекторов;
эффекторная часть иммунного ответа.
Основу теории специфического распознавания антигенов составляют следующие постулаты:
1. На поверхности лимфоцитов присутствуют специфические антигенсвязывающие рецепторы, которые экспрессируются вне зависимости от того, встречался ли ранее организм с данным антигеном.
2. Каждый лимфоцит имеет рецептор только одной специфичности.
3. Антигенсвязывающие рецепторы экспрессируются на поверхности как Т-, так и В-лимфоцитов.
4. Лимфоциты, наделенные рецепторами одной специфичности, являются потомками одной родительской клетки и составляют клон.
5. Макрофаги осуществляют презентацию антигена лимфоциту.
6. Распознавание «чужого» напрямую связано с распознаванием « своего », т.е. антигенсвязывающий рецептор лимфоцита распознает на поверхности макрофага комплекс, состоящий из чужеродного антигена и собственного антигена гистосовместимости (МНС).
В состав молекулярного аппарата антигенного распознавания входят антигены главного комплекса гистосовместимости, антигенсвязывающие рецепторы лимфоцитов, иммуноглобулины, молекулы клеточной адгезии.
К основным этапам антигенного распознавания относятся:
Неспецифический этап;
распознавание антигена Т-клетками;
распознавание антигена В-клетками;
клональная селекция.
Неспецифический этап
Макрофаг первым вступает во взаимодействие с антигеном, осуществляя филогенетически самую древнюю разновидность иммунной реакции. Антиген подвергается фагоцитозу и перевариванию, результатом которого является «разборка» крупных молекул на составные части. Этот процесс называется «процессингом антигена». Затем процессированный антиген экспрессируется в комплексе с белками главного комплекса гистосовместимости на поверхности макрофага.
Распознавание антигена Т- клетками. Т - хелпер распознает комплекс, состоящий из чужеродного антигена и собственного антигена МНС. Для иммунного ответа необходимо одновременное распознавание как чужеродного антигена, так и собственного антигена МНС.
Распознавание антигена В- клетками. В- лимфоциты распознают антигены посредством своих иммуноглобулиновых рецепторов. Антиген также может подвергаться повторному процессингу при взаимодействии с В-лимфоцитом. Процессированный антиген помещается на поверхность В- клетки, где он распознается активированным Т - хелпером. В- лимфоцит не способен к самостоятельному ответу на антигенную стимуляцию, поэтому ему необходимо получить второй сигнал от Т -хелпера. Антигены, иммунная реакция на которые возможна только с таким повторным сигналом, называются тимусзависимыми. Иногда активация В - лимфоцитов возможна и без участия Т - клеток. Бактериальный липополисахарид в высоких концентрациях вызывает активацию В - лимфоцитов. При этом специфичность иммуноглобулиновых рецепторов В - лимфоцита не имеет значения. В данном случае собственная митогенная активность липополисахарида исполняет роль второго сигнала для В - лимфоцитов. Такие антигены называют тимуснезависимыми антигенами типа I. Некоторые линейные антигены (полисахариды пневмококков, поливинилпирролидон и др.), также стимулируют В- клетки без участия Т - лимфоцитов. Эти антигены длительное время остаются на мембране специализированных макрофагов и называются тимуснезависимыми антигенами типа II.
Клональная селекция
При попадании в организм антигена происходит селекция клонов с рецепторами, комплементарными данному антигену. Только представители этих клонов участвуют в дальнейшей антигензависимой дифференцировке клона В-лимфоцитов.
Формирование эффекторного звена иммунной реакции происходит путем дифференцировки клона В-лимфоцитов и образования цитотоксических Т-лимфоцитов.
Взаимодействие между клетками в процессе формирования иммунного ответа на антигенную стимуляцию осуществляется за счет особых растворимых медиаторов - цитокинов. Под воздействием различных цитокинов, продуцируемых макрофагами либо Т-лимфоцитами, происходит созревание В-лимфоцитов в антителообразующие клетки.
Для В- лимфоцитов конечным этапом дифференцировки является преобразование в плазматическую клетку, которая продуцирует огромное количество антител. Специфичность этих антител соответствует специфичности иммуноглобулинового рецептора В- лимфоцита -предшественника.
После того, как эффекторное звено иммунной реакции сформировано, наступает ее третий этап. На завершающем этапе иммунного ответа задействованы антитела, система комплемента, а также цитотоксические Т-лимфоциты, осуществляющие цитотоксическую реакцию.
Комплекс микроорганизма с антителом запускает классический путь активации системы комплемента, в результате чего образуется мембраноатакующий комплекс (МАК), наносящий клеточной стенке бактерии повреждения. Кроме того антитела нейтрализуют бактериальные токсины и, связываясь с инкапсулированными бактериями, облегчают их фагоцитоз макрофагами. Этот феномен называется опсонизацией. Доказано, что неопсонизированным инкапсулированным бактериям часто удается избежать фагоцитоза.
Внешне же иммунный ответ проявляется в развитии острой воспалительной реакции.
Иммунные реакции
Под иммунитетом понимают систему защиты организма от всего генетически чужеродного — будь то микробы, трансплантаты (пересаженные ткани и органы) или изменившиеся в антигенном отношении собственные клетки, включая раковые или отжившие свой срок нормальные.
Прежде чем нейтрализовать, уничтожить и элиминировать (вывести) из организма носителей генетической чужеродности, их необходимо обнаружить и распознать. Все клетки индивидуального организма имеют специальную маркировку (антигены тканевой совместимости), благодаря которой они воспринимаются иммунной системой как «свои». Клетки, не имеющие такой маркировки, воспринимаются как «чужие», атакуются и уничтожаются иммунной системой. Чужеродные вещества и клетки, вызывающие специфический иммунный ответ, называются антигенами. Различают экзогенные антигены (белки, полисахариды, искусственные полимеры, вирусы, бактерии и их токсины, трансплантаты) и эндогенные антигены , к которым относятся собственные ткани организма, измененные повреждением, и мутантные клетки, постоянно появляющиеся в организме человека (в сутки образуется до 106 мутантных клеток). Таким образом, иммунная система защищает многоклеточный организм от вторжения извне и от «внутренней измены» и, тем самым, обеспечивает генетическое постоянство всех соматических клеток, составляющих конкретный индивидуальный организм.
Иммунный ответ осуществляется иммунокомпетентными клетками и продуктами их жизнедеятельности — медиаторами иммунных реакций. Различают Т- и В-системы иммунитета. Т-система обеспечивает преимущественно противоопухолевую, антивирусную защиту, а также реакции отторжения трансплантата. В-система обеспечивает, главным образом, гуморальную антибактериальную защиту и нейтрализацию токсинов. Т-система иммунитета представлена популяцией тимусзависимых лимфоцитов (Т-лимфоцитов), которые имеют разную специализацию:
¨ Т-киллеры (Тк) — клетки-убийцы генетически чужеродных клеток;
¨ Т-хелперы (Тх) — клетки-помощники — стимулируют посредством хелперных медиаторов образование клона антигенчувствительных Т-киллеров и В-лимфоцитов;
¨ Т-супрессоры (Тс) — клетки, подавляющие посредством супрессорных медиаторов иммунный ответ.
Совместная деятельность Тх- и Тс-лимфоцитов определяет направленность, силу и продолжительность иммунного ответа. В начальный период нормального иммунного ответа превалирует активность Т-хелперов, в момент окончания — Т-супрессоров. Активность иммунокомпетентных клеток находится под контролем специальных генов иммунного ответа — Ir-генов. В частности, Ir-гены контролируют синтез антител и медиаторов иммунитета (хелперных и супрессорных).
В-система представлена популяцией В-лимфоцитов, которые, в ответ на антиген (антигенную стимуляцию), трансформируются в плазмоциты, — клетки, синтезирующие антитела (иммуноглобулины) (рис. 8.1). Фагоциты осуществляют фагоцитоз (рис. 8.2).

Рис. 8.1. Этапы формирования приобретённого иммунитета:
I — взаимодействие Т- и В-лимфоцитов с участием макрофага;
II — формирование клеток, хранящих информацию об антигенной структуре конкретного микроорганизма и способных вырабатывать специфические белки, связывающие микроорганизмы (антитела)

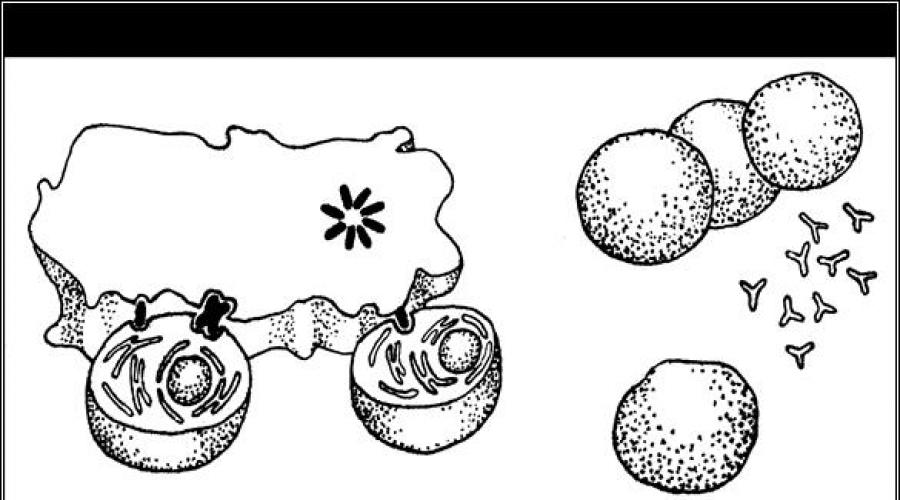
Рис. 8.2. Стадии фагоцитоза:
I — сближение фагоцита с объектом (комплексом антиген-антитело);
II — прилипание (адгезия) — способствуют опсонины;
III — захват фагоцитируемого объекта;
IV — переваривание комплекса антиген-антитело
Известны пять классов иммуноглобулинов: IgМ, IgG, IgА, IgE и IgD, которые продуцируются в строго определенной последовательности. IgM — низкоспецифичные антитела, которые вырабатываются первыми в ответ на антиген. Они образуют непрочную связь с антигеном и мобилизуют плазмоциты на продукцию высокоспецифичных антител (IgG и IgA). Смена синтеза IgM на синтез IgG и IgA происходит под влиянием лимфокинов (медиаторов), секретируемых Т-хелперами. IgG находятся в сыворотке крови и называются сывороточными антителами . Они прочно связывают антиген и являются самыми распространенными антителами против антигенной угрозы. IgA секретируются слизистыми оболочками носа, дыхательных путей, кишечника, урогенитальной системы. Они называются секреторными антителами и выполняют роль «первой линии обороны» в местах внедрения антигена. У млекопитающих они передаются от матери к ребенку через грудное молоко. IgE (реагины) синтезируются преимущественно в лимфоидной ткани слизистых оболочек и лимфатических узлах кишечника и бронхов. Они обладают высокой гомоцитотропностью (сродством к клеткам собственного организма) и поэтому могут выступать в качестве соучастников аллергических реакций. Роль IgD пока не установлена.
Действие иммуноглобулинов на антигены проявляется в следующих вариантах:
1. Агглютинация (склеивание) и иммунный лизис — растворение бактериальных антигенов.
Иммунный ответ
Такие иммуноглобулины называются агглютининами и бактериолизинами. Реакции иммунного лизиса происходят при участии комплемента — составной части кровяной сыворотки.
2. Цитотоксическое действие антител (цитотоксинов) — лишение клеток жизнеспособности. Эта реакция также протекает при участии комплемента.
3. Нейтрализация токсинов антителами (антитоксинами).
4. Опсонизация — усиление антителами (опсонинами) фагоцитарной активности микро- и макрофагов.
5. Преципитация — осаждение антигенов антителами.
Полноценный иммунный ответ обеспечивается кооперативным взаимодействием Т-лимфоцитов, В-лимфоцитов и макрофагов. Включение иммунных механизмов защиты начинается с момента проникновения антигена в организм. Макрофаг (моноцит) захватывает антиген, перерабатывает и выводит его антигенные детерминанты (структуры, обусловливающие антигенную уникальность и чужеродность) на свою клеточную поверхность. Обработанный таким образом антиген в 100-1000 раз более иммуногенен, чем нативный антиген. Он включает дальнейшие иммунные механизмы. Антигенные детерминанты, представленные макрофагом, распознаются В-лимфоцитами и Тх-клетками.
При экзогенной антигенной стимуляции В-лимфоциты трансформируются в плазмоциты и начинают сразу же продуцировать низкоспецифичные IgM. Через некоторое время, под влиянием медиаторов Т-хелперов, плазмоциты переключают синтез иммуноглобулинов на высокоспецифичные к данному антигену IgG, а затем — IgA. Одновременно Тх-лимфоциты стимулируют образование клона В- лимфоцитов, в которых формируется иммунная память на данный антиген. Таким способом обеспечивается активный иммунитет .
Тх-лимфоциты стимулируют положительный хемотаксис нейтрофильных лейкоцитов (микрофагов) к месту расположения антигена, что является важным механизмом в обезвреживании бактерий.
Эндогенная антигенная стимуляция вовлекает в иммунный ответ Тк-лимфоциты. В результате кооперации макрофага, Т-хелпера и Т-киллера, последний приобретает свойства размножаться, создавая популяцию антигенчувствительных Тк-клеток, и целенаправленно уничтожать антигены. Помимо Тк-клеток цитотоксические эффекты осуществляются Нк-лимфоцитами (натуральными киллерами), которые уничтожают клеточные антигены (клетки-мишени) без предварительной кооперации (рис. 8.3).
Полноценный иммунный ответ редко осуществляется без взаимодействия его клеточного и гуморального вариантов. Так, Т-киллеры становятся антигенчувствительными, когда связываются со специфическими иммуноглобулинами, комплементарными антигенам клеток-мишений. Макрофаги, опсонизированные иммуноглобулинами, приобретают способность направленно атаковать клетки- мишени и растворять их.
Указанные механизмы иммунного ответа лежат также в основе аллергических реакций.
Предыдущая16171819202122232425262728293031Следующая
ПОСМОТРЕТЬ ЕЩЕ:

Иммунные клетки и иммуноглобулины
Вместе с тем иммунная реакция может происходить по разным сценариям. Вначале иммунная система блокирует деятельность чужеродных объектов (иммуногенов), создавая особые химически реактивные молекулы (иммуноглобулины), ингибирующие деятельность иммуногенов.
Иммуноглобулины создаются лимфоцитами, которые являются основными клетками иммунной системы. Существует два основных вида лимфоцитов, при совместной активности создающих все виды иммунных реакций: T-лимфоциты (T-клетки) и B-лимфоциты (B-клетки). T-лимфоциты при восприятии чужеродного материала сами осуществляют иммунный ответ – уничтожают генетически чужеродные клетки. T-лимфоциты – это основа клеточного иммунитета.
Гуморальный иммунитет
B-лимфоциты нейтрализуют чужеродные объекты дистанционно, создавая особые химически реактивные молекулы – антитела. B-лимфоциты – это основа гуморального иммунитета.
Существует пять классов антител: IgM, IgD, IgE, IgG, IgA. Основным классом иммуноглобулинов ялвятеся IgG.
Что такое иммунная реакция или иммунный ответ?
Антитела IgG составляют около 70% от всех антител. Иммуноглобулины IgA составляют около 20% всех антител. Антитела остальных классов составляют всего 10% от всех антител.
Когда происходит гуморальная иммунная реакция, уничтожение чужеродного материала происходит в плазме крови в виде химической реакции. Иммуноглобулины, созданные вследствие иммунной реакции, могут оставаться на многие годы и десятилетия, обеспечивая организм защитой от повторного заражения, например свинкой, ветрянкой, краснухой. Благодаря этому процессу возможна вакцинация.
T-клетки отвечают за иммунный ответ на двух уровнях. На первом уровне они способствуют обнаружению чужеродного материала (иммуногена) и активируют B-клетки к синтезу иммуноглобулинов. На втором уровне, после стимуляции B-клеток к выработке иммуноглобулинов, T-клетки начинают расщеплять и разрушать чужеродный материал напрямую.
Такая активированная T-клетка уничтожает вредоносную клетку, сталкиваясь и прикрепляясь к ней вплотную – поэтому их стали называть клетками-убийцами или T-киллерами.
Клеточный иммунитет
Клеточная иммунная защита была открыта И.И. Мечниковым в конце XIX века. Он доказал, что защита организма от заражения микроорганизмами происходит благодаря способности особых клеток крови прикрепляться и расщеплять вредоносные микроорганизмы.
Этот процесс назвали фагоцитозом, а клеток-убийц, выслеживающих чужеродные микроорганизмы – фагоцитами. Синтез иммуноглобулинов и процесс фагоцитоза являются специфическими факторами иммунитета человека.
Неспецифический иммунитет
Помимо специфических, имеются неспецифические факторы иммунитета. Среди них:
непропускание возбудителей инфекции эпителием;
присутствие в кожных выделениях и желудочном соке веществ, негативно воздействующих на инфекционные агенты;
наличие в плазме крови, слюне, слезах и т.д. особых энзимных систем, расщепляющих бактерий и вирусов (например, мурамидаза).
Защита организма осуществляется не только разрушением внедряющегося в него генетически чужеродного материала, но и выведением из органов и тканей уже локализовавшихся в них иммуногенов. Известно, что вирусы, бактерии и отходы их жизнедеятельности, а также погибшие бактерии транспортируются наружу через потовые железы, мочевыделительную систему и кишечник.
Еще одним неспецифическим механизмом защиты служит интерферон – антивирусная белковая структура, синтезируемая инфицированной клеткой. Перемещаясь по внеклеточному матриксу и попадая в здоровые клетки, этот белок защищает клетку от вируса и от системы комплемента – комплекса белков, постоянно присутствующих в плазме крови и других жидкостях организма, которые уничтожают клетки, содержащие чужеродный материал.
Защита организма ослабевает чаще всего из-за несоблюдения здорового образа жизни или вследствие злоупотребления антибиотиками.
Перед применением необходимо проконсультироваться со специалистом.
Родоначальницей всех клеток иммунной системы является кроветворная стволовая клетка (КСК). Самоподдерживающаяся популяция таких клеток образуется в костном мозге и дает начало всем клеткам крови, а также КСК генерирует лимфоидную стволовую клетку (ЛСК) – общего прародителя всех лимфоцитов. ЛСК образует 2 типа клеток: предшественников Т-лимфоцитов и предшественников В-лимфоцитов из которых развиваются Т- и В- популяции лимфоцитов.
Развитие Т-лимфоцитов происходит в центральном органе иммунной системы – тимусе, поэтому Т-лимфоциты называют тимус-зависимые. Они образуют и поставляют в кровь три самостоятельных типа лимфоцитов – Т-помощники (хелперы, распознающие антиген и активизирующие В-лимфоциты, которые только после этого могут вступать в реакции), Т-эффекторы (вступающие в реакцию с антигеном) и Т-супрессоры (угнетатели, подавляющие иммунный ответ).
Предшественники В-лимфоцитов в бурсе Фабрициуса у птиц или ее аналогах у млекопитающих и человека (аппендикс, миндалины, а также сам костный мозг) становятся иммунокомпетентными и поставляют в кровь и периферические лимфоидные органы активные В-лимфоциты, способные обеспечивать накопление плазматических клеток, продуцирующих антитела.
Иммунная реакция организма может иметь различный характер, но всегда начинается с захвата антигена макрофагами (эти клетки так называются из-за их размеров и способности к фагоцитозу) крови и тканей. Антиген обрабатывается макрофагом, причем чаще всего подвергается лишь частичной деградации, некоторая часть его адсорбируется на поверхность макрофага. Именно благодаря этому Т-хелперы быстро распознают антиген. Одновременно с антигеном соединяются и Т-эффекторы. Это обеспечивает сенсибилизацию (повышение чувствительности лимфоцитов к антигену). Распознав антиген, Т-хелперы секретируют гамма-интерферон, который активирует макрофаги и способствует уничтожению захваченных ими микроорганизмов
Т- и В-лимфоциты с захваченными антигенами оседают в ближайших лимфатических узлах и там претерпевают ряд клеточных изменений, превращаясь в малодифференцированные клетки-бласты.
Интенсивно делясь, Т-лимфобласты образуют активные лимфоциты-киллеры, которые и обеспечивают специфический клеточный иммунитет . После того, как Т-киллер получает информацию о наличие чужеродного антигена, он совершает цитотоксическое действие (цитолиз). Т-киллер совершает «укол» клетки, выпускает из своей цитоплазмы специфические вещества, нарушающие целостность мембраны клетки-мишени, что в конечном итоге приводит к гибели этой клетки. Такие удары Т-киллер может производить неоднократно.
В-лимфобласты образуют активные В-лимфоциты и плазматические клетки, которые вырабатывают и выделяют в кровь антитела, осуществляющие специфический гуморальный иммунитет.
Одновременно с этим, Т-лимфобласты и В-лимфобласты вырабатывают и выделяют в кровь клетки иммунологической памяти, которые при повторном контакте с антигеном вызывают значительную активацию иммунитета. Например, если пересадить лоскут кожи (трансплантат) от одной особи к другой, то он отторгается в результате иммунной реакции через 10-11 дней. Вторичный трансплантат от того же донора отторгается в среднем в 2 раза быстрее. Подобная реакция носит название вторичного иммунного ответа и приводит к массовому выбросу антител, которые быстро нейтрализуют вредное действие антигена.
Так формируется иммунитет. Следует помнить, что иммунитет к одному антигену не защищает организм от других антигенов. Каждый раз при попадании в организм нового патогенного агента заболевание может быть предотвращено только в том случае, если образуются соответствующие антитела нового типа.
Т.о. в развитии иммунного ответа можно выделить 3 основные фазы:
1) афферентная фаза – распознавание антигена и активация иммунокомпетентных клеток;
2) центральная фаза – вовлечение в процесс клеток-предшественниц, пролиферация, дифференциация, в том числе в клетки памяти и клетки-эффекторы;
3) эффекторная фаза – разрушение, элиминация антигена из организма либо гуморальным путем за счет реакции антитело+антиген, либо клеточным – цитотоксическая реакция.
Еще одна важная особенность иммунитета – иммунологическая толерантность – характеризует способность иммунной системы не реагировать на антигены собственного организма.
Развитие лимфоидных образований в организме человека подчинено ряду закономерностей. Во-первых, все иммунные образования рано формируются в эмбриогенезе. Во-вторых, к моменту рождения человека все лимфоидные структуры в основном уже сформированы (это важно, т.к. после рождения организм ребенка один на один остается с внешней средой и ее многообразным влиянием). В-третьих, число и размеры лимфоидных образований (узелков) в стенках внутренних органов после рождения быстро увеличиваются, а в детском и подростковом возрасте достигают максимума. В-четвертых, эти показатели заметно уменьшаются до очень низких значений в пожилом и старческом возрасте, что ведет к снижению защитных возможностей организма. С этим, вероятно, коррелирует рост числа опухолевых и других заболеваний именно в эти периоды онтогенеза. Есть также основания предполагать, что именно более выраженное уменьшение массы иммунокомпетентных элементов обусловливает меньшую продолжительность жизни мужчин.
За последние десятилетия иммунная система людей испытывает огромную нагрузку в результате стрессов, применения лекарств, нездоровой экологии и вредных привычек.
Одним из основных показателей состояния иммунной системы является количественная характеристика, касающаяся различных форм лейкоцитов. В нормальных условиях количество лейкоцитов составляет 4 – 8,8*10 9 /л. Лейкоцитарная формула, т.е. % содержание в крови отдельных форм лейкоцитов, такова: нейтрофилы – 60-70%, эозинофилы 0-5%, базофилы – 0-1%, лимфоциты – 18-40%, моноциты – 2-9%. В настоящее время анализ крови дополняется данными о количественном составе лимфоцитов: в нормальных условиях на долю Т-лимфоцитов приходится 50-80% от всех лимфоцитов, на долю В-лимфоцитов – 20-30%, на долю 0-лимфоцитов – 10-20%. Отклонение от данных значений, характеризующих лейкоцитарную популяцию форменных элементов крови, указывает на наличие патологии (лейкопения, лейкоцитоз).
1.1. ФОРМЫ ИММУНИТЕТА
Специфический иммунный ответ развивается в организме параллельно с развитием инфекции или после вакцинации и приводит к формированию ряда специфических эффекторных механизмов противоинфекционной защиты:
- Гуморальный иммунный ответ (Влимфоцит);
- Клеточный иммунный ответ (Тлимфоцит);
- Иммунологическая память (Т и Влимфоциты);
- Иммунологическая толерантность.
К этим механизмам относятся эффекторные молекулы (антитела) и эффекторные клетки (Тлимфоциты и макрофаги) иммунной системы.
Гуморальные иммунные реакции
В гуморальных иммунных реакциях участвуют три клеточных типа: макрофаги (Агпредставляющие клетки), Тхелперы и Влимфоциты.
Агпредставляющие клетки фагоцитируют микроорганизм и перерабатывают его, расщепляя на фрагменты (процессинг Аг). Фрагменты Аг выставляются на поверхности Агпредставляющей клетки вместе с молекулой МНС. Комплекс «Агмолекула МНС класса II» предъявляется Тхелперу. Распознавание комплекса Тхелпером стимулирует секрецию ИЛ1 макрофагами.
Тхелпер под действием ИЛ1 синтезирует ИЛ2 и рецепторы к ИЛ2; последний стимулирует пролиферацию Тхелперов, а также ЦТЛ. Таким образом, после взаимодействия с Агпредставляющей клеткой Тхелпер приобретает способность отвечать на действие ИЛ2 бурным размножением. Биологический смысл этого явления состоит в накоплении Тхелперов, обеспечивающих образование в лимфоидных органах необходимого пула плазматических клеток, вырабатывающих АТ к данному Аг.
Влимфоцит. Активация Влимфоцита предполагает прямое взаимодействие Аг с молекулой Ig на поверхности Вклетки. В этом случае сам Влимфоцит перерабатывает Аг и представляет его фрагмент в связи с молекулой МНС II на своей поверхности. Этот комплекс распознает Тхелпер, отобранный при помощи того же Аг. Узнавание рецептором Тхелпера комплекса Агмолекула МНС класса II на поверхности Влимфоцита приводит к секреции Тхелпером ИЛ2, ИЛ4, ИЛ5, ИЛ6, под действием которых Вклетка размножается, образуя клон плазматических клеток (плазмоцитов). Плазмоциты синтезируют антитела. Часть зрелых Влимфоцитов после антигензависимой дифференцировки циркулируют в организме в виде клеток памяти.
Антитела, специфически взаимодействуя с антигенными детерминантами (эпитопами) на поверхности микроорганизмов, образуют с ними иммунные комплексы, что ведет к активации мембраноатакующего комплекса системы комплемента и лизису микробных клеток. Кроме того, иммунные комплексы, включающие микроорганизмы и специфические антитела, быстрее и легче захватываются фагоцитирующими клетками организма при участии Fcрецепторов. При этом ускоряется и облегчается внутриклеточная гибель и переваривание. Защитная роль антител в антитоксическом иммунитете определяется также их способностью нейтрализовать токсины. Секреторные иммуноглобулины класса А обеспечивают местный специфический иммунитет слизистых оболочек, препятствуя прикреплению и проникновению патогенных микроорганизмов.
Рис. 1. Гуморальный иммунный ответ.
В результате кооперации макрофагов, Тхелперов и Влимфоцитов и дальнейшей дифференцировки
Влимфоцитов в плазматические клетки, последние продуцируют антитела, которые нейтрализуют антиген.
Клеточные иммунные реакции
В очаге иммунного воспаления Тэффекторы ГЗТ, активированные при контакте с микробными антигенами, продуцируют лимфокины, индуцирующие микробоцидные механизмы фагоцитов. В результате усиливается внутриклеточная гибель захваченных фагоцитами возбудителей.
Другой механизм гибели зараженных клеток носит название антителозависимой цитотоксичности (АЗЦТ). Он заключается в распознавании микробных антигенов на мембране зараженной клетки»мишени» антителами, адсорбированными на Fcрецепторах NKклеток или макрофагов. При этом цитотоксичность является результатом действия лизосомных ферментов и других продуктов секреции данных клеток.

Рис. 2. Клеточный иммунный ответ опосредован активированными
Тхелперами макрофагами и другими фагоцитирующими клетками, а также цитотоксическими Тлимфацитами.
Иммунологическая память
Иммунологическая память способность организма отвечать на повторное введение антигена иммунной реакцией, характеризующейся большей силой и более быстрым развитием.
Клетки иммунологической памяти долгоживущие Т и Влимфоциты, сохраняющие многие годы способность реагировать на повторное введение антигена, так как вырабатываются рецепторы к этому антигену. Иммунологическая память проявляется как ускоренный специфический ответ на повторное введение антигена.
Иммунологическая память к антигенным компонентам окружающей среды лежит в основе аллергических заболеваний, а к резусантигену (возникает при резуснесовместимости беременности) в основе гемолитической болезни новорожденных. Феномен иммунологической памяти используется в практике вакцинации людей.
Иммунологическая толерантность
Иммунологическая толерантность явление, противоположное иммунному ответу и иммунологической памяти, проявляющееся в том, что на введение антигена вместо выработки иммунитета в организме развивается ареактивность, инертность, отсутствие ответа на антиген.
Иммунный ответ против собственных тканей организма в нормальных условиях не развивается, т.е. иммунная система толерантна к подавляющему большинству Аг тканей организма (аутоантигены). Искусственная толерантность к чужеродным Аг может быть вызвана иммунизацией по определенной схеме (например, толерантность «низкой дозы» дробное введение Аг в возрастающих количествах или толерантность «высокой дозы» однократное введение Аг в высокой дозе).
1.2. ВИДЫ ИММУНИТЕТА
Многообразие систем защиты организма позволяют человеку оставаться невосприимчивым к действию инфекционных агентов.
Видовой иммунитет (врожденный) генетически закрепленная невосприимчивость присущая каждому виду. Например, человек никогда не заболевает чумой крупного рогатого скота. Крысы резистентны к дифтерийному токсину.
Приобретенный иммунитет формируется в течение жизни индивидуума и не передается по наследству; может быть естественным и искусственным, активным и пассивным.
Естественно приобретенный иммунитет (активный) развивается после перенесенного инфекционного заболевания, протекавшего в клинически выраженной форме, либо после скрытых контактов с микробными Аг (так называемая бытовая иммунизация). В зависимости от свойств возбудителя и состояния иммунной системы организма невосприимчивость может быть пожизненной (например, после кори), длительной (после брюшного тифа) или сравнительно кратковременной (после гриппа).
Инфекционный (нестерильный) иммунитет особая форма приобретенной невосприимчивости; не является следствием перенесенной инфекции, обусловлен наличием инфекционного агента в организме. Невосприимчивость исчезает сразу после элиминации возбудителя из организма (например, туберкулез; вероятно, малярия).
Естественный пассивный иммунитет связан с переносом IgG от матери к плоду через плаценту (передача по вертикали) или с грудным молоком (SIgA) новорожденному. Это обеспечивает устойчивость новорожденного ко многим возбудителям в течение некоторого, обычно индивидуально варьирующего срока.
Искусственно приобретенный иммунитет. Состояние невосприимчивости развивается в результате вакцинации, серопрофилактики (введение сыворотки) и других манипуляций.
Активно приобретенный иммунитет развивается после иммунизации ослабленными или убитыми микроорганизмами либо их антигенами. В обоих случаях организм активно участвует в создании невосприимчивости, отвечая развитием иммунного ответа и формированием пула клеток памяти.
Пассивно приобретенный иммунитет достигается введением готовых АТ или, реже, сенсибилизированных лимфоцитов. В таких ситуациях иммунная система реагирует пассивно, не участвуя в своевременном развитии соответствующих иммунных реакций.
Иммунитет может формироваться против микроорганизмов, их токсинов, вирусов, антигенов опухолей. В этих случаях иммунитет называют антимикробным, антитоксическим, антивирусным, противоопухолевым соответственно. При трансплантации несовместимых тканей возникает трансплантационный иммунитет (реакция отторжения трансплантата).
Поступление в организм антигена через дыхательные пути, пищеварительный тракт и другие участки слизистых поверхностей и кожи нередко обуславливает развитие выраженной локальной иммунной реакции. В таких случаях речь идет о местном иммунитете.
1.3. РЕГУЛЯЦИЯ ИММУННОГО ОТВЕТА
Интенсивность и продолжительность иммунного ответа контролируется и регулируется при участии ряда механизмов обратной связи на генетическом, клеточном и организменном уровнях.
Генетический контроль иммунного ответа связан с наличием конкретных генов, контролирующих синтез и выход специфических рецепторов на поверхность иммунокомпетентных клеток, что непосредственно влияет на уровень представления и распознавания антигена.
Иммунная система представляет собой комплекс взаимодействующих клеток, связанных между собой внутренними регуляторными связями посредством цитокинов.
На уровне организма осуществляется взаимодействие нервной, эндокринной и иммунной систем, иммунный ответ контролируется и регулируется нейрогуморальными механизмами, среди которых ведущую роль играют кортикостероидные гормоны, подавляющие процессы пролиферации, дифференцировки и миграции лимфоидных клеток и ингибирующие биосинтез интерлейкинов.
Воспаление сумма защитноадаптивных реакций, развивающихся в тканях при их повреждении; впоследствии они могут полностью восстанавливать свою структуру и функции либо в них формируются стойкие дефекты. Хорошо известны классические признаки, характеризующие острое воспаление: покраснение, отек, боль, локальное повышение температуры и нарушение функций органа или ткани. Если интенсивность острой реакции оказывается недостаточной для элиминации возбудителя, то она меняет свои характеристики и принимает хроническое течение.
С позиции защиты от патогенов большинство системных реакций острого воспаления резко изменяет лимфо и кровообращение в очаге. Вазодилатация и повышение проницаемости капилляров облегчает выход из просвета капилляров больших молекул (например, компонентов комплемента) и полиморфонуклеаров. Весьма важным фактором является снижение рН в воспаленных тканях, обусловленное преимущественно секрецией молочной кислоты фагоцитами. Снижение рН оказывает губительное действие на бактерии, повышает микробицидную активность низкомолекулярных органических кислот и снижает резистентность к действию антимикробных химиопрепаратов.
Любое инфекционное воспаление начинается с запуска комплементарного каскада и активации свертывающей системы, многие компоненты которых известны как медиаторы воспалительных реакций.
Лимфоидные клетки организма выполняют основную функцию в развитии иммунитета - невосприимчивости, не только по отношению к микроорганизмам, но и ко всем генетически чужеродным клеткам, например при пересадке тканей. Лимфоидные клетки обладают способностью отличать «свое» от «чужого» и устранять «чужое» (элиминировать).
Родоначальницей всех клеток иммунной системы является кроветворная стволовая клетка. В дальнейшем происходит развитие двух типов лимфоцитов: Т и В (тимусзависимых и бурсазависимых). Эти названия клетки получили в связи с их происхождением. Т-клетки развиваются в тимусе (зобной, или вилочковой железе) и под влиянием веществ, выделяемых тимусом, в периферической лимфоидной ткани.
Название В-лимфоциты (бурсазависимые) произошло от слова «бурса» - сумка. В сумке Фабрициуса у птиц развиваются клетки, сходные с В-лимфоцитами человека. Хотя у человека не найдено органа, аналогичного сумке Фабрициуса, название связано с этой сумкой.
При развитии В-лимфоцитов из стволовой клетки они проходят несколько стадий и преобразуются в лимфоциты, способные образовывать плазматические клетки. Плазматические клетки в свою очередь образуют антитела и на их поверхности имеются иммуноглобулины трех классов: IgG, IgM и IgA.
Иммунный ответ в виде продукции специфических антител происходит следующим образом; чужеродный антиген, проникнув в организм, прежде всего фагоцитируется макрофагами. Макрофаги, перерабатывая и концентрируя антиген на своей поверхности, передают информацию о нем Т-клеткам, которые начинают делиться, «созревают» и выделяют гуморальный фактор, включающий в антителопродукцию В-лимфоциты. Последние также «созревают», развиваются в плазматические клетки, которые и синтезируют антитела заданной специфичности.
Так, соединенными усилиями макрофаги, Т - и В-лимфоциты осуществляют иммунные функции организма - защиту от всего генетически чужеродного, в том числе и от возбудителей инфекционных болезней. Защита с помощью антител осуществляется таким образом, что синтезированные к данному антигену иммуноглобулины, соединяясь с ним (антигеном), подготавливают его, делают чувствительным к разрушению, обезвреживанию различными естественными механизмами: фагоцитами, комплементом и пр.
Теории иммунитета. Значение антител в развитии иммунитета неоспоримо. Каков же механизм их образования? Этот вопрос в течение длительного времени является предметом споров и обсуждений.
Создано несколько теорий антителообразования, которые можно разделить на две группы: селективные (селекция - отбор) и инструктивные (инструктировать-наставлять, направлять).
Селективные теории предполагают существование в организме уже готовых антител к каждому антигену или клеток, способных синтезировать эти антитела.
Так, Эрлих (1898) предполагал, что клетка имеет готовые «рецепторы» (антитела), которые соединяются с антигеном. После соединения с антигеном, антитела образуются еще в большем количестве.
Такого же мнения придерживались создатели других селективных теорий: Н. Ерне (1955) и Ф. Вернет (1957). Они утверждали, что уже в организме плода, а затем и во взрослом организме имеются клетки, способные к взаимодействию с любым антигеном, но под влиянием определенных антигенов определенные клетки вырабатывают «нужные» антитела.
Инструктивные теории [Гауровитц Ф., Полинг Л., Ландштей-нер К., 1937-1940] рассматривают антиген, как «матрицу», штамп, на котором формируются специфические группировки молекулы антител.
Однако эти теории не объясняли всех явлений иммунитета и в настоящее время наиболее принятой является клонально-селекционная теория Ф. Бернета (1964). Согласно этой теории в эмбриональном периоде в организме плода имеется множество лимфоцитов - клеток-предшественников, которые при встрече с собственными антигенами разрушаются. Поэтому во взрослом организме уже нет клеток для выработки антител к собственным Антигенам. Однако, когда взрослый организм встречается с чужеродным антигеном, происходит селекция (отбор) клона иммунологически активных клеток и, они вырабатывают специфические антитела, направленные против данного «чужого» антигена. При повторной встрече с этим антигеном клеток «отобранного» клона уже больше и они быстрее образуют большее количество антител. Эта теория наиболее полно объясняет основные явления иммунитета.
Механизм взаимодействия антигена и антител имеет различные объяснения. Так, Эрлих уподоблял их соединение реакции между сильной кислотой и сильным основанием с образованием нового вещества типа соли.
Бордэ считал, что антиген и антитела взаимно адсорбируют друг друга подобно краске и фильтровальной бумаге или йоду и крахмалу. Однако эти теории не объясняли главного - специфичности иммунных реакций.

Рис.67Схематическое изображение взаимодействия антител и
антигена. д - по схеме Маррека; Б - по схеме, Полинга. Структура комплекса: а - при оптимальных соотношениях; б - при избытке антигена; в - при избытке антител.
Наиболее полно механизм соединения антигена и антитела объяснен гипотезой Маррека (теория «решетки») и Полинга (теория «фермы») (рис. 33). Маррек рассматривает соединение антигена и антител в виде решетки, в которой антиген чередуется с антителом, образуя решетчатые конгломераты. Согласно гипотезе Полинга (см. рис. 33) антитела имеют две валентности (две специфические детерминанты), а антиген несколько валентностей - он поливалентен. При соединении антигена и антител образуются агломераты, напоминающие «фермы» построек.
При оптимальном соотношении антигена и антител образуются большие прочные комплексы, видимые простым глазом. При избытке антигена каждый активный центр антител заполнен молекулой антигена, не хватает антител для соединения с другими молекулами антигена и образуются мелкие, невидимые глазом комплексы. При избытке антител, для образования решетки не хватает антигена, детерминанты антител отсутствуют, и видимого проявления реакции нет.
На основании изложенных теорий специфичность реакции антиген - антитело сегодня представляют как взаимодействие детерминантной группы антигена и активных центров антитела. Так как антитела формируются под воздействием антигену, их структура соответствует детерминантным группам антигена. Детерминантная группа антигена и фрагменты активных центров антитела имеют противоположные электрические заряды и, соединяясь, образуют.комплекс, прочность которого зависит от соотношения компонентов и среды, в которой они взаимодействуют.
Учение об иммунитете - иммунология - достигло за последние десятилетия больших успехов. Раскрытие закономерностей иммунного процесса позволило решить различные задачи во многих областях медицины. Разработаны и совершенствуются методы предупреждения многих инфекционных заболеваний; лечения инфекционных и ряда других (аутоиммунных, иммунодефинитных) болезней; предупреждения гибели плода при резус-конфликтных ситуациях; трансплантации тканей и органов; борьбы со злокачественными новообразованиями; иммунодиагностики - использования реакций иммунитета в диагностических целях.
Реакции иммунитета - это реакции между антигеном и антителом или между антигеном и сенсибилизированными лимфоцитами, которые происходят д живом организме и могут быть воспроизведены в лабораторных условиях.
Реакции иммунитета вошли в практику диагностики инфекционных болезней в конце XIX-начале XX века. В силу высокой чувствительности (улавливают антигены в очень больших разведениях) и, главное, строгой специфичности (позволяют отличить близкие по составу антигены) они нашли широкое применений в решении теоретических и практических вопросов медицины и биологии. Этими реакциями пользуются иммунологи, микробиологи, инфекционисты, биохимики, генетики, молекулярные биологи, экспериментальные онкологи и врачи других специальностей.
Реакции антигена с антителом называются серологическими (от лат. serum - сыворотка) или гуморальными (от лат. humor-жидкость), потому что участвующие в них антитела (иммуноглобулины) всегда находятся в сыворотке крови.
Реакции антигена с сенсибилизированными лимфоцитами называются клеточными.

 Рис.68 Взаимодействие антигенов с антителами
Рис.68 Взаимодействие антигенов с антителами
Рис.69 Схема иммунного ответа.