Генная и клеточная терапия моногенных и мультифакторных заболеваний. Основы молекулярной терапии
Читайте также
14943 0
Установление локализации и последовательности гена, мутации которого вызывают конкретные заболевания, а также самой мутации и современные способы ее тестирования позволяют диагностировать заболевание в нео- и даже пренатальный период развития организма. Это дает возможность смягчить проявление генетического дефекта с помощью медикаментозного лечения, диеты, переливания крови и т.д.
Однако такой подход не приводит к исправлению самого дефекта и, как правило, наследственные заболевания не излечиваются. Ситуация осложняется еще и тем, что мутация одного гена может давать самые разные последствия на организм. Если мутация гена вызывает изменения активности фермента, который он кодирует, то это может привести к накоплению токсичного субстрата или, наоборот, к дефициту соединения, необходимого для нормального функционирования клетки.
Хорошо известным примером такого заболевания является фенилкетонурия. Его вызывает мутация в гене печеночного фермента фенилаланиндегидроксилазы, катализирующего превращение фенилаланина в тирозин. В результате повышается уровень эндогенного фенилаланина в крови, что вызывает неправильное формирование миелиновой оболочки вокруг аксонов нервных клеток центральной нервной системы и, как следствие, тяжелую умственную отсталость.
Если мутация затрагивает ген структурного белка, то это может приводить к серьезным нарушениям на уровне клеток, тканей или органов. Примером такого заболевания является кистозный фиброз.
Делеция в гене, кодирующем белок, который называется транспортер кистозного фиброза, приводит к синтезу дефектного белка (отсутствие фенилаланина 508) и нарушениям транспорта ионов хлора сквозь клеточные мембраны. Одним из наиболее вредных последствий этого является то, что слизь, которая выстилает и защищает легкие, становится ненормально густой. Это затрудняет доступ к клеткам легких и способствует накоплению вредных микроорганизмов. Клетки, выстилающие воздухоносные пути легких, погибают и заменяются фиброзной рубцовой тканью (отсюда название болезни). В результате пациент погибает от нарушения дыхания.
Наследственные заболевания отличаются сложными клиническими проявлениями, и их традицинное лечение имеет в основном симптоматический характер: для лечения фенилкетонурии назначают безаланиновую диету, дефектные белки заменяют функциональным внутривенным введением, для компенсации утраченных функций проводят трансплантацию костного мозга или других органов. Все эти меры, как правило, малоэффективны, дороги, длительны, и лишь немногие пациенты доживают до старости. Поэтому разработка принципиально новых видов терапии очень актуальна.
Генная терапия
Генной терапией называется генетическая инженерия соматических клеток человека, направленная на исправление генетического дефекта, вызывающего заболевание. Коррекция специфического заболевания осуществляется путем введения в дефектные соматические клетки нормальных экспрессирующихся генов. К 80-м гг., когда были разработаны методы получения отдельных генов и созданы эукариотические экспрессирующие векторы, стали рутинными эксперименты по переносу генов на мышах, перспективы генной коррекции стали реальными.В 1990 г. в США доктором У. Френч Андерсоном (W. French Andrson) были предпринята первая попытка генотерапии для лечения тяжелого комбинированного иммунодефицита (ТКИД) у трехлетней девочки Ашанти де Силва (Ashanthi da Silva). Это заболевание вызывается мутацией в гене, кодирующем аденозанаденилазу (АДА). Дефицит этого фермента способствует накоплению в крови аденозина и дезоксиаденозина, токсическое действие которых приводит к гибели В- и Т-лимфоцитов периферической крови и, как следствие, иммунодефициту.
Дети с таким заболеванием должны быть защищены от любых инфекций (содержаться в специальных стерильных камерах), поскольку любая болезнь может оказаться смертельной. Через 4 года после начала лечения у ребенка наблюдалась экспрессия нормально функционирующей АДА и облегчение симптомов ТКИД, что позволило ей покинуть стерильную камеру и жить нормальной жизнью.
Таким образом, была продемонстрирована принципиальная возможность успешной генетической терапии соматических клеток. Начиная с 90-х гг. проходят испытания генной терапии целого ряда генетических заболеваний, среди которых такие тяжелейшие, как гемофилия, СПИД, разные виды злокачественных новообразований, муковисцидоз и др. На данный момент поддаются излечению с помощью трансгенеза уже около 10 болезней человека.
Разнообразие генетических заболеваний предопределило развитие множества подходов генной терапии. При этом решаются 2 главные проблемы: средство доставки терапевтического гена; способ обеспечения адресной доставки к клеткам, предназначенным для коррекции. К настоящему времени все подходы к генной терапии соматических клеток можно разделить на две категории: терапия ex vivo и in vivo (рис. 3.15).
Рис. 3.15. Схема проведения генной терапии ex vivo (а) и in vivo (а)
Генная терапия ex vivo предполагает генетическое исправление дефектных клеток вне организма с последующим возвращением нормально функционирующих клеток в организм.
Генная терапия in vivo предусматривает доставку терапевтического гена непосредственно в клетки определенной ткани пациента. Рассмотрим эти подходы подробнее.
Генная терапия ex vivo включает следующие этапы:
1) получение дефектных клеток больного и их культивирование;
2) перенос нужного гена в изолированные клетки с помощью трансфекции терапевтической генной конструкции;
3) отбор и наращивание генетически исправленных клеток;
4) трансплантация или трансфузия этих клеток пациенту.
Использование собственных клеток пациента гарантирует, что после их возвращения у него не разовьется иммунный ответ. Процедура переноса генной конструкции должна быть эффективной, а нормальный ген должен стабильно поддерживаться и непрерывно экспрессироваться.
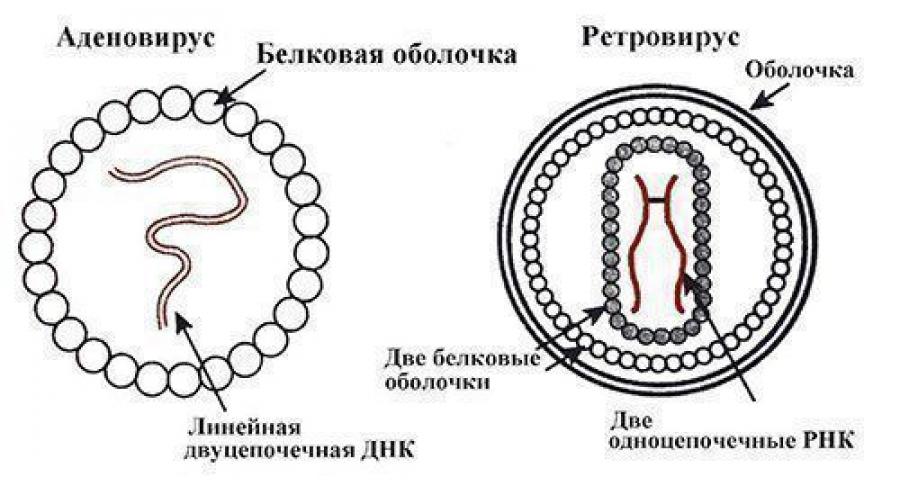
Средством переноса генов, созданного самой природой, являются вирусы. С целью получения эффективных векторов для доставки генов в основном используют две группы вирусов - аденовирусы и ретровирусы (рис. 3.16). В генной терапии применяют варианты генетически обезвреженных вирусов.

Рис. 3.16. Вирусы, применяемые для создания терапевтических векторов
Рассмотрим устройство и использование конструкций на основе ретро-вирусов. Напомним, что геном ретровируса представлен двумя идентичными одноцепочечными молекулами РНК, каждая из которых состоит из шести участков: два длинных концевых повтора (LTR) на 5" и 3" концах, некодирующая последовательность *Р+, необходимая для упаковки РНК в вирусную частицу, и три участка, кодирующих структурный белок внутреннего капсида (gag), обратную транскриптазу (pol) и белок оболочки (env) (рис. 3.17, а).

Рис. 3.17. Генетическая карта типичного ретровируса (а) и карта ретровирусного вектора (а)
Напомним, что жизненный цикл ретровируса включает следующие стадии:
1. Инфицирование клеток-мишени.
2. Синтез ДНК копии генома с помощью собственной обратной транскриптазы.
3. Транспорт вирусной ДНК в ядро.
4. Встраивание вирусной ДНК в хромосому клетки-хозяина.
5. Транскрипция мРНК с вирусной ДНК под контролем сильного промотора, локализованного на участке 5"-LTR.
6. Трансляция белков Gag, Pol и Env.
7. Образование вирусного капсида и упаковки двух РНК-цепей и молекул обратной транскриптазы.
8. Высвобождение вирионов из клетки.
При получении ретровирусного вектора полноразмерную ДНК ретро-вируса встраивают в плазмиду, удаляют большую часть гена gag и полностью гены pol и env, а вместо них встраивают «терапевтический» ген Т и при необходимости маркерный селективный ген Rg с собственным промотором (рис. 3.17, б). Транскрипция гена Т будет контролироваться все тем же сильным промотором, локализованным на 5"-LTR участке. На основе этой схемы созданы различные ретровирусные векторы и максимальный размер ДНК-вставки примерно 8 тыс. п.о.
Полученную таким образом конструкцию можно саму по себе использовать для трансформации, но ее эффективность и последующая интеграция в геном клетки-хозяина крайне низки. Поэтому была разработана методика упаковки полноразмерной РНК ретровирусного вектора в интактные вирусные частицы, которые с высокой частотой проникают в клетку и гарантированно встраиваются в геном хозяина. Для этого была создана так называемая «пакующая» клеточная линия. В двух разных участках хромосом этих клеток вшиты ретровирусные гены gag и pol-env, лишенные способности паковаться из-за отсутствия последовательности + (84*+) (рис. 3.18).

Рис. 3.18. Схема получения упакованного вирусного вектора
То есть оба эти фрагмента транскрибируются, но при этом образуются лишенные РНК пустые капсиды. При трансфекции РНК вирусного вектора в такие клетки она встраивается в хромосомную ДНК и транскрибируется с образованием полноразмерной РНК ретровируса, и в таких условиях в капсидах упаковывается только РНК вектора (только в ней имеется +-последовательность). Образующиеся интактные вирусные частицы используют для эффективной доставки ретровирусного вектора в клетки-мишени.
Ретровирусы активно инфицируют только интенсивно делящиеся клетки. Для переноса генов их обрабатывают очищенными частицами упакованного ретровирусного вектора или совместно культивируют с производящей их клеточной линией, а затем осуществляют селекцию для разделения клеток-мишеней и пакующих клеток.
Трансдуцированные клетки тщательно проверяют на уровень синтеза продукта терапевтического гена, отсутствие компетентных по репликации ретровирусов, отсутствие изменений способности клеток к росту или функционированию.
Наиболее пригодными для проведения генной терапии являются клетки костного мозга. Это связано с наличием в нем тотипотентных эмбриональных стволовых клеток, которые могут пролиферировать и дифференцироваться в различные типы клеток -В- и Т-лимфоциты, макрофаги, эритроциты, тромбоциты и остеокласты. Именно эти клетки применяют для лечения целого ряда наследственных заболеваний, среди них уже упомянутый нами тяжелый комбинированный иммунодефицит, болезнь Гоше, серповидноклеточная анемия, талассемия, остеопороз и др.
Помимо тотипотентных стволовых клеток костного мозга, которые трудно выделять и культивировать, используют стволовые клетки из пупoвинной крови (предпочтительное использование для генотерапии новорожденных), а также клетки печени - гепатоциты - для лечения гиперхолестеролемии.
При генной терапии in vivo особенно важно обеспечить доставку терапевтического гена к дефектным клеткам. Такую адресную доставку могут обеспечить модифицированные векторы, созданные на основе вирусов, способных инфицировать специфические виды клеток. Рассмотрим подход, разработанный для лечения уже упомянутого выше кистозного фиброза. Поскольку легкие являются открытой полостью, терапевтические гены к ним доставить относительно легко. Клонированный вариант здорового гена был введен в инактивированный аденовирус (рис. 3.19). Специфика этого типа вируса заключается в том, что он инфицирует выстилку легких, вызывая простуду.

Рис. 3.19. Схема получения вектора на основе аденовируса
Сконструированный таким образом вирус испытывали, распыляя его в нос и легкие экспериментальных животных, а затем людей-пациентов. В некоторых случаях наблюдалось введение и экспрессия здорового гена, и восстановление нормального переноса ионов хлора. Возможно, этот подход (введение нормального гена с помощью носовых аэрозолей) в ближайшем будущем будет широко использоваться для лечения симптомов кистозного фиброза в легких.
Кроме ретро- и аденовирусов в экспериментах по генной терапии используют и другие типы вирусов, например вирус Herpes simplex. Особенностью этого двунитевого (152 тыс. п.о.) ДНК-вируса является его способность специфически поражать нейроны. Известно множество генетических заболеваний, поражающих центральную и периферическую нервную систему - опухоли, метаболические нарушения, нейродегенеративные заболевания (болезнь Альцгеймера, болезнь Паркинсона).
Вирус простого герпеса I типа (HSV) является весьма подходящим вектором для терапии таких заболеваний. Капсид этого вируса сливается с мембраной нейрона, и его ДНК транспортируется в ядро. Предложено несколько способов переноса терапевтического гена с помощью HSV-векторов и проведены успешные испытания на экспериментальных животных.
Вирусные векторы имеют несколько недостатков: высокая стоимость, ограниченная клонирующая емкость и возможная воспалительная реакция. Так, в 1999 г. в результате развившегося необычайно сильного иммунного ответа на введение аденовирусного вектора погиб 18-летний доброволец, принимавший участие в испытаниях препарата. В 2002 г. у двух детей во Франции во время лечения от иммунодефицита (введением терапевтических генов в стволовые клетки с помощью ретровирусов) развилось состояние, похожее на лейкемию.
Поэтому разрабатываются невирусные системы доставки генов. Самый простой и неэффективный способ - это инъекция плазмидной ДНК в ткани. Второй подход - это бомбардировка тканей микрочастицами золота (1-3 мкм), конъюгированными с ДНК. При этом терапевтические гены экспрессируются в тканях-мишенях и их продукты - терапевтические белки - поступают в кровь. Основным недостатком этого подхода является преждевременная инактивация или разрушение этих белков компонентами крови.
Доставку ДНК можно осуществить, упаковав ее в искусственную липидную оболочку. Полученные таким образом сферические частицы-липосомы легко проникают через клеточную мембрану. Созданы липосомы с самыми разными свойствами, однако пока эффективность такой доставки невысока, поскольку большая часть ДНК подвергается лизосомному разрушению. Также для доставки генетической конструкции синтезируют конъюгаты ДНК с различными молекулами, способными обеспечить ее сохранность, адресную доставку и проникновение в клетку.
В последние годы проводятся интенсивные эксперименты по созданию искусственной 47-й хромосомы, которая позволила бы включить большое количество генетического материала с полным набором регуляторных элементов для одного или нескольких терапевтических генов. Это дало бы возможность использовать геномный вариант терапевтического гена и тем самым обеспечить его стабильность и эффективную длительную экспрессию. Проведенные эксперименты показали, что создание искусственной хромосомы человека, содержащей терапевтические гены, вполне реально, однако пока непонятно, каким образом вводить такую огромную молекулу в ядро клетки-мишени.
Основными проблемами, которые стоят перед генной терапией, помимо риска тяжелой иммунной реакции, являются трудности длительного хранения и функционирования терапевтической ДНК в организме пациента, мультигенность многих болезней, делающая их трудной мишенью для генной терапии, а также риск использования вирусов в качестве векторов.
Н.А. Воинов, Т.Г. Волова
30 августа 2017 года Управление по контролю за пищевыми продуктами и лекарственными средствами США (FDA) одобрена первая в мире генная терапия рака крови . Речь идет о Kymriah (tisagenlecleucel) компании Novartis Pharmaceuticals, который создан на основе технологии CAR-T и предназначен для лечения В-клеточного острого лимфобластного лейкоза у детей и молодых взрослых пациентов до 25 лет, рефрактерным к другим методам лечения или имеющим рецидив заболевания.
Использование технологии редактирования генома CRISPR/Cas9 открывает новые возможности в генной терапии. CRISPR/Cas9 позволяет очень точно и безопасно изменять ДНК клеток. И если совместить технологию CRISPR/Cas9 с доставкой при помощи аденоассоциированных вирусов, то это, по-видимому, позволит системно воздействовать на организм и совершенно безопасно изменять геном очень большого числа клеток.
И вот в 2016 году генетики из университета Дьюка (США) объявили, что им впервые в истории удалось успешно провести генную терапию взрослого млекопитающего (мыши) и вылечить его от генетического заболевания, связанного с дистрофией мышц. Для этого была использована модифицированная версия сравнительно новой технологии редактирования генов CRISPR/Cas9. Технология редактирования генов CRISPR/Cas9 связана с использованием аденоассоциированного вируса, помогающего доставлять генетический материал до места назначения. При помощи этой технологии были проведены успешные опыты по редактированию генов отдельных клеток в пробирках и одноклеточных эмбрионов. К сожалению, пока что возможность генетических манипуляций на эмбрионах человека вызывает ожесточённые споры.
CRISPR/Cas превзошел все ожидания. Он позволила с минимальным числом ошибок как «выключать» нужные гены, так и встраивать новые гены в строго определенные участки генома.
В декабре 2015 года научная группа Фенга Джанга видоизменила данную систему так, что она стала и вовсе безошибочной, что было опубликовано в ведущем научном журнале Science. Ученые заменили 3 аминокислоты «кирпичики», из которых состоит белок) в эндонуклеазе Cas9, после чего число ошибок такой системы свелось практически к нулю.
Использование CRISP/Cas9 особенно актуально для генной терапии старения, где требуется воздействовать на пути долголетия, общие для большинства клеток организма. По генной терапии старения до 2015 года не проведено ни одного клинического испытания на людях, что неудивительно, поскольку старение до сих пор не признано болезнью.
Кроме того, генная терапия старения пока еще очень молодая и развивающаяся область. Сейчас все исследования по генной терапии старения проводятся на модельных мышах, крысах, обезьянах и клеточных культурах человека - клетках в пробирке.
Все подходы к генной терапии старения делятся на те, где в организм доставляется ген долголетия, и на те, где вводятся малые РНК, «выключающие» ген или путь старения. То есть в первом случае вводится нечто полезное для долголетия, а во втором - отключается вредное. В строгом смысле исследований по генной терапии старения на млекопитающих до 2015 года было проведено только два.
Гораздо больше работ моделируют генную терапию на трансгенных мышах. В таких исследованиях терапевтический ген не доставляют в организм взрослой мыши, а при помощи генной инженерии создают мышей, геном которых изменен с рождения. Как и генная терапия, это позволяет исследовать, как увеличение или снижение активности разных генов влияет на продолжительность жизни и старение организма.
Давайте рассмотрим, что можно теоретически сделать с помощью генной терапии и генной инженерии для борьбы со старением.
Преимущество генной терапии перед другими способами продления жизни
Зачем нам генная терапия, если можно использовать препараты от старения (геропротекторы)? В сравнении с другими подходами к продлению жизни (например, геропротекторами или ограничением питания , продлевающими жизнь до 30-50%) генную терапию достаточно провести только один раз за всю жизнь, а таблетки нужно пить всё время и не забывать - иначе и результат будет не полным. Например, в работе Андржея Бартке 2001 года ограничение питания продлило жизнь мышам на 30% . Однако мыши употребляли низкокалорийную диету до 670 дней подряд - то есть каждый день, в течение половины своей жизни! Для большинства людей - это мало реально. А в эксперименте по генной терапии Марии Бласко (будет рассмотрено дальше в этой статье) 2012 года генная терапия теломеразой привела к немного меньшему эффекту - мыши стали жить дольше на 20%. Однако в этой работе мыши получили только 1 инъекцию лекарства в кровь за всю жизнь в довольно преклонном возрасте!Поэтому, если мы говорим о трансляции исследований по продлению жизни на человека, то генная терапия имеет абсолютное преимущество, поскольку не снижает качество жизни из-за необходимости постоянного лечения - соблюдать ежедневно определенную диету или же постоянно употреблять геропротекторы или другие лекарства. Также генная терапия высокотаргетна и поэтому имеет потенциал к меньшему числу побочных эффектов.
Кроме того, лекарственные средства имеют ограничения по биодоступности в различные ткани и органы.
Внедрение гена теломеразы (TERT) у двухлетних мышей дикого типа (40-50 лет по человеческим меркам) с помощью одной инъекции увеличивает длину теломеров и продлевает им жизнь на 20%.

Ученый предположил, что в клетках существует некий счетчик делений, ограничивающий их общее число. Спустя 10 лет российским ученым Алексеем Оловниковых был предложен гипотетический механизм работы этого счетчика.
Оловников предположил, что при делении клеток концы хромосом, называемые теломерами, немного сокращаются. А когда теломеры достигают критической длины, клетка перестает делиться и стареет. В дальнейшем Элизабет Элен Блэкбёрн - американский учёный-цитогенетик, стала лауреатом Нобелевской премии по физиологии или медицине за 2009 год совместно с Кэрол Грейдер и Джеком Шостаком с формулировкой «за открытие механизмов защиты хромосом теломерами и фермента теломеразы» по теории, в 1971 году предложенной Алексеем Оловниковым.
В нестареющих клетках (например, половых и эмбриональных стволовых), напротив, должен существовать фермент, который удлиняет теломеры, позволяя клеткам делиться практически до бесконечности. Кроме того, было показано, что повреждение гена теломеразы сильно сокращает жизнь модельных животных и приводит к возникновению синдрома преждевременного старения - прогерии.
После открытия теломеразы десятки ученых загорелись тем, чтобы сделать на ее основе лекарство от старости. Казалось бы, «включение» теломеразы во всех клетках может сделать организм бессмертным. Однако вскоре возникли опасения в связи с тем, что активный синтез теломеразы наблюдается и в 90% раковых опухолей. Встал вопрос: не приведет ли активация теломеразы к риску злокачественной трансформации?
Кроме того, оказалось, что старение клеток далеко не всегда сопровождается сокращением теломер. Например, в случае эпителиальных клеток слизистой полости рта или роговицы глаза человека. Это говорило о том, что одной активации теломеразы может быть недостаточно для омоложения всего организма. Перед тем как перейти к генной терапии, эффекты теломеразы исследовались на трансгенных мышах. Оказалось, что если «включить» ген TERT во всех клетках мыши, то продолжительность жизни увеличивается на 40%! Однако постоянная активность теломеразы увеличивала и риск рака. Поэтому стал вопрос о том, как активировать работу теломеразы на более короткий срок.

Именно это было сделано в работе Марии Бласко 2012 года (см. график). Ген теломеразы доставлялся в организм мыши при помощи аденоассоциированного вируса (AAV9), способного обеспечивать системную доставку. Аденоассоциированные вирусы характеризуются высокой безопасностью: они не встраивают доставляемый ген в геном хозяина, и поэтому не приводят к мутагенезу (нет риска рака). Кроме того, они почти не вызывают иммунный ответ. При этом, терапия геном TERT оказалась совершенно безопасной: риск рака у мышей не увеличивался. Двухлетним мышам делалась одна инъекция, с аденовирусом, к которому вставлен ген теломеразы. Это продлевало жизнь мышам на 20 % (как показано на графике выше). А это теоретически может позволить сделать людям в возрасте 40-50 лет одну инъекцию такого лекарства и продлить жизнь ещё на 8-12 лет.
Сегодня простимулировать теломеразу можно и лекарствами. Интересное исследование в этой области провели ученые из Университета Любляны (Словения) в 2016 году после ряда успешных клинических испытаний по омоложению сосудов низкими дозами валсартана и флувастатина. На этот раз они измерили активность теломеразы после омоложения сосудов в образцах крови 130 пациентов пациентов.
Так одномесячный курс существенно повышает активность теломеразы в 3.28 раза , которая достоверно коррелирует с улучшением эндотелиальной функции (омоложением сосудов) и снижением воспаления в кровеносных сосудах. И этот повышенный уровень теломеразы сохраняется, постепенно снижаясь, ещё полгода. Но насколько эффективно такое повышение теломеразы влияет на теломеры ещё предстоит определить.
 Важно знать, что теломеры не обязательно могут продлить нам жизнь, если подобную терапию делать не в нужный момент и слишком долго.
Важно знать, что теломеры не обязательно могут продлить нам жизнь, если подобную терапию делать не в нужный момент и слишком долго.
К тому же одна лишь стимуляция теломеразы может не удлинить теломеры. Активность теломеразы с возрастом почти не меняется - вот посмотрите график слева. А теломеры всё равно сокращаются.
 Также сегодня есть на рынке препарат, который повышает активность теломеразы - ТА-65. Он очень дорогой, а жизнь мышей никак не продлевал в исследованиях. Вот смотрите график слева. В исследовании 2011 года ученые из Испанского Национального Онкологического Центра начали давать долгоживущим двух летним мышам ТА-65 для повышения теломеразы, как и в предыдущем исследовании. Только в предыдущем исследовании мышам делали инъекцию для генной терапии. Но препарат ТА-65 никак не продлил жизнь мышам в отличие от генной терапии (см. график слева) и оказался абсолютно бесполезным для продления жизни и замедления старения.
Также сегодня есть на рынке препарат, который повышает активность теломеразы - ТА-65. Он очень дорогой, а жизнь мышей никак не продлевал в исследованиях. Вот смотрите график слева. В исследовании 2011 года ученые из Испанского Национального Онкологического Центра начали давать долгоживущим двух летним мышам ТА-65 для повышения теломеразы, как и в предыдущем исследовании. Только в предыдущем исследовании мышам делали инъекцию для генной терапии. Но препарат ТА-65 никак не продлил жизнь мышам в отличие от генной терапии (см. график слева) и оказался абсолютно бесполезным для продления жизни и замедления старения.
В 2011 году ученые из Техасского Университета исследовали теломеры и теломеразу в культурах клеток более 60 видов млекопитающих . Роль теломер в долголетии оказалось не так очевидна… Исследования показывают (при сравнении около 60 видов млекопитающих), чем длиннее теломеры у вида, тем быстрее накапливаются у него мутации ДНК, больше раковых опухолей и короче продолжительность жизни. Длина теломер обратно коррелирует с продолжительностью жизни. Это даёт основания предполагать, что результат по продлению жизни теломеразой, который был получен на мышах с помощью одной инъекции, может не продлить жизнь людям. Вопрос по теломерам для людей остаётся открытым.
Вывод: В будущем теоретически мы сможем с помощью внедрения гена теломеразы (TERT) в возрасте 40-50 лет с помощью одной инъекции увеличивать длину теломеров, но одной такой терапии явно недостаточно. Быстрее всего, мы должны найти сочетание генотерапевтических воздействий, чтобы существенно продлить жизнь человека. Сегодня мы можем имитировать эффект с помощью одномесячной терапии 1 раз в полгода комбинацией препаратов валсартана 20 мг + флувастатина 10-20 мг , либо телмисартан + аторвастатин 10 мг. По крайне мере эти препараты в комбинации способны стимулировать саму теломеразу.
Нарушение работы гена Agtr1a, кодирующего рецепторы ангиотензина AT1a продлевает жизнь трансгенным мышам на 26% в сравнении с мышами дикого типа.
Антагонисты рецепторов ангиотензина II, или блокаторы АТ1-рецепторов - одна из новых групп антигипертензивных средств (лекарства для лечения артериального давления). К таким лекарствам можно отнести все лекарства группы сартанов (например, телмисартан) .Каплан на примере приматов показал, что если собрать группу самцов приматов, то в течение скольких-то дней у обезьян появится социальная иерархия. Самое худшее место в такой иерархии - это внизу. Самцы приматов, находящиеся в подчиненном положении, демонстрируют ряд показателей хронического стресса. Часто у них возникает атеросклероз. Когда учёные давали самцам приматов, находящимся внизу социальной иерархии (группа риска), бета-блокатор пропранолол , подавляющий активность симпатической нервной системы, то атеросклероз сосудов не развивался.
Оказалось, что симпатическая нервная система из-за стресса негативно влияет на развитие атеросклероза и участвует в проблемах с сердцем и сосудами. Эмоциональный стресс реализует себя через симпатическую (адренергическую) автономную нервную систему, которая связывает управляющие центры нашего мозга и внутренние органы. В том числе - с иммунными, костным мозгом и др. Атеросклероз - главный фактор, который приводит к наибольшему число смертей в развитых странах от инфаркта сердца и инсульта мозга.
Рандомизированное, двойное слепое, плацебо-контролируемое исследование 1983 года , организованное Goldstein S и коллегами, показало, что терапия пропранололом у 3837 пациентов с острым инфарктом миокарда снижает смертность от сердечно-сосудистых заболеваний (причина смертности №1 в мире).
В марте 2017 года, французские ученые сообщили об успешных клинических исследованиях генной терапии для лечения серповидноклеточной анемии.
Комитет Американской Национальной Академии наук и Национальной Академии медицины дал поддержку редактирования генома человеческих эмбрионов уже в 2017 году . Но только для серьезных заболеваний и под строгим контролем.
Выводы
1. Все подходы к генной терапии старения делятся на те, где в организм доставляется ген долголетия, и на те, где «выключается» ген или путь старения.
2. В сравнении с другими подходами к продлению жизни генную терапию достаточно провести только один раз за всю жизнь.
3. Внедрение гена теломеразы (TERT), нарушение работы гена Agtr1a, нокаут GHRKO, нарушение в генах, кодирующих рецепторы к IGF-1, сверх экспрессия FGF21, нокаут AC5, удаление RIP3, редактирование гена PCSK9, сверх экспрессия Klotho, нокаут RAGE, сверх экспрессия BubR1, сверх экспрессия MTH1 - всё это примеры самых эффективных способов генной инженерии или генной терапии, позволяющих продлевать жизнь животным.
4. Чтобы добиться более существенных результатов в генной терапии старения и в генной инженерии против старения, необходимо комбинировать разные подходы. Добавить метки
Генная терапия - это лечение наследственных, ненаследственных, которое осуществляется путем введения в клетки пациента других генов. Целью терапии является устранение генных дефектов либо придание клеткам новых функций. Намного проще ввести в клетку здоровый, полноценно работающий ген, чем исправлять дефекты в имеющемся.
Генная терапия ограничивается исследованиями в соматических тканях. Это связано с тем, что любое вмешательство в половые и зародышевые клетки может дать совершенно непредсказуемый результат.
Применяемая в настоящее время методика эффективна при лечении как моногенных, так и мультифакториальных заболеваний (злокачественные опухоли, некоторые виды тяжелых сердечно-сосудистых, вирусных заболеваний).
Около 80% всех проектов генной терапии касаются ВИЧ-инфекции и В настоящее время ведутся исследования таких как гемофилия В, муковисцидоз, гиперхолестеринемия.
Лечение подразумевает:
· выделение и размножение отдельных типов клеток пациента;
· введение чужеродных генов;
· отбор клеток, в которых «прижился» чужеродный ген;
· вживление их больному (например, посредством переливания крови).
Генная терапия основывается на введении клонированных ДНК в ткани больного. Самыми эффективными методами при этом считаются инъекционные и аэрозольные вакцины.
Генная терапия работает в двух направлениях:
1. Лечение моногенных заболеваний. К ним относятся нарушения в работе головного мозга, которые связаны с какими-либо повреждениями клеток, которые вырабатывают нейромедиаторы.
2. Лечение Основные подходы, использующиеся в данной области:
· генетическое усовершенствование иммунных клеток;
· повышение иммунореактивности опухоли;
· блок экспрессии онкогенов;
· защита здоровых клеток от химиотерапии;
· ввод генов-супрессоров опухоли;
· производство противоопухолевых веществ здоровыми клетками;
· продукция противоопухолевых вакцин;
· локальное воспроизведение нормальных тканей при помощи антиоксидантов.
Использование генной терапии имеет много плюсов и в некоторых случаях является единственным шансом на нормальную жизнь для больных людей. Тем не менее, эта область науки до конца не изучена. Существует международный запрет на испытания на половых и доимплантационных зародышевых клетках. Это сделано с целью предотвращения нежелательных генных конструкций и мутаций.
Разработаны и общепризнанны некоторые условия, при которых допускаются клинические испытания:
Ген, перенесенный в клетки-мишени, должен быть активен продолжительное время.
В чужеродной среде ген должен сохранять свою эффективность.
Перенос гена не должен вызывать негативных реакций в организме.
Существует ряд вопросов, которые и сегодня остаются актуальными для многих ученых по всему миру:
Смогут ли ученые, работающие в области генной терапии, разработать полную генокоррекцию, которая не будет представлять угрозы потомству?
Будет ли необходимость и полезность генотерапевтической процедуры для отдельной супружеской пары превосходить риск этого вмешательства для будущего человечества?
Оправданы ли подобные процедуры, учитывая в будущем?
Каким образом будут соотноситься подобные процедуры на человеке с вопросами гомеостаза биосферы и общества?
В заключении можно отметить, что генетическая терапия на современном этапе предлагает человечеству пути лечения самых тяжелых заболеваний, которые совсем недавно считались неизлечимыми и смертельными. Однако, в то же время, развитие этой науки ставит перед учеными новые проблемы, которые необходимо решать уже сегодня.
Миодистрофия Дюшенна — одно из нечасто встречающихся, но все же относительно распространенных генетических заболеваний. Болезнь диагностируется в трех-пятилетнем возрасте, обычно у мальчиков, проявляясь поначалу лишь в затрудненных движениях, к десяти годам страдающий такой миодистрофией уже не может ходить, к 20−22 годам его жизнь заканчивается. Она вызвана мутацией гена дистрофина, который находится в Х-хромосоме. Он кодирует белок, соединяющий мембрану мышечной клетки с сократительными волокнами. Функционально это своеобразная пружина, обеспечивающая плавное сокращение и целостность клеточной мембраны. Мутации в гене приводят к дистрофии скелетных мышечных тканей, диафрагмы и сердца. Лечение заболевания носит паллиативный характер и позволяет лишь немного облегчить страдания. Однако с развитием генной инженерии появился свет в конце тоннеля.
О войне и мире
Генная терапия — это доставка внутрь клетки конструкций на основе нуклеиновых кислот для лечения генетических заболеваний. С помощью такой терапии можно исправить генетическую проблему на уровне ДНК и РНК, меняя процесс экспрессии нужного белка. Например, в клетку можно доставить ДНК с исправленной последовательностью, с которой синтезируется функциональный белок. Или, напротив, возможны удаления определенных генетических последовательностей, что также поможет уменьшить вредные последствия мутации. В теории это просто, однако на практике генная терапия базируется на сложнейших технологиях работы с объектами микромира и представляет собой совокупность передовых ноу-хау в области молекулярной биологии.
 Инъекция ДНК в пронуклеус зиготы — одна из самых ранних и наиболее традиционных технологий создания трансгенов. Инъекция производится вручную с помощью сверхтонких игл под микроскопом с 400-кратным увеличением.
Инъекция ДНК в пронуклеус зиготы — одна из самых ранних и наиболее традиционных технологий создания трансгенов. Инъекция производится вручную с помощью сверхтонких игл под микроскопом с 400-кратным увеличением.
«Ген дистрофина, мутации которого порождают миодистрофию Дюшенна, огромный, — рассказывает директор по развитию биотехнологической компании «Марлин Биотех», кандидат биологических наук Вадим Жерновков. — Он включает в себя 2,5 млн пар нуклеотидов, что можно было бы сравнить с количеством букв в романе «Война и мир». И вот представим себе, что мы вырвали из эпопеи несколько каких-то важных страниц. Если на этих страницах описываются существенные события, то понимание книги было бы уже затруднено. Но с геном все сложнее. Найти другую копию «Войны и мира» несложно, и тогда недостающие страницы можно было бы прочитать. Но ген дистрофина находится в X-хромосоме, а у мужчин она одна. Таким образом, в половых хромосомах у мальчиков при рождении хранится лишь одна копия гена. Другую взять негде.

Наконец, при синтезе белка из РНК важно сохранение рамки считывания. Рамка считывания определяет, какая группа из трех нуклеотидов считывается как кодон, что соответствует одной аминокислоте в белке. Если произошло удаление в гене фрагмента ДНК, не кратное трем нуклеотидам, происходит сдвиг рамки считывания — кодировка изменяется. Это можно было бы сравнить с ситуацией, когда после вырванных страниц во всей оставшейся книге все буквы заменятся на следующие по алфавиту. Получится абракадабра. Вот то же самое происходит с неправильно синтезируемым белком».
Биомолекулярный пластырь
Один из эффективных методов генной терапии для восстановления нормального синтеза белка — пропуск экзонов с помощью коротких нуклеотидных последовательностей. В «Марлин Биотех» уже отработана технология работы с геном дистрофина с помощью такого метода. Как известно, в процессе транскрипции (синтеза РНК) сначала формируется так называемая прематричная РНК, заключающая в себе как кодирующие белок участки (экзоны), так и некодирующие (интроны). Далее начинается процесс сплайсинга, в ходе которого интроны и экзоны разъединяются и формируется «зрелая» РНК, состоящая только из экзонов. В этот момент некоторые экзоны можно заблокировать, «залепить» с помощью особых молекул. В итоге в зрелой РНК не окажется тех кодирующих участков, от которых мы предпочли бы избавиться, и таким образом восстановится рамка считывания, белок будет синтезироваться.

«Эту технологию мы отладили in vitro, — рассказывает Вадим Жерновков, то есть на клеточных культурах, выращенных из клеток пациентов с миодистрофией Дюшенна. Но отдельные клетки — это не организм. Вторгаясь в процессы клетки, мы должны наблюдать последствия вживую, однако привлечь к испытаниям людей не представляется возможным по разным причинам — от этических до организационных. Поэтому возникла необходимость получения модели миодистрофии Дюшенна с определенными мутациями на основе лабораторного животного».
Как уколоть микромир
Трансгенные животные — это полученные в лаборатории животные, в геном которых целенаправленно, осознанно внесены изменения. Еще в 70-е годы прошлого века стало понятно, что создание трансгенов — это важнейший метод исследования функций генов и белков. Одним из самых ранних методов получения полностью генно-модифицированного организма стала инъекция ДНК в пронуклеус («предшественник ядра») зигот оплодотворенных яйцеклеток. Это логично, так как модифицировать геном животного проще всего в самом начале его развития.
 На схеме продемонстрирован процесс CRISPR/Cas9, в котором участвуют субгеномная РНК (sgRNA), ее участок, работающий как РНК-гид, а также белок-нуклеаза Cas9, который рассекает обе нити геномной ДНК в указанном РНК-гидом месте.
На схеме продемонстрирован процесс CRISPR/Cas9, в котором участвуют субгеномная РНК (sgRNA), ее участок, работающий как РНК-гид, а также белок-нуклеаза Cas9, который рассекает обе нити геномной ДНК в указанном РНК-гидом месте.
Инъекция в ядро зиготы — весьма нетривиальная процедура, ведь речь идет о микромасштабах. Яйцеклетка мыши имеет диаметр 100 мкм, а пронуклеус — 20 мкм. Операция происходит под микроскопом с 400-кратным увеличением, однако инъекция — это самая что ни на есть ручная работа. Разумеется, для «укола» применяется не традиционный шприц, а специальная стеклянная игла с полым каналом внутри, куда набирается генный материал. Один ее конец можно держать в руке, а другой — сверхтонкий и острый — практически не виден невооруженным глазом. Конечно, такая хрупкая конструкция из боросиликатного стекла не может храниться долго, поэтому в распоряжении лаборатории есть набор заготовок, которые непосредственно перед работой вытягиваются на специальном станке. Используется особая система контрастной визуализации клетки без окрашивания — вмешательство в пронуклеус само по себе травматично и является фактором риска для выживания клетки. Краска стала бы еще одним таким фактором. К счастью, яйцеклетки достаточно живучи, однако количество зигот, которые дают начало трансгенным животным, составляют лишь несколько процентов от общего числа яйцеклеток, в которые была сделана инъекция ДНК.
Следующий этап — хирургический. Проводится операция по трансплантации микроинъецированных зигот в воронку яйцевода мыши-реципиента, которая станет суррогатной матерью будущим трансгенам. Далее лабораторное животное естественным путем проходит цикл беременности, и на свет появляется потомство. Обычно в помете находится около 20% трансгенных мышат, что также говорит о несовершенстве метода, ибо в нем присутствует большой элемент случайности. При инъекции исследователь не может контролировать, как именно внедренные фрагменты ДНК встроятся в геном будущего организма. Высока вероятность таких комбинаций, которые приведут к гибели животного еще на эмбриональной стадии. Тем не менее метод работает и вполне годен для ряда научных целей.
 Развитие трансгенных технологий позволяет производить животные белки, востребованные фармацевтической промышленностью. Эти белки экстрагируются из молока трансгенных коз и коров. Также есть технологии получения специфических белков из куриного яйца.
Развитие трансгенных технологий позволяет производить животные белки, востребованные фармацевтической промышленностью. Эти белки экстрагируются из молока трансгенных коз и коров. Также есть технологии получения специфических белков из куриного яйца.
Ножницы для ДНК
Но есть более эффективный способ на основе целевого редактирования генома по технологии CRISPR/Cas9. «Сегодня молекулярная биология в чем-то подобна эпохе дальних морских экспедиций под парусами, — говорит Вадим Жерновков. — Практически каждый год в этой науке происходят значительные открытия, которые могут изменить нашу жизнь. Например, несколько лет назад микробиологи обнаружили у давно, казалось бы, изученного вида бактерий иммунитет к вирусным инфекциям. В результате дальнейших исследований выяснилось, что ДНК бактерий содержат в себе особые локусы (CRISPR), с которых синтезируются фрагменты РНК, умеющие комплементарно связываться с нуклеиновыми кислотами чужеродных элементов, например с ДНК или РНК вирусов. С такой РНК связывается белок Cas9, представляющий собой фермент-нуклеазу. РНК служит для Cas9 гидом, помечающим определенный участок ДНК, в котором нуклеаза совершает разрез. Примерно три-пять лет назад появились первые научные труды, в которых разрабатывалась технология CRISPR/Cas9 для редактирования генома».
 Трансгенные мыши позволяют создавать живые модели тяжелых генетических заболеваний человека. Люди должны быть благодарны этим крохотным существам.
Трансгенные мыши позволяют создавать живые модели тяжелых генетических заболеваний человека. Люди должны быть благодарны этим крохотным существам.
По сравнению со способом введения конструкции для случайного встраивания, новый метод позволяет подобрать элементы системы CRISPR/Cas9 таким образом, чтобы точно нацелить РНК-гиды на нужные участки генома и добиться целенаправленной делеции или вставки нужной последовательности ДНК. В этом методе тоже возможны ошибки (РНК-гид иногда соединяется не с тем участком, на который его нацеливают), однако при использовании CRISPR/Cas9 эффективность создания трансгенов составляет уже около 80%. «Этот метод имеет широкие перспективы, и не только для создания трансгенов, но и в других областях, в частности в генной терапии, — говорит Вадим Жерновков. — Однако технология находится только в начале пути, и представить себе, что в ближайшее время исправлять генный код людей будут с помощью CRISPR/Cas9, довольно сложно. Пока есть вероятность ошибки, есть и опасность, что человек лишится какой-то важной кодирующей части генома».

Молоко-лекарство
Российской компании «Марлин Биотех» удалось создать трансгенную мышь, в которой полностью воспроизведена мутация, приводящая к миодистрофии Дюшенна, и следующим этапом станут испытания технологий генной терапии. Вместе с тем создание моделей генетических заболеваний человека на основе лабораторных животных — не единственное возможное применение трансгенов. Так, в России и западных лабораториях ведутся работы в области биотехнологий, позволяющие получать важные для фарминдустрии лекарственные белки животного происхождения. В качестве продуцентов могут выступать коровы или козы, у которых можно изменять клеточный аппарат производства содержащихся в молоке белков. Из молока можно экстрагировать лекарственный белок, который получен не химическим способом, а с помощью природного механизма, что повысит эффективность лекарства. В настоящее время разработаны технологии получения таких лекарственных белков, как лактоферрин человека, проурокиназа, лизоцим, атрин, антитромбин и другие.
Генная терапия – одна из стремительно развивающихся областей медицины, которая предполагает лечение человека посредством введения в организм здоровых генов. Причем, как утверждают ученые, с помощью генной терапии можно добавить недостающий ген, исправить или заменить его, улучшив тем самым работу организма на клеточном уровне и нормализовав состояние больного.
По словам ученых, потенциальными кандидатами для генной терапии на сегодняшний день являются 200 млн. жителей планеты, причем эта цифра неуклонно растет. И очень отрадно, что несколько тысяч пациентов уже получили лечение от неизлечимых недугов в рамках проводимых испытаний.
В данной статье расскажем о том, какие задачи ставит перед собой генная терапия, какие заболевания можно лечить этим методом и с какими проблемами приходится сталкиваться ученым.
Где применяется генотерапия
Изначально генная терапия была задумана для борьбы с тяжелыми наследственными заболеваниями, такими как болезнь Хантингтона, муковисцидоз (кистозный фиброз) и некоторыми инфекционными заражениями. Однако 1990-й год, когда ученым удалось скорректировать дефектный ген, и, введя его в организм больного, победить муковисцидоз, стал поистине революционным в области генной терапии. Миллионы людей во всем мире получили надежду на лечение заболеваний, которые прежде считались неизлечимыми. И пусть такая терапия находится у самых истоков развития, ее потенциал вызывает удивление даже в научном мире.
Так, например, кроме кистозного фиброза, современные ученые добились успехов борьбе с такими наследственными патологиями, как гемофилия, энзимопатия и иммунодефицит. Более того, лечение генами позволяет бороться с некоторыми онкологическими заболеваниями, а также с патологиями сердца, болезнями нервной системы и даже травмами, к примеру, с повреждениями нервов. Таким образом, генная терапия занимается заболеваниями с крайне тяжелым протеканием, которые приводят к ранней смертности и, зачастую, не имеют другого лечения, кроме терапии генами.
Принцип лечения генами
В качестве действующего вещества врачи используют генетическую информацию, а если быть точным, молекулы, которые являются носителями такой информации. Реже для этого применяют нуклеиновые кислоты РНК, а чаще – клетки ДНК.
Каждая такая клетка обладает так называемым «ксероксом» – механизмом, при помощи которого она переводит генетическую информацию в белки. Клетка, у которой имеется правильный ген и без сбоев работает «ксерокс», с точки зрения генной терапии является здоровой клеткой. У каждой здоровой клетки имеется целая библиотека оригинальных генов, которые она использует для правильной и слаженной работы всего организма. Однако если по какой-либо причине важный ген утерян, восстановить такую потерю не представляется возможным.
Это становится причиной развития серьезных генетических заболеваний, таких как миодистрофия Дюшена (при ней у больного прогрессирует мышечный паралич, и он в большинстве случаев не доживает до 30 лет, умирая от остановки дыхания). Или менее фатальная ситуация. К примеру, «поломка» определенного гена приводит к тому, что белок перестает выполнять свои функции. И это становится причиной развития гемофилии.
В любом из перечисленных случаев на помощь приходит генная терапия, задачей которой является доставить нормальную копию гена в больную клетку и подложить в её в клеточный «ксерокс». В этом случае наладится работа клетки, а может быть, восстановится функционирование всего организма, благодаря чему человек избавится от тяжелого недуга и сможет продлить свою жизнь.

Какие болезни лечит генная терапия
Насколько реально помогает человеку генная терапия? По подсчетам ученых, в мире насчитывается около 4200 заболеваний, которые возникают в результате неправильной работы генов. В этом плане потенциал у данного направления медицины просто невероятный. Однако гораздо важнее то, чего на сегодняшний день удалось добиться медикам. Безусловно, на этом пути хватает трудностей, однако уже сегодня можно выделить ряд локальных побед.
К примеру, современные ученые разрабатывают подходы к лечению ишемической болезни сердца посредством генов. А ведь это невероятно распространенное заболевание, которое поражает гораздо больше людей, чем врожденные патологии. В конечном итоге, человек, столкнувшийся с ишемической болезнью, оказывается в таком состоянии, когда единственным спасением для него может стать генная терапия.
Более того, на сегодняшний день при помощи генов лечатся патологии, связанные с поражением центральной нервной системы. Это такие заболевания, как боковой амиотрофический склероз, болезнь Альцгеймера или болезнь Паркинсона. Что интересно, для лечения перечисленных недугов используются вирусы, которые имеют свойство атаковать нервную систему. Так, при помощи вируса герпеса в нервную систему доставляют цитокины и факторы роста, замедляющие развитие заболевания. Это яркий пример того, как патогенный вирус, который обычно вызывает болезнь, обрабатывается в лабораторных условиях, лишаясь белков, несущих заболевание, и используется как кассета, которая доставляет в нервы целебные вещества и тем самым действует во благо здоровья, продлевая жизнь человека.
Еще одним тяжелым наследственным заболеванием является холестеринемия, которая приводит организм человека к неспособности регулировать холестерин, вследствие чего в его организме скапливаются жиры, и возрастает риск инфарктов и инсультов. Чтобы справиться с этой проблемой, специалисты удаляют больному часть печени и исправляют поврежденный ген, останавливая дальнейшее накопление холестерина организмом. После этого исправленный ген помещают в обезвреженный вирус гепатита, и с его помощью отправляют обратно в печень.
Читайте также:
Имеются положительные подвижки и в борьбе со СПИДом. Не секрет ведь, что СПИД вызывается вирусом иммунодефицита человека, который разрушает иммунную систему и открывает ворота к организму смертельно опасным заболеваниям. Современные ученые уже знают, каким образом изменить гены, чтобы они перестали ослаблять иммунную систему, а начали укреплять ее для противодействия вирусу. Такие гены вводятся через кровь, посредством ее переливания.
Работает генная терапия и против раковых заболеваний, в частности, против рака кожи (меланомы). Лечение таких пациентов предполагает введение генов с факторами некроза опухоли, т.е. генов, которые содержат противоопухолевый белок. Более того, сегодня проводятся испытания по лечению рака мозга, где больным пациентам вводят ген, содержащий информацию по увеличению чувствительности злокачественных клеток к применяемым препаратам.
Болезнь Гоше представляет собой тяжелейшее наследственное заболевание, которое вызывается мутацией гена, подавляющего производство особого фермента – глюкоцереброзидазы. У лиц, страдающих от этого неизлечимого недуга, увеличена селезенка и печень, а с прогрессированием недуга начинают разрушаться кости. Ученым уже сегодня удались опыты по введению в организм таких пациентов гена, содержащего информацию по выработке данного фермента.
А вот еще один пример. Не секрет, что ослепший человек на всю оставшуюся жизнь лишается возможности воспринимать зрительные образы. Одной из причин врожденной слепоты считается так называемая атрофия Лебера, которая, по сути, является генной мутацией. На сегодняшний день ученые вернули 80 слепым людям зрительные способности, посредством модифицированного аденовируса, который доставил «рабочий» ген в ткани глаза. К слову, несколько лет назад ученым удалось вылечить дальтонизм у подопытных обезьян, путем внедрения в сетчатку глаза животного здорового человеческого гена. А совсем недавно такая операция позволила вылечить дальтонизм первым пациентам.
Что характерно, метод доставки генной информации при помощи вирусов является самым оптимальным, так как вирусы сами находят свои цели в организме (вирус герпеса обязательно найдет нейроны, а вирус гепатита – печень). Однако у данного метода доставки генов есть существенный недостаток – вирусы иммуногены, а значит, при попадании в организм могут быть уничтожены иммунитетом до того, как успеют сработать, а то и вызовут мощные иммунные ответы организма, лишь ухудшив состояние здоровья.
Существует и другой способ доставки генного материала. Это кольцевая молекула ДНК или плазмида. Она отлично спирализуется, становясь очень компактной, что позволяет ученым «упаковать» ее в химический полимер и внедрить в клетку. В отличие от вируса, плазмида не вызывает иммунной реакции организма. Однако этот способ менее подходящий, т.к. спустя 14 дней плазмида удаляется из клетки и продукция белка останавливается. То есть, таким способом ген необходимо вводить на протяжении длительного времени, пока клетка будет «выздоравливать».
Таким образом, у современных ученых есть два мощных метода доставки генов к «больным» клеткам, причем использование вирусов выглядит более предпочтительным. В любом случае окончательное решение по выбору того или иного метода выбирает врач, исходя из реакции организма пациента.
Проблемы, с которыми сталкивается генотерапия
Можно сделать определенный вывод о том, что генная терапия – малоизученная область медицины, которая сопряжена с большим количеством неудач и побочных эффектов, и в этом ее огромный недостаток. Однако есть еще и этический вопрос, ведь многие ученые выступают категорически против вмешательства в генетическое строение человеческого организма. Именно поэтому, сегодня существует международный запрет на использование в генотерапии половых клеток, а также доимплантационных зародышевых клеток. Сделано это для того, чтобы предотвратить нежелательные генные изменения и мутации у наших потомков.
В остальном же, генная терапия не нарушает никаких этических норм, ведь она призвана бороться с тяжелыми и неизлечимыми заболеваниями, в которых официальная медицина попросту бессильна. И в этом самое главное преимущество лечения генами.
Берегите себя!