Гиалиноз мелкой артерии мозга. Гиалиноз: что это, развитие, локализации и характеристика, последствия
Читайте также
Дистрофия (от греч. dys - нарушение и trophe - питаю) - сложный патологический процесс, в основе которого лежит нарушение тканевого (кле- точного) метаболизма, ведущее к структурным изменениям Поэтому дистро- фии рассматриваются как один из видов повреждения. Употреблявшийся ра- нее для обозначения дистрофического процесса термин «дегенерация» (от лат. degenerare - перерождение) не отражает его сущности.
Под трофикой понимают совокупность механизмов, определяющих мета- болизм и структурную организацию ткани (клетки), которые необходимы для отправления специализированной функции. Среди этих механизмов выделяют клеточные и внеклеточные (рис. 1). Клеточные механизмы обеспечи- ваются структурной организацией клетки и ее ауторегуляцией. Это значит, что трофика клетки в значительной мере является свойством самой клетки как сложной саморегулирующейся системы. Жизнедеятельность клетки обес- печивается «окружающей средой» и регулируется с помощью ряда систем ор- ганизма. Поэтому внеклеточные механизмы трофики располагают транс- портными (кровь, лимфа, микроциркуляторное русло) и интегративными (нейроэндокринные, нейрогуморальные) системами ее регуляции.
Из сказанного становится понятным, что непосредственной причинойразви- тия дистрофий могут служить нарушения как клеточных, так и внеклеточных механизмов, обеспечивающих трофику.
Рис. I. Механизмы регуляции трофики (по М. Г. Балш).
1. Расстройства ауторегуляции клетки, которые могут быть вызваны различными факторами (гиперфункция, токсические вещества, радиа- ция, наследственная недостаточность или отсутствие фермента и т. д.), ведут к энергетическому ее дефициту и к нарушению фермента- тивных процессов в клетке. Ферментопатия, или энзимопатия (приобретенная или наследственная), становится основным патогенетическим звеном и выражением дистрофии при нарушениях клеточных механизмов трофики.
Концепция наследственных ферментопатий принадлежит французскому исследователю Гар- ро, который рассматривал наследственные нарушения обмена как состояния, при которых из-за отсутствия определенного фермента блокируется соответствующее звено реакции, составляющей часть метаболического пути. В результате этого продукты обмена, образовавшиеся до блокиро- ванной реакции, накапливаются в клетках и тканях, а метаболиты, которые должны были бы образоваться на последующих этапах, не образуются.
В настоящее время известно много процессов и болезней, относящихся к наследственным ферментопатиям и называемых болезнями накопления, или тезаурисмозами (от греч. tesauros - запас). Вместе с тем природа нарушений, лежащих в основе ферментопатий не- однозначна. В одних случаях механизм заключается в синтезе ферментного белка с измененной структурой, каталитические свойства которого нарушены, в других - в синтезе варианта фер- мента, который нестоек и быстро распадается, в третьих - может иметь место полное прекра- щение синтеза ферментного белка.
2. Нарушения работы транспортных систем, обеспечиваю- щих метаболизм и структурную сохранность тканей (клеток), вызывает ги- поксию, которая является ведущей в патогенезе дисциркуляторных дистрофий.
З.При расстройствах эндокринной регуляции трофики (тиреотоксикоз, диабет, гиперпаратиреоз и т. д.) можно говорить об эндо- кринных, а при нарушении нервной регуляции трофики (нарушен- ная иннервация, опухоль головного мозга и т. д.) - о нервных, или цере- бральных, дистрофиях.
Особенности патогенеза внутриутробных дистрофий опреде- ляются непосредственной связью их с болезнями матери. В исходе при гибели части зачатка органа или ткани может развиться необратимый порок развития.
При дистрофиях в клетках и (или) межклеточном веществе накапливаются различные продукты" обмена (белки, жиры, углеводы, минералы, вода), ко- торые характеризуются количественными или качественными изменениями в результате нарушения ферментативных процессов.
Среди морфогенетических механизмов, ведущих к развитию характерных для дистрофий изменений, различают инфильтрацию, декомпозицию (фане- роз), извращенный синтез и трансформацию. Инфильтрация - избыточ- ное проникновение продуктов обмена из крови и лимфы в клетки или межкле- точное вещество с последующим их накоплением в связи с недостаточностью ферментных систем, метаболизирующих эти продукты. Таковы, например, ин- фильтрация грубодисперсным белком эпителия проксимальных канальцев почек при нефротическом синдроме, инфильтрация холестерином, его эфи- рами и липопротеидами интимы аорты и крупных артерий при атеро- склерозе.
Декомпозиция (фанероз) - распад ультраструктур клеток и меж- клеточного вещества, ведущий к нарушению тканевого (клеточного) метабо- лизма и накоплению продуктов нарушенного обмена в ткани (клетке). Таковы жировая дистрофия кардиомиоцитов при дифтерийной интоксикации, фибри- ноидное набухание соединительной ткани при ревматических болезнях.
Извращенный синтез - это синтез в клетках или в тканях веществ, не встречающихся в них в норме. К ним относятся: синтез аномального белка амилоида в клетке и аномальных белково-полисахаридных комплексов ами- лоида в межклеточном веществе; синтез белка алкогольного гиалина гепато- цитом; синтез гликогена в эпителии узкого сегмента нефрона при сахарном диабете.
Трансформация - образование продуктов одного вида обмена из об- щих исходных продуктов, которые идут на построение белков, жиров, и угле- водов. Гакова, например, трансформация компонентов жиров и углеводов в белки, усиленная полимеризация глюкозы в гликоген и др.
Инфильтрация и декомпозиция - ведущие морфогенетические механизмы дистрофий - часто являются последовательными стадиями в их развитии. Од- нако в некоторых органах и тканях в связи со структурно-функциональными их особенностями преобладает какой-либо один из морфогенетических меха- низмов (инфильтрация - в эпителии почечных канальцев, декомпозиция - в клетках миокарда), что позволяет говорить об ортологии (от греч. ort- hos - прямой, типичный) дистрофий.
Морфологическая специфика дистрофий при изучении их на разных уров- нях - ультраструктурном, клеточном, тканевом, органном - проявляется не- однозначно. Ультраструктурная морфология дистрофий не имеет какой-либо специфики, однако возможность выявления ряда продуктов обмена (липиды, гликоген, ферритин) позволяет говорить об" ультраструк- турных изменениях, характерных для того или иного вида дистрофий.
Это связано с тем, что изменения органелл клеток различных органов и тканей при разных воздействиях однотипны. Правда, степень этих изменений в одной клетке и особенно в группах соседних клеток неодинакова (мозаичность изменений ультраструктур), а чувствительность раз- ных органелл клетки к воздействию различна (наиболее чувствительны митохондрии и эндо- плазматическая сеть). К тому же ультраструктурная морфология дистрофий отражает не только повреждение органелл, но и их репарацию (внутриклеточная регенерация). Таким образом, ста- новятся понятными общность и разнообразие ультраструктурных изменений при разных дистрофиях.
Характерная морфология дистрофий выявляется, как правило, на кле- точном и тканевом уровнях, хотя для доказательства связи дистро- фии с нарушениями того или иного вида обмена требуется применение гисто- химических методов. Без установления качества продукта нарушенного обмена нельзя верифицировать тканевую дистрофию, т. е. отнести ее к бел- ковым, жировым, углеводным или другим. Изменения органа при ди- строфии (размер, цвет, консистенция, структура на разрезе) в одних случаях представлены исключительно ярко, в других отсутствуют, и лишь микроско- пическое исследование позволяет выявить их специфичность. В ряде случаев можно говорить осистемномхарактере изменений при дистрофии (си- стемный гемосидероз, системный мезенхимальный амилоидоз, системный липоидоз).
В классификации дистрофий придерживаются нескольких принципов. I. В зависимости от преобладания морфологических изменений в специа- лизированных элементах паренхимы или строме и сосудах: 1) паренхима- тозные; 2) мезенхимальные; 3) смешанные.
II. По преобладанию нарушений того или иного вида обмена: 1) бел- ковые; 2.) жировые; 3) углеводные; 4) минеральные.
В зависимости от влияния генетических факторов: 1) приобретенные; 2) наследственные.
По распространенности процесса: 1) общие; 2) местные.
ПАРЕНХИМАТОЗНЫЕ ДИСТРОФИИ
Паренхиматозные дистрофии - проявления нарушений обмена в высокоспециализированных в функциональном отношении клетках.
Клетка представляет собой сложную гетерогенную саморегулирующуюся систему, в кото- рой многие процессы осуществляются по типу разветвленных цепных реакций. Эти процессы на- правлены на выполнение специализированной функции. При этом элементы клетки выполняют строго определенные функции: мембранная система осуществляет транспорт веществ, эндоплаз- матическая сеть и рибосомы синтезируют «полуфабрикаты», комплекс Гольджи секретирует окончательный продукт, лизосомы осуществляют клеточное пищеварение, митохондрии - выра- ботку энергии, ядро и ядрышко - генетическое кодирование специфической функции и сохран- ность клеточной популяции. Однако эти элементы строго координированы в своей деятельно- сти, причем координация в выработке специфического продукта клетки подчинена закону «внутриклеточного конвейера», который осуществляет взаимосвязь между структурными компо- нентами клетки (главным образом эндоплазматической сетью, комплексом Гольджи и лизосо- мами) и протекающими в ней процессами обмена. В итоге образуются те или иные вещества, определяющие функциональную специфику клетки. Большую роль в ауторегуляции клетки при- дают генам-репрессорам, осуществляющим «координационное торможение» функций различных ультрастуктур.
В зависимости от нарушений того или иного вида обмена паренхима- тозные дистрофии делят на белковые (диспротеинозы), жировые (липи- дозы) и углеводные.
Паренхиматозные белковые дистрофии (диспротеинозы)
Большая часть белков цитоплазмы (простых и сложных) находится в соединении с липидами, образуя липопротеидные комплексы. Эти комп- лексы составляют основу мембран митохондрий, эндоплазматической сети, комплекса Гольджи и других структур. Помимо связанных белков, в цито- плазме содержатся и свободные. Многие из последних обладают функцией ферментов.
Сущность паренхиматозных диспротеинозов состоит в том, что изменяют- ся физико-химические и морфологические свойства белков клетки - они под- вергаются денатурации и коагуляции или, наоборот, колликвации, что ведет
к гидратации цитоплазмы. В тех случаях, когда нарушаются связи белков с липидами, возникает деструкция мембранных структур клетки.
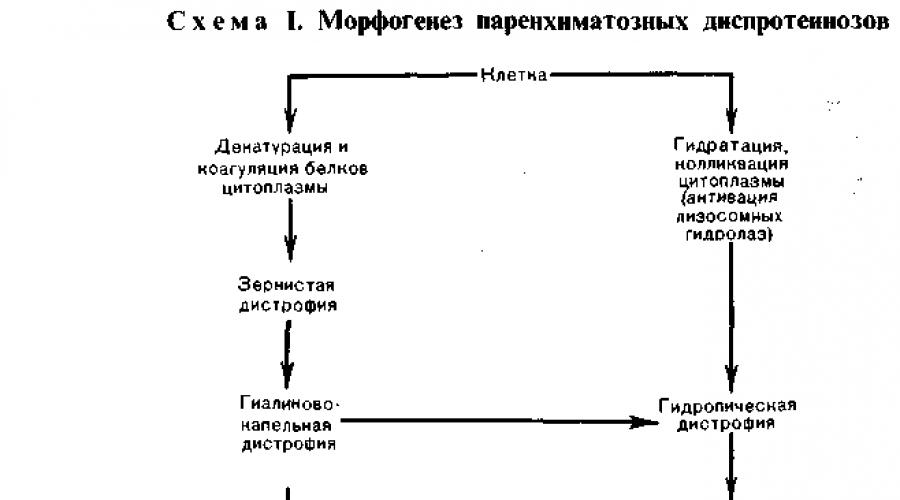
К паренхиматозным диспротеинозам относят зернистую, гиалиново-ка- пельную, гидропическую и роговую дистрофии. Эти дистрофии нередко пред- ставляют собой последовательные этапы нарушений метаболизма белков ци- топлазмы в зависимости от преобладания денатурации и коагуляции, или гидратации и колликвации цитоплазмы. В исходе этих нарушений может раз- виться коагуляционныи (сухой) или колликвационный (влажный) некроз (схема I).

Зернистая дистрофия характеризуется появлением в цитоплазме большого числа зерен белковой природы. Это самый частый вид дистрофии среди диспротеинозов. Процесс бывает наиболее ярко выражен в печени, почках и сердце.
Микроскопическая картина: клетки печени, эпителия извитых канальцев по- чек, мышечных волокон сердца изменяются. Они увеличиваются, набухают, цитоплазма их становится мутной, богатой белковыми гранулами или капля- ми, хорошо выявляемыми гистохимическими методами (реакции Даниелли и Милона) и с помощью электронного микроскопа. Электронно-микроскопи- ческое исследование позволяет выявить в таких случаях набухание или вакуо- лизацию митохондрий (рис. 2), а также расширенные цистерны эндоплазмати- ческой сети, в которых определяются скопления белков; отмечается деструкция мембран.
Внешний вид органов при зернистой дистрофии весьма характерен: они не- сколько увеличены, имеют дряблую консистенцию, на разрезе ткань выбухает, лишена обычного блеска, тусклая, мутная. На основании этих признаков го- ворят о тусклом, или мутном, набухании органов.

Следует иметь в виду, что картина, сходная с мутным набуханием, может быть результатом трупных изменений. О прижизненное™ процесса в таких случаях можно судить по увеличению размеров клеток, которое нехарактерно для трупных изменений.
Причины зернистой дистрофии разнообразны: расстройства кровообраще- ния (застойное полнокровие, стазы и др.) и лимфообращения, инфекции (тифы, скарлатина, дифтерия и др.), интоксикации и другие факторы, которые могут вести к снижению интенсивности окислительных процессов, энергетиче- скому дефициту клетки, накоплению в ней кислых продуктов и денатурации белков цитоплазмы.
Механизм появления белковых зерен в цитоплазме сложен и связан с мно- гими процессами, значение которых различно.
Появление белковых зерен в цитоплазме не всегда позволяет рассматривать этот процесс как дистрофический, он может отражать как структурно-функциональные особен- ности клетки в физиологических условиях (образование секреторных гранул, например, клетками островков поджелудочной железы, передней доли гипофиза, юкстагломерулярного ап- парата; физиологическую резорбцию белков, например, эпителием проксимальных канальцев почек, слизистой оболочки тонкой кишки и т. д.), так и усиление белоксинтезирую- щ е й функции (синтез белков гепатоцитами, секреторными клетками поджелудочной железы).
Накопление гранул белков в клетке как выражение дистрофии мо- жет быть связано с механизмами инфильтрации (инфильтрация эпителия проксимальных и дистальных канальцев почек), декомпозиции - при де- струкции мембранных структур клетки (например, в миокарде), трансфор- мации компонентов исходных продуктов углеводов и жиров в белки (напри- мер, в гепатоцитах).
Важно подчеркнуть, что при декомпозиции нарушается обмен не только белков, но и липидов. В связи с этим иногда трудно провести четкую грань между белковой (зернистой) и жировой дистрофией; нередко вторая сменяет первую.
Исход зернистой дистрофии различный. В большинстве случаев она обра- тима, но если вызвавшие ее причины не устранены, возможен ее переход в гиалиново-капельную, гидропическую или жировую дистрофию.

Функциональное значение зернистой дистрофии невелико и может про- являться в изменении, в частности некотором ослаблении функции пора- женных органов.
Гиалиноз – вид диспротеиноза, при котором в ткани образуются однородные полупрозрачные плотные массы (гиалин), напоминающие гиалиновый хрящ. Гиалин состоит из 1. фибриллярный белок; 2. белки плазмы; 3. иммунные комплексы; 4. липиды. Окраски: 1. кислые красители (эозин, кислый фуксин); 2. пикрофуксин по ван Гизон – красный или желтый цвет; 3. положительная ШИК-реакция. Виды гиалиноза: 1. внутриклеточный (русселевские тельца при хроническом воспалении, образуются из плазматических клеток в слизистых оболочках); 2. физиологический (сосуды матки после родов, ткань яичников в старческом возрасте); 3. мертвых материалов (гиалиновые тромбы, гиалиновые цилиндры в канальцах почки) 4. гиалиноз (гиалиновая дистрофия) стенок сосудов (наибольшее значение имеет гиалиноз артериол при гипертонической болезни) и соединительной ткани. Виды гиалина: 1. простой (при гипертонической болезни); 2. сложный (при ревматизме); 3. липогиалин (при сахарном диабете). Причины: развивается в исходе 1. плазматического пропитывания; 2. фибриноидного набухания; 3. склероза и некроза.
Морфогенез и значение: артериол 1. нейрогенный спазм артериол; 2. повреждение эндотелия, аргирофильных мембран(вид соединительнотканных волокон, способных связывать соли серебра) и гладкомышечных волокон; 3. повышение проницаемости стенки сосуда; 4. плазморрагия – пропитывание стенки сосуда плазменными белками; 5. коагуляция и уплотнение белка с образованием плотного гиалиноподобного вещества. Значение- Вызывает значительные нарушения функции почек – развитие хронической почечной недостаточности, уремии. Соед.тк: 1. деструкция коллагена; 2. пропитывание ткани плазмен–ными белками и полисахаридами; 3. превращение соединительно–тканных пучков в однородную плотную хрящеподобную массу. Значение- Значительное функциональное нарушение, потеря эластичности, деформация.
Гиалиноз может явиться проявлением общих нарушений белкового обмена, однако чаще всего это местный очаговый или же системный (в сосудах) дистрофический процесс; Гиалиноз проявляется как в физиол., так и в патологический условиях.
Понятие «гиалиноз» объединяет различные по происхождению, механизму развития и биол. сущности процессы. Основное в развитии гиалиноз - деструкция волокнистых структур соединительной ткани и повышение тканево-сосудистой проницаемости в связи с ангионевротическими (дисциркуляторными), метаболическими, воспалительными и иммунопатологический процессами (смотри Плазморрагия). В результате нарушения проницаемости происходит пропитывание ткани плазменными белками и адсорбция их неизменённых волокнистых структур с последующей преципитацией. Образующийся гиалин имеет различный, в зависимости от характера заболевания, хим. состав (например., гиалин при диабетической микроангиопатии и гиалин при так называемый иммунокомплексных заболеваниях).
Гиалиноз относится к внеклеточным (мезенхимальным) диспротеинозам. Появление в цитоплазме гиалиновых капель (гиалиново-капельная дистрофия) или шаров (гиалиновые шары) не связано с Гиалиноз. Гиалин является фибриллярным белком (рисунок 1), в построении которого принимают участие плазменные белки, в частности фибрин. При иммуно-гистохимические исследовании в гиалине обнаруживают не только фибрин, но и компоненты иммунных комплексов (иммунные глобулины, фракции комплемента). Гиалиновые массы стойки к действию кислот, щелочей, ферментов, хорошо окрашиваются кислыми красками (эозин, кислый фуксин), пикрофуксином красятся в жёлтый или красный цвет; в массах гиалина могут откладываться липиды, соли кальция. Внешний вид органов и тканей при Гиалиноз зависит от стадии процесса; чаще Гиалиноз ничем не проявляется и обнаруживается лишь при микроскопическом исследовании. В тех случаях, когда процесс выражен резко, ткани становятся бледными, плотными, полупрозрачными. Гиалиноз, в частности артериол, может привести к деформации и сморщиванию органов (например, развитие артериолосклеротического нефроцирроза, клапанного порока сердца).
Гиалиноз наблюдается в соединительной ткани, строме органов и стенке сосудов (рисунок 2) в исходе плазматического пропитывания, фибриноидного набухания, склероза, хронический воспаления, некроза. В исходе плазматического пропитывания возникает Гиалиноз сосудов, чаще в артериальной системе. Наиболее распространён Гиалиноз мелких артерий и артериол (смотри Артериолосклероз). Гиалиноз артериол возникает в результате повреждения эндотелия, аргирофильных мембран и гладкомышечных волокон и пропитывания стенок сосуда белками плазмы крови, которые затем подвергаются ферментативным воздействиям, коагулируются и уплотняются, превращаясь в гиалиноподобное плотное вещество. Гиалиновые массы оттесняют кнаружи и разрушают эластическую пластинку, что ведёт к истончению средней оболочки; в результате артериолы превращаются в утолщённые плотные трубочки с резко суженным или полностью закрытым просветом. Гиалиноз мелких артерий и артериол, носящий системный характер, но наиболее выраженный в почках (рисунок 3 и 4), головном мозге, сетчатке глаза, поджелудочной железе, коже (рисунок 5), особенно характерен для гипертонической болезни (гипертонический артериологиалиноз). Нередко системный Гиалиноз артериол и мелких артерий наблюдается при хронический васкулярном гломерулонефрите и симптоматической артериальной гипертензии любого генеза. Распространённый Гиалиноз артерий эластического и эластическо-мышечного типов постоянно наблюдается при атеросклерозе, диабете и отражает процессы плазморрагии и инсудации, характерные для этих заболеваний. Местный Гиалиноз артерий как физиологическое явление встречается в селезёнке взрослых и пожилых людей, отражая функционально-морфологически особенности селезёнки как органа депонирования крови.
В исходе фибриноидного набухания, ведущего к деструкции коллагена и пропитыванию ткани плазменными белками и полисахаридами, соединительнотканные пучки разбухают, теряют фибриллярность и сливаются в однородную плотную хрящеподобную массу; клеточные элементы сдавливаются и подвергаются атрофии. Подобный механизм развития Гиалиноз собственно соединительной ткани и сосудистой стенки особенно часто наблюдается при заболеваниях с иммунными нарушениями. Так, системный Гиалиноз соединительной ткани и стенок сосудов выражен при коллагеновых болезнях: Гиалиноз клапанов сердца, стромы миокарда - при ревматизме, Гиалиноз синовиальных оболочек - при ревматоидном артрите, Гиалиноз кожи - при склеродермии, Гиалиноз стенок сосудов - при узелковом артериите и системной красной волчанке. Таков же механизм распространённого Гиалиноз почечных клубочков при иммунокомплексном гломерулонефрите. В этих случаях гиалин строится на иммунных комплексах, что подтверждает роль иммунологический механизмов в развитии Гиалиноз. Местный Гиалиноз может завершать фибриноидные изменения в дне хронический язвы желудка, в ткани червеобразного отростка при аппендиците, а также в очаге хронический воспаления.
Гиалиноз в исходе склероза имеет в основном местный характер. Таков Гиалиноз в рубцах (рисунок 6), фиброзных спайках серозных полостей, Гиалиноз сосудистой стенки при атеросклерозе, инволюционном склерозе артерий, при организации тромба, Гиалиноз капсулы, окружающей какой-либо патологический очаг, стромы опухоли. В основе Гиалиноз в этих случаях лежат местные метаболические нарушения соединительной ткани; подобный механизм имеет Гиалиноз некротизированных тканей, фибринозных наложений и других органических субстанций.
В большинстве случаев процесс необратим, но возможно и рассасывание гиалиновых масс. Так, гиалин в рубцах, так называемый келоидах (смотри), может подвергаться разрыхлению и рассасыванию. Обратим Гиалиноз молочной железы, причём рассасывание гиалиновых масс происходит в условиях гиперфункции железы. В ряде случаев гиалинизированная ткань ослизняется.
Функциональное значение Гиалиноз различно в зависимости от локализации, степени и распространённости процесса. Например, Гиалиноз в небольших кожных рубцах обычно не вызывает особых расстройств. Распространённый же Гиалиноз ведёт к значительным функциональным нарушениям, как это наблюдается, например, при ревматизме, склеродермии, гипертонической болезни, диабете.
Гиалиноз – необратимая дистрофия, при которой в гистионе образуются гомогенные плотные массы, которые напоминают гиалиновый хрящ.
ГИАЛИН – сложный фибриллярный белок, в состав которого входят:
белки плазмы крови
фибрин
липиды
компоненты иммунных комплексов
Гиалин окрашивается еозином и фуксином в красный цвет.
Причины:
Фибриноидное набухание
Воспаление
Ангионевротические реакции
Патогенез :
Ведущую роль сыграет повышенная сосудистая проницаемость. Накапливаются белки, ГАГ. Возникает денатурация, преципитация белка.
Гиалиноз – двух видов :
Гиалиноз сосудов
Гиалиноз соединительной ткани
По распространённости процесса :
ГИАЛИНОЗ СОСУДОВ
Поражения преимущественно мелких артерий, артериол.
В сосудах возникают явления ПЛАЗМОрРАГИИ.
Накапливается гиалин ПОД ЭНДОТЕЛИЕМ, со временем занимает всю стенку сосуда.
Гиалиноз сосудов 3 видов , в зависимости от химического состава гиалина:
простой гиалин – возникает при действии ангионевротических факторов (спазм или расширение сосудов) плазморрагия гиалиноз. (гипертоническая болезнь, атеросклероз, гемолитичесая анемия, болезнь Верльгофа)
липогиалин – ГИАЛИН + ЛИПИДЫ, -ЛИПОПРОТЕИДЫ (сахарный диабет)
сложный Г. – ГТАЛИН + ИММУННЫЕ КОМПЛЕКСЫ (ревматические болезни)
ГИАЛИНОЗ СОЕДИНИТЕЛЬНОЙ ТКАНИ
Возникает вследствие фибриноидного набухания. При этом на деструктивно измененную соединительную ткань наслаиваются белки плазмы крови и полисахариды, а в дальнейшем денатурация и преципитация белка (хроническая язва, спаечная болезнь, опухоли, ожоговая болезнь).
Макр.: Деформация органа. Если орган имеет капсулу – то она утолщается (“глазурная” капсула)
Значение:
Необратимый процесс, но некоторые гиалиновые массы могут самостоятельно рассасываться.
Приводит к резкому нарушению функции органа (створки клапанов сердца недостаток сердца; почка почечная недостаточность)
Амилоидоз
Амилоидоз – это мезенхимальный диспротеиноз, характеризующийся появлением аномального фибриллярного белка с последующим образованием сложного белково-полисахаридного комплекса – АМИЛОИДА.
Рокитанский, 1844г.
АМИЛОИД – гликопротеид, основным компонентом которого является фибриллярный белок – F-компонент .
F-компонент: различают 4 вида:
АА-билок – не ассоциированный с IG
AL-белок – ассоциированный с IG
AF-белок – синтезируется из преальбумина
ASC 1- белок – синтезируется из предшественника – преальбумина
Вторым компонентом является Р–компонент (плазменный компонент). Это полисахариды крови.
АМИЛОИД = F-компонент + Р–компонент + ГАГ + ФИБРИН + ИММУННЫЕ КОМПЛЕКСЫ
Амилоид – довольно стойкое вещество. Иммунные клетки не распознают амилоид.
Патогенез:
4 теории возникновения амилоида.
Теория диспротеиноза (при глубоком нарушении белкового обмена)
Иммунологическая теория
Теория клеточной локальной секреции
Мутагенная теория – согласно теории возникает мутация клетки и эта клетка начинает синтезировать аномальный белок. Иммунная система не распознает эти клетки.
Согласно этой теории амилоид развивается в 4 стадии:
Доамилоидная – возникает клеточная трансформация клетка превращается в АМИЛОИДОБЛАСТ. Как правило, это клетки РЭС – макрофаги, плазмобласты.
Синтез амилоидобластами аномального белка – F-компонента
Образование АМИЛОИДНОЙ СУБСТАНЦИИ. F-компонент образовывает каркас амилоида.
Синтез амилоида.
Классификация Амилоидоза .
Первичный (идиопатический) – носит генерализованный характер; синтез AL-белка (преимущественно поражаются: сердечно-сосудистая система, скелетные мышцы, кожа, нервы).
Наследственный – наиболее частое в тех этнических группах, где имеют место родственные браки; AF-белок (нервные волокна, почки).
Возрастной (старческий) – ASC 1- белок (сердце, артерии, головной мозг, поджелудочная железа).
Вторичный – возникает вследствие синтеза АА-белка (болезни, которые носят гнойно-деструктивный характер: tbc, бронхоэктатическая болезнь, остеомиелит, парапротеинемические лейкозы, опухоли, ревматоидный артрит).
Макр.: на ранних этапах орган без перемен (со временем орган увеличивается в размерах, плотный, легко ломается, молниевый вид (“сальный”)
Микр.: МЕТАХРОМАЗИЯ
Подробности
Мезенхимальные дистрофии развиваются в результате нарушений обмена в соединительной ткани и выявляются в строе органов и стенках сосудов. При нарушениях обмена в соединительной ткани, преимущественно, в ее межклеточном веществе, накапливаются продукты метаболизма, которые могут приноситься с кровью и лимфой, быть результатом извращенного синтеза или появляться в результате дезорганизации основного вещества и волокон соединительной ткани.
1. Стромально-сосудистые диспротеинозы
С дистрофиям такого типа относят мукоидное набухание, фибриноидное набухание, гиалиноз, амилоидоз.
Нередко мукоидное набухание, фибриноидное набухание и гиалиноз являются последовательными стадиями дезорганизации соединительной ткани. В основе этого процесса лежат накопление продуктов плазмы крови в основном веществе в результате повышения тканево-сосудистой проницаемости (плазморрагия ), деструкция элементов соединительной ткани и образование белково-полисахаридных комплексов. Амилоидоз отличается тем, что в состав образующихся комплексом входит аномальный белок, который синтезируют амилоидобласты.
1) Мукоидное набухание
Поверхностная и обратимая дезорганизация соединительной ткани. При этом в основном веществе происходят накопление и перераспределение гликозаминогликанов за счет увеличения содержания прежде всего глюкуроновой кислоты. Так как гликозаминогликаны обладают повышенными гидрофильными свойствами, их накопление обуславливает повышение тканевой и сосудистой проницаемости. В результате к ГАГ примешиваются белки плазмы (в основном, глобулины) и гликопротеиды. Развиваются гидратация и набухание основного межуточного вещества.
Микроскопия : основное вещество базофильное. Возникает феномен метахромазии – изменение состояния основного межуточного вещества из-за изменения рН с накоплением хромотропных веществ. Коллагеновые волокна набухают, обычно сохраняют пучковое строение. Становятся малоустойчивыми к действию коллагеназы.
Изменения могут сопровождаться появлением лимфоцитарных, плазмоклеточных и гистиоцитарных инфильтратов.
Такой тип набухания встречается в различных органах и тканях, но чаще в стенках артерий, клапанах сердца, эндокарде, эпикарде, то есть там, где хромотропные вещества встречаются и в норме (однако при патологии их количество резко возрастает).
Внешний вид: ткань или орган сохранены.
Причины : гипоксия, инфекционные и аллергические заболевания, ревматические болезни, атеросклероз, эндокринопатия и т.д.
Исход : двоякий. Либо полное восстановление ткани, либо переход в фибриноидное набухание.
2) Фибриноидное набухание.
Глубока и необратимая дезорганизация соединительной ткани, в основе которой лежит деструкция ее основного вещества и волокон, сопровождающаяся резким повышением сосудистой проницаемости и образование фибриноида. Фибриноид – сложное вещество, в состав входят белки и полисахариды распадающихся коллагеновых волокон, основного вещества и плазмы крови, а также клеточные нуклеопротеиды. Обязательным компонентом является фибрин.
Микроскопия : пучки коллагеновых волокон, пропитанные плазмой, становятся гомогенными, образуя с фибрином нерастворимые прочные эозинофильные соединения. Метахромазия тканей не выражена или выражена слабо (так как ГАГ основного вещества деполимеризованы).
Внешний вид : внешне органы и ткани мало изменяются.
Причины : чаще всего это проявление инфекционно-аллергических, аутоиммунных и ангионевротических реакций. В таких случаях набухание носит системный характер. Местно фибриноидное набухание может возникать при воспалении, особенно, хроническом.
Исход: характеризируется развитием фибриноидного некроза, замещением очага деструкции соединительной тканью (склероз) или гиалинозом.
Такое набухание ведет к нарушению, иногда к прекращению функции органа.
3) Гиалиноз
В соединительной ткани образуются однородные полупрозрачные плотные массы, напоминающие гиалиновый хрящ. Ткань при этом уплотняется.
В развитии гиалиноза ведущую роль играют деструкция волокнистых структур и повышение тканево-сосудистой проницаемости. С плазморрагией связаны пропитывание ткани белками плазмы и адсорбция их на измененных волокнистых структурах с последующей преципитацией и образованием гиалина. В образовании сосудистого гиалина принимают участие гладкомышечные клетки. Гиалиноз может развиваться в исходе различных процессов: плазматического пропитывания, фибриноидного набухания, воспаления.
Различают:
А) гиалиноз сосудов
Гиалинозу подвергаются преимущественно мелкие артерии и артериолы. Ему предшествуют повреждения эндотелия, его мембраны и гладкомышечных клеток стенки и пропитывание ее плазмой крови.
Микроскопия : гиалин обнаруживается в субэндотелиальном пространстве6 он оттесняет кнаружи и разрушает эластическую пластинку, средняя оболочка истончается, в фиале артериолы превращаются в утолщенные стеклянные трубки с резко суженным или полностью закрытым просветом.
Такой гиалиноз носит системный характер, однако6 наиболее выражен в почках, головном мозге, сетчатке глаза, поджелудочной железе., коже. Характерен для гипертонической болезни, диабетической микроангиопатии и заболеваний с нарушениями иммунитета. Как физиологическое явление местный гиалиноз артерий наблюдается в селезенке взрослых и пожилых людей (отражает функционально-морфологические особенности этого органа – депонирование крови).
Сосудистый гиалин – вещество преимущественно гематогенной природы. Руководствуясь особенностями патогенеза гиалиноза сосудов, выделяют:
- простой сосудистый гиалин
Возникает вследствие инсудации неизмененных или малоизмененных компонентов плазмы крови, Такой тип гиалина чаще встречается у пациентов с доброкачественной гипертензией, атеросклерозе, а также у здоровых людей.
- липогиалин
Содержит липиды и бета-липопротеиды. Такой тип гиалина часто обнаруживается при сахарном диабете.
- сложный гиалин
Строится из иммунных комплексов, фибрина и разрушающихся структур сосудистой стенки. Такой гиалин характерен для пациентов с иммунопатологиями, например, с ревматическими заболеваниями.
Б) гиалиноз собственно соединительной ткани
Развивается, как правило, в исходе фибриноидного набухания, ведущего к деструкции коллагена и пропитыванию ткани белками плазмы и полисахаридами.
Имеет большое клиническое значение гиалиноз миометрия. После выполнения Кесарево сечения на матке остается рубец, на границе с мышцей в клетках откладывается гиалин. Если женщина будет рожать второго ребенка естественным путем, то произойдет разрыв.
Микроскопия : соединительнотканные пучки теряют фибриллярность, а клеточные элементы превращаются в хрящеподобную массу.
Гиалиноз может завершать фибриноидные изменения в очаге хронического воспаления. Гиалиноз как исход склероза имеет, в основном, местный характер: он развивается в рубцах, фиброзных спайках серозных полостей, сосудистой стенке при атеросклерозе.
Внешний вид : при выраженном гиалинозе внешний вид органов изменяется. Гиалиноз артериол и мелких артерий ведет к атрофии, деформации и сморщиванию органа. При гиалинозе собственно соединительной ткани она становится плотной, белесоватой, полупрозрачной.
Исход : в большинстве случаев неблагоприятный, однако, возможно и рассасывание гиалиновых масс.
4) Амилоидоз
Сопровождается глубоким нарушением белкового обмена, появлением аномального фибриллярного белка и образованием в межуточной ткани и стенках сосудов амилоида.
Амилоид представляет собой гликопротеид, основным компонентном которого являются фибриллярные белки (F-компонент, синтезируется амилоидобластами). Они образуют фибриллы. Фибриллярные белки амилоида неоднородны:
а) AA белок: неассоциированный с иммуноглобулинами, образующийся из своего сывороточного аналога – белка SAA
б) AL белок: ассоциированный с иммуноглобулинами, его предшественником являются легкие цепи иммуноглобулинов
в) AF белок: в его образовании участвует преальбумин
г) ASC 1 белок – белок, предшественником которого также является преальбумин
Эти фибриллярные белки входят в сложные соединения с глюкопротеидами плазмы крови. Этот плазменный компонент (Р-компонент) амилоида представлен палочковидными структурами.
И F, и P-компоненты обладают антигенными свойствами. Фибриллы амилоида и плазменный компонент вступают в соединения в хондроитин-сульфатами ткани, а к образующемуся комплексу присоединяются «гематогенные добавки», среди которых основное значение имеют фибрин и иммунные комплексы. Все связи в амилоиде очень прочные, поэтому на него не действуют ферменты организма.
Классификация амилоидоза основывается на возможных причинах, специфике фибриллярных белков, распространенности, клинических проявлениях.
А. По причинам возникновения:
Первичный (идиопатический) амилоидоз
Для него характерно: отсутствие предшествующего или сопутствующего «причинного» заболевания; поражение преимущественно мезодермальных тканей – ССС, скелетных и гладких мышц, нервов и кожи; склонность к образованию узловатых отложений, непостоянство красочных реакций амилоидного вещества
Наследственный (генетический, семейный) амилоидоз
Наследственный амилоидоз с преимущественным поражением почек характерен для периодической болезни (семейная средиземноморская лихорадка), которая чаще наблюдается у представителей древних народов (евреи, армяне, арабы).
Вторичный (приобретенный) амилоидоз
В отличие от других форм развивается как осложнение, а не как самостоятельная болезни. К такому амилоидозу приводят хронические неспецифические воспалительные заболевания легких, туберкулез, остеомиелит, злокачественные новообразования, ревматические болезни.
Такой амилоидоз, как правило, генерализован и встречается наиболее часто.
Старческий амилоидоз
Типичны поражения сердца, артерий, головного мозга, островков Лангерганса. Эти изменения обуславливают физическую и психическую старческую деградацию. При старческом амилоидозе наиболее часты локальные формы, хотя встречается и генерализованный старческий амилоидоз.
Б. По специфике фибриллярных белков:
AL-амилоидоз
Включает первичный (идиопатический) амилоидоз и амилоидоз при «плазмоклеточной дискразии», которая объединяет парапротеинемические лейкозы, злокачественные лимфомы и др.
Всегда генерализованный с поражением сердца, легких и сосудов.
AA-амилоидоз
Охватывает вторичный амилоидоз и болезни Маккла и Уэльса. Также генерализован, но преимущественно поражает почки.
AF-амилоидоз
Наследственный, представлен семейной амилоидной нефропатией. Поражаются, главным образом, периферические нервы.
ASC 1 -амилоидоз
Старческий генерализованный или системный с преимущественным поражением сердца и сосудов.
В. По распространенности
- генерализованная форма
Первичный амилоидоз, амилоидоз при “плазмоклеточной дискразии” (AL), вторичный амилоидоз и некоторые типы наследственного (AA), старческий системный амилоидз (ASC 1).
Локальный амилоидоз
Объединяет ряд форм наследственного и старческого амилоидоза, а также локальный опухолевидный амилоидоз.
Г. По клиническим проявлениям
- кардиопатический
Чаще встречается при первичном и старческом системном амилоидозе.
- нефропатический
При вторичном амилоидозе, периодической болезни и болезни Маккла и Уэллса.
- нейропатический
Как правило, имеет наследственный характер.
Гепатопатический
Эпинефропатический
- смешанный
Вторичный амилоидоз.
APUD-амилоидоз
Развивается в органах APUD системы при развитии в них опухолей (апудом), а также в островках поджелудочной железы при старческом амилоидозе.
Морфо- и патогенез амилоидоза
Иногда функцию амилоидобластов выполняют макрофаги, плазматические клетки, фибробласты и т.д. При локальных формах в роли амилоидобластов могут выступать кардиомиоциты, гладкомышечные клетки, кератиноциты.
При вторичном амилоидозе (исключая амилоидоз при «плазмоклеточной дискразии») мутации и появление амилоидобластов можно связать длительной антигенной стимуляции.
Клеточные мутации при «плазмоклеточной дискразии» и при амилоидозе опухолей обусловлено опухолевыми мутагенами.
При генетическом амилоидозе речь идет о мутации гена, которая может произойти в различных локусах, чем и различаются составы амилоидных белков. Вероятно, имеют место подобные механизмы и при старческом амилоидозе.
Поскольку антигены белка амилоидных фибрилл являются чрезвычайно слабыми иммуногенами, мутирующие клетки не распознаются и не элиминируются. Развивается иммунологическая толерантность к белкам амилоида, что приводит к прогрессированию амилоидоза.
Образование амилоидного белка может быть связано с:
Ретикулярными волокнами (периретикулярный амилоидоз)
Амилоид выпадает по ходу мембран сосудов и желез, а также ретикулярной стромы паренхиматозных органов. Характерно преимущественное поражение селезенки, печени, почек, надпочечников, кишечника, интимы сосудов мелкого и среднего калибра (паренхиматозный амилоидоз).
Коллагеновыми волокнами (периколлагеновый)
Амилоид выпадает по ходу коллагеновых волокон, свойственно преимущественное поражение адвентиции сосудов среднего и крупного калибра, миокарда, поперечно-полосатой и гладкой мускулатуры, нервов, кожи (мезенхимальный амилоидоз).
Патогенез амилоидоза сложен и неоднозначен. Лучше всего изучен патогенез AA – и AL-амилоидоза.
При АА-амилоидозе фибриллы амилоида образуются из поступающего в макрофаг предшественника фибриллярного белка амилоида – белка SAA, который синтезируется в печени. Синтез SAA стимулирует макрофагальный медиатор интерлейкин-1, что приводит к резкому увеличению SAA в крови. В этих условиях макрофаги не осуществляют полную деградацию SAA, и из его фрагментов и инвагинатах плазматической мембраны амилоидобласта происходит сборка фибрилл амилоида. Эту сборку стимулирует амилоидстимулярующий фактор – АСФ, который обнаруживается в тканях в предамилоидной стадии.

Итак, ведущую роль в патогенезе АА-амилоидоза играет магрофагальная система: она стимулирует усиленный синтез SAA,она же участвует в образовании фибрилл амилоида из деградирующих фрагментов белка.
При AL-амилоидозе сывороточным предшественником белка амилоидных фибрилл являются L-цепи иммуноглобулинов. Возможны два механизма образования AL-фибрилл: 1) нарушение деградации легких цепей с образованием фрагментов, способных к агрегации а фибриллы; 2) появление легких цепей с особыми вторичными и третичными структурами при аминокислотных заменах.
Синтез амилоидных фибрилл может происходить не только в макрофагах, но и в плазматических и миеломных клетках, синтезирующих парапротеины.
Соответственно, с извращенной функцией лимфоидной системы связано появление амилоидогенных легких цепей иммуноглобулинов – предшественника амилоидных фибрилл.

Макро- и микроскопия
Внешний вид органов зависит от степени процесса, Если отложения небольшие, внешний вид органа мало изменен. При выраженном амилоидозе орган увеличивается, становится очень плотным и ломким, а на разрезе имеет восковидный, сальный вид.
В селезенке амилоид откладывается в лимфатических фолликулах (саговая селезенка - плотная, увеличена, на разрезе полупрозрачные зерна) или равномерно по всей пульпе (сальная селезенка - увеличена, плотная, коричнево-красная, гладкая, имеет сальный блеск на разрезе).
В почках амилоид откладывается в стенке сосудов, в капиллярных петлях и мезангии клубочков, в базальных мембранах канальцев и в стреме. Почки становятся плотными, большими, сальными. По мере нарастания процесса клубочки и пирамиды полностью замещаются амилоидом, разрастается соединительная ткань и развивается амилоидное сморщивание.
В печени отложение амилоида наблюдается по ходу ретикулярной стромы долек. В стенках сосудов, протоков, соединительной ткани портальных трактов. Гепатоциты сморщиваются и погибают. Печень увеличена, плотная, выглядит сальной.
В кишечнике амилоид выпадает по ходу ретикулярной стромы слизистой, а также в стенках сосудов как слизистой оболочки, так и подслизистого слоя. При резко выраженном амилоидозе железистый аппарат кишечника атрофируется.
В сердце амилоид обнаруживается под эндокардом, в строме и сосудах миокарда, а также в эпикарде по ходу вен. Отложение ведет к амилоидной кардиомегалии. Сердце становится плотным, сальным.
Исход амилоидоза неблагоприятный.
2. Стромально-сосудистые липидозы
Возникают при нарушениях обмена нейтральных жиров или холестерина и его эфиров.
Нейтральные жиры – лабильные жиры, обеспечивающие энергетические запас организма.
Ожирение – увеличение количества нейтральных жиров в жировых депо, имеющее общий характер. Оно выражается в обильном отложении жиров в подкожной клетчатке, сальнике, брыжейке. средостении, эпикарде. Жировая ткань появляется также там, где она в норме отсутствует, например, в строме миокарда, поджелудочной железе.
Классификация основывается на различных принципах:
А. По этиологическому признаку:
Первичная форма
Его причина неизвестна, поэтому его называют идиопатическим.
Вторичная форма
Представлено следующими видами:
Алиментарное, причина которого – гиподинамия и несбалансированное питание
Церебральное, развивающееся при травме, опухолях, ряде нейротропных инфекций
Эндокринное-синдромы Иценко-Кушинга, Фрелиха
Наследственное – синдром Лоренса-Муна-Бидля, болезнь Гирке
Б. По внешним проявлениям:
Симметричный тип
Жиры откладываются равномерно в разных частях тела.
Накопление в подкожной клетчатке лица, затылка, шеи, верхнего плечевого пояса, молочных желез.
Жир откладывается в подкожной клетчатке живота в виде фартука
В области бедер и голеней
В. По превышению массы тела:
I степень – 20-29% избыточной массы тела
II степень – 30-49%
III степень - 50-99%
IV степень – 100% и более
Г. По характеристике морфологических изменений
Учитывают число адипоцитов и их размер.
Гипертрофический тип
Жировые клетки увеличены и содержат в несколько раз больше триглицеридов, чем обычные. Число адипоцитов не меняется. Адипоциты малочувствительны к инсулину, но высокочувствительны к липолитическим гормонам.
Гиперпластический тип
Число адипоцитов увеличивается. Функция адипоцитов не нарушена, метаболические изменения отсутствуют, течение болезни доброкачественное.
Причины и механизмы развития
Большое значение имеют несбалансированное питание, гиподинамия, нарушение ЦНС, эндокринной регуляции, наследственные факторы.
Непосредственный механизм ожирения лежит в нарушении равновесия липогенеза и липолиза в жировой клетке в пользу липогенеза.
Исход : редко бывает благоприятным.

Нарушения обмена холестерина и его эфиров.
Такие нарушения лежат в основе атеросклероза. При этом в интиме артерий накапливаются и холестерин и его эфиры, но и бета-липопротеиды низкой плотности, и белки плазмы крови, чему способствует повышение сосудистой проницаемости.
Накопление ведет к деструкции интимы.
В результате в интиме образуется жиробелковый детрит, разрастается соединительная ткань, формируется фиброзная бляшка, сужающая просвет сосуда.
3. Стромально-сосудистые углеводные дистрофии
Могут быть связаны с нарушением баланса гликопротеидов и гликозаминогликанов.
Ослизнение тканей – дистрофия, связанная с нарушением обмена гликопротеидов. Хромотропные вещества высвобождаются из связей с белками и накапливаются в межуточном веществе. В отличие от мукоидного набухания при этом происходит замещение коллагеновых волокон слизеподобной массой. Соединительная ткань, строма органов, жировая ткань, хрящ становятся полупрозрачными, слизеподобными, а клетки их – звездчатыми.
Причина : чаще всего вследствие дисфункции эндокринных желе, истощения (например, микседема, слизистый отек, ослизнение соединительных тканей при кахексии).
Исход : процесс может быть обратимым, однако его прогрессирование приводит к колликвации и некрозу.
Гиалиноз артериол - характернейшее явление в патологической картине гипертонической болезни.
Гиалиновые массы откладываются во внутренней оболочке артериол под эндотелиальным покровом между внутренним и наружным листками эластической пластинки; средняя мышечная оболочка сосудов оттесняется гиалиновыми массами кнаружи. Отложение гиалиновых масс приводит к сильному утолщению стенок сосуда, сужению сосудистого просвета, а иногда и к полному его закрытию. Возможно, что гиалин образуется в стенках сосуда в результате коагуляции жидкой белковой массы, поступающей во внутренние слои сосуда из кровеносного русла. С этой точки зрения гиалиноз можно рассматривать как исход белкового пропитывания. Гиалиновые массы более гомогенны и плотны. Реактивных явлений вокруг скопившихся в стенках сосудов гиалиновых масс обычно не наблюдается.
Гиалиноз артериол встречается не только у больных гипертонией. В большом числе случаев и в слабой форме он может быть найден у людей пожилого возраста, не страдавших гипертонической болезнью. Гиалиноз артериол поражает различные сосудистые области далеко не одинаково. В наибольшей мере он бывает выражен в артериях селезенки, притом не только у больных гипертонией, но и у пожилых людей с нормальным давлением. Очень часто и в выраженной степени он встречается при гипертонической болезни в сосудах почек, надпочечников, поджелудочной железы. Если гиалиноз артериол почек при гипертонической болезни встречается в 97% случаев, то среди нормотоников он наблюдается только у 2%. Следовательно, гиалиноз почечных артериол является феноменом, достаточно характерным для гипертонии.
Белковые массы, поступающие в толщу сосудистых стенок при гипертонии, могут в дальнейшем подвергаться рассасыванию. Таким образом, белковое пропитывание на первых порах, если оно не достигло большой степени, есть процесс обратимый. Это чрезвычайно важное для обстоятельство должно послужить дополнительным стимулом к энергичному лечению гипертоников.
Но чаще всего белковое пропитывание и гиалиноз артериол при гипертонии сопровождаются деструктивными и склеротическими изменениями. Артериолосклероз есть обычный исход более поздних стадий повышенного давления. Он приводит к последующим расстройствам кровоснабжения и питания тканей и органов, еще более сильно суживая кровеносное русло в дополнение к тому сужению, которое создается в результате гипертонического изменения тонуса сосудов.
Белковое пропитывание и гиалиноз артериол часто можно наблюдать при гипертонии одновременно, причем в разных органах эти изменения могут находиться в различных фазах своего развития, то более свежих, то более поздних. Это говорит, что плазматическое пропитывание, гиалиноз и артериолосклероз - формы одного процесса, протекающие в виде повторных вспышек, «причем каждый раз в процесс вовлекаются все новые участки артериальной сети». В одних органах наблюдается главным образом гиалиноз, в других - плазматическое пропитывание, в третьих - их сочетание.
Статью подготовил и отредактировал: врач-хирургВидео:
Полезно:
Статьи по теме:
- Большая частота изменений почек при гипертонической болезни, особенно в ее поздней стадии, делает понятным то...
- В какой мере в реакции повышения давления со стороны надпочечников принимает участие их корковый слой,...
- Гипертония сопровождается некоторыми нарушениями углеводного обмена. Одним из элементарных показателей этих нарушений может служить наклонность...