Блокаторы na каналов. Блокаторы молекулярных рецепторов и ионных каналов
Читайте также
Карбамазепин (Тегретол, Финлепсин) является производным иминос- тильбена, наряду с выраженным противоэпилептическим эффектом оказывает нормотимическое (улучшение настроения) и антидепрессивное действие. Кроме того, карбамазепин обладает выраженной анальгетической активностью.
Противосудорожное действие препарата связано с блокадой натриевых каналов мембран нервных клеток. Уменьшает способность нейронов поддерживать высокочастотную импульсацию, типичную для эпилептогенной активности.
В дополнение к этому препарат может действовать пресинаптически, нарушая высвобождение медиатора за счет блокады пресинаптических натриевых каналов.
Является препаратом выбора для предупреждения парциальных судорог и больших судорожных припадков. Используется для ослабления нейропатической боли, в частности, при невралгии тройничного нерва (является препаратом выбора). Применяют также для профилактики маниакально-депрессивных состояний.
Карбамазепин при приеме внутрь почти полностью всасывается из ЖКТ в кровь, скорость всасывания индивидуальна и подвержена колебаниям. Максимальная концентрация в плазме после приема внутрь достигается в течение 4- 5 ч. В грудном молоке концентрация вещества достигает 60% от концентрации в плазме крови матери. Метаболизируется в печени, повышает скорость собственного метаболизма за счет индукции микросомальных ферментов печени. Один из метаболитов - карбамазепин-10,11-эпоксид - обладает противосудорожной, ан- тидепрессивной и антиневралгической активностью. Выводится в основном почками (более 70%).
Карбамазепин вызывает многочисленные побочные эффекты, среди которых потеря аппетита, тошнота, головная боль, сонливость, атаксия; нарушение аккомодации; диплопия (двоение в глазах), нарушения сердечного ритма, гипонатри- емия, гипокальциемия, гепатит, аллергические реакции, лейкопения, тромбоци- топения, агранулоцитоз (требуется контроль картины крови). Существует риск развития тератогенного действия. Применение препарата при беременности возможно только по жизненным показаниям. Так как карбамазепин угнетает психомоторные реакции, его не следует назначать лицам, деятельность которых требует повышенного внимания (например, водителям автотранспорта). Карбамазепин повышает скорость метаболизма, вследствие чего снижает в крови концентрацию некоторых лекарственных веществ, в том числе противоэпилептических препаратов (клоназепама, ламотриджина, натрия вальпроата, этосуксимида и др.).

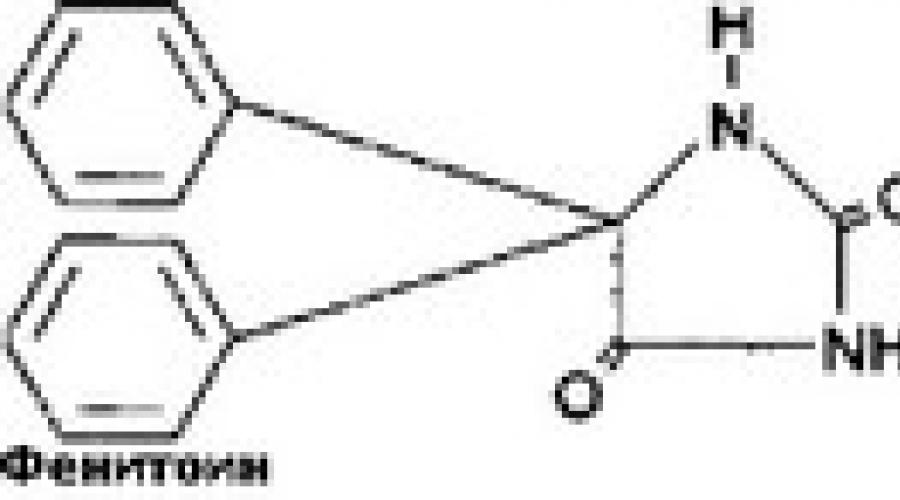
Фенитоин (Дифенин) является производным гидантоина, оказывает противосудорожное действие без выраженного снотворного эффекта. Кроме того, препарат обладает антиаритмической активностью, в особенности при аритмиях, вызванных передозировкой сердечных гликозидов (см. гл. 19 «Антиаритми- ческие средства»), оказывает анальгетическое действие, в особенности при невралгии тройничного нерва.
Механизм противосудорожного действия фенитоина связывают с блокадой натриевых каналов, уменьшением вхождения в нейроны ионов натрия, что препятствует генерации и распространению высокочастотных разрядов, снижает возбудимость нейронов и препятствует их активации при поступлении к ним импульсов из эпилептогенного очага.
Используется для лечения различных форм эпилепсии, за исключением малых судорожных припадков, в частности для предупреждения парциальных судорог и больших судорожных припадков. Для предупреждения судорожных припадков фенитоин назначают внутрь в виде таблеток. Фенитоин-натрий применяют для купирования эпилептического статуса, вводят внутривенно. При приеме внутрь скорость всасывания препарата из ЖКТ в значительной степени зависит от лекарственной формы, состава таблеток (размера частиц, вспомогательных веществ), при этом время достижения максимальной концентрации вещества в крови может варьировать в пределах от 3 до 12 ч. Фенитоин интенсивно связывается с белками плазмы крови (на 90%). Метаболизируется в печени, основной неактивный метаболит - 5-(п-гидроксифенил)-5-фенилгидантоин - подвергается конъюгации с глюкуроновой кислотой. В основном выводится из организма почками в виде метаболитов. Период полуэлиминации варьирует от 12 до 36 ч в зависимости от концентрации фенитоина в плазме крови (большие значения tVj наблюдаются при высоких концентрациях вещества в крови, что связано с насыщением ферментов печени, метаболизирующих фенитоин).
Фенитоин вызывает многочисленные побочные эффекты: головокружение, возбуждение, тошноту, рвоту, тремор, нистагм, атаксию, диплопию, гирсутизм; гиперплазию десен (особенно у молодых людей), снижение уровня фолатов и мегалобластную анемию, остеомаляцию (связано с нарушением метаболизма витамина D), аллергические реакции и др. Отмечено тератогенное действие. Вызывает индукцию микросомальных ферментов в печени и таким образом ускоряет метаболизм ряда лекарственных веществ (кортикостероиды, эстрогены, теофил- лин), повышает их концентрацию в крови.
Ламотриджин (Ламиктал) блокирует натриевые каналы мембран нейронов, а также уменьшает выделение глутамата из пресинаптических окончаний (что связывают с блокадой натриевых каналов пресинаптических мембран). Ламотриджин применяют практически при всех формах эпилепсии: для предупреждения парциальных судорог, больших судорожных припадков, малых приступов эпилепсии. Назначают для лечения эпилепсии, устойчивой к другим противо- эпилептическим средствам, или как дополнение к терапии другими препаратами. Побочные эффекты: сонливость, диплопия, головная боль, атаксия, тремор, тошнота, кожные высыпания.
Точные механизмы и места действия многих антиаритмических препаратов (ААП) окончательно еще не выяснены. Большинство из них работают сходным образом. ААП связываются с каналами, контролирующими ионные потоки через мембраны сердечных клеток. В результате изменяются скорость и продолжительность фаз потенциала действия, соответственно этому изменяются основные электрофизиологические свойства сердечной ткани: скорость проведения, рефрактерность и автоматизм. Большинство антиаритмических лекарственных средств имеют более чем одну точку приложения своего действия, и их эффекты обусловлены сложной цепью взаимоотношений с мембраной клетки, ее ионными каналами, насосами и рецепторами.
Применение ААП осложняется тем, что не все механизмы развития аритмий у человека известны. В ряде случаев о патогенезе можно только догадываться, в связи с чем препараты подбираются эмпирически. Наряду с терапевтическим действием - предотвращением или купированием аритмии, ААП способны вызывать нежелательные эффекты, в том числе аритмогенные. Многие побочные эффекты ААП дозозависимы и связаны с их электрофизиологическими действиями.
Дается характеристика действия ААП I и Ш классов аденозина, сульфата магния, препаратов калия. Характеристику антиаритмического эффекта ААП II класса (β-блокаторы) и IV класса (антагонисты кальция), а также дигоксина см. в соответствующих главах.
Ключевые слова: ионные каналы, потенциал действия, нарушения проводимости, повышение автоматизма, триггерная активность (псевдоавтоматизм), повторный вход возбуждения, классификация Вогана Вильямса, прямая и обратная частотная зависимость, гемодинамические эффекты, фармакокинетические характеристики, аденозин, магния сульфат, препараты калия.
ЭЛЕКТРОФИЗИОЛОГИЧЕСКИЕ МЕХАНИЗМЫ АРИТМИЙ
Работа сердца обеспечивается высококоординированной электрофизиологической активностью множества ионных каналов, представляющих собой белковые комплексы в мембранах кардиомиоцитов. Каналы регулируют вход и выход в клетки ионов натрия, калия и кальция. Изменение концентраций ионов по обе стороны клеточной мембраны формирует концентрационный градиент и связанный с ним трансмембранный электрический потенциал клеток сердца.
Повторяющиеся фазовые изменения трансмембранного электрического потенциала клеток, заключающиеся в деполяризации и поэтапной реполяризации мембран кардиомиоцитов, создают условия для распространения регулярно возникающего электрического импульса по миофибриллам и для их сокращения.
Участие различных ионных каналов в формировании потенциала действия определяет несходство в скорости передачи и распространения возбуждения в разных клетках миокарда.
В кардиомиоцитах и клетках системы Гиса-Пуркинье деполяризация клеточной мембраны регулируется открытием «быстрых» натриевых каналов. В результате внутрь клетки почти мгновенно поступает такое количество ионов натрия, что внутренняя поверхность мембраны не только утрачивает отрицательный заряд, но и приобретает положительный.
Дальнейшее восстановление исходного потенциала определяется главным образом входящим током ионов кальция и выходящим током ионов калия. Постепенно калиевый ток усиливается, а кальциевый ослабевает, и электрический заряд мембраны возвращается к исходному уровню. Продолжительность периода восстановления потенциала покоя (фаза реполяризации) обуславливает продолжительность периода, в течение которого клетка не способна реагировать на новый стимул (рефрактерный период).
В синусовом узле и а-в узле, характеризующихся исходно более низким потенциалом покоя и не имеющих «быстрых» натриевых каналов, деполяризация обусловлена поступлением в клетку ионов кальция, что сопровождается не столь стремительной деполяризацией. Поскольку скорость распространения импульсов проводящей системе сердца и миокарду определяется быстротой деполяризации клеточной мембраны, то по а-в узлу импульсы проводятся значительно медленнее, чем по предсердиям и желудочкам. Период восстановления в структурах с «медленным» ответом четко не дифференцируется, а их суммарная продолжительность не соответствует величине рефрактерного периода.
С каждым потенциалом действия в кардиомиоцит входят ионы натрия и выходят ионы калия - ионные градиенты при этом уменьшаются. Для поддержания ионных градиентов в клетках работает Na+К+-АТФ-аза. Она переносит ионы через мембрану. Поддержание низкой концентрации кальция в период покоя кардиомиоцитов обеспечивается работой Са 2 +-АТФ-азы саркоплазматического ретикулума и Na+/Ca 2 + -обменника сарколеммы.
ПАТОГЕНЕТИЧЕСКИЕ ОСНОВЫ АРИТМИЙ
Изменения основных параметров потенциала действия, вызванные каким-либо патологическим процессом, нарушениями электролитного баланса или фармакологическими воздействиями, способны приводить к появлению аритмий или блокад.
В основе аритмий лежат нарушения автоматизма и проводимости. В одних случаях наблюдается уменьшение ЧСС в целом (снижение автоматизма) или частоты сокращений желудочков (замедление или нарушение проведения в а-в узле или системе Гиса-Пуркинье). Эти нарушения могут возникать как при органическом повреждении
проводящей системы, так и под действием лекарственных средств. В основе нарушений ритма, сопровождающихся повышением ЧСС, лежат 3 основных механизма: повышение автоматизма, триггерная активность (псевдоавтоматизм) и повторный вход возбуждения.
Повышение автоматизма
Повышение автоматизма возникает в клетках синусового узла, а-в узла и системы Гиса-Пуркинье., которым свойственна спонтанная диастолическая деполяризация. Стимуляция бета-адренорецепторов, гипокалиемия и механическое растяжение кардиомиоцитов увеличивают скорость спонтанной диастолической деполяризации и тем самым частоту самопроизвольных разрядов. Ацетилхолин, наоборот, снижает эту частоту, вызывая гиперполяризацию клеток. Автоматизм может возникать и в тех клетках, которым в норме он не свойственен. Такая ситуацмя может возникать при ишемии миокарда. Распространение возбуждения из очага повышенного или патологического автоматизма приводит к возникновению аритмии.
Триггерная активность (псевдоавтоматизм)
В некоторых патологических ситуациях достаточно сильный преждевременный импульс, развившийся в конце фазы реполяризации, может вызвать внеочередной потенциал действия (последеполяризацию). Это явление называют триггерной активностью, или псевдоавтоматизмом. Выделяют поздний и ранний тип последеполяризации. Поздняя деполяризация возникает после полной реполяризации в условиях повышенной внутриклеточной концентрации кальция (при ишемии, чрезмерной адренергической стимуляции, гликозидной интоксикации). Если поздняя последеполяризация достигает порога, возникает потенциал действия - триггерная активность. Аритмии, в основе которых, как считается, лежит поздняя последеполяризация, чаще возникают на фоне повышенной ЧСС.
Ранняя последеполяризация прерывает реполяризацию и при определенных условиях может вызвать триггерную активность. Ранняя последеполяризация чаще возникает при брадикардии, низкой внеклеточной концентрации калия и под действием лекарственных средств, увеличивающих продолжительность потенциала действия. Вероятность триггерной активности на фоне ранней после-
деполяризации увеличивается при стимуляции альфа- и бета-адренорецепторов. При значительном удлинении реполяризации может возникать полиморфная желудочковая тахикардия с удлиненным интервалом QT (желудочковая тахикардия типа «пируэт»).
Повторный вход возбуждения
Повторный вход возбуждения (контур) возникает при наличии 2 параллельных путей проведения между 2-ми участками сердца, обладающими разными электрофизиологическими свойствами,- разницей в рефрактерности в разных частях контура и задержкой проведения в одном из путей контура. Подобные анатомические контуры возникают в а-в узле при а-в узловой реципрокной аритмии без или с участием дополнительных путей проведения и в предсердиях при их трепетании. Повторный вход возбуждения может возникать и без анатомического контура. Замедление проведения в какомлибо участке миокарда в результате ишемии или других факторов может приводить к тому, что возбуждение выходит из этого участка тогда, когда остальной миокард уже вновь возбудим. Так, если кардиомиоциты возбуждаются сразу после того, как реполяризация достигает достаточного для возникновения потенциала действия уровня, может развиться фибрилляция предсердий или желудочков. В отличие от анатомически обусловленных контуров, такие контуры могут смещаться, и в сердце их может образовываться много. При этом возбуждение носит хаотический характер и координированного сокращения миокарда не происходит.
КЛАССИФИКАЦИЯ ААП
В соответствии с наиболее распространенной классификацией Вогана Вильямса (Vaughan Williams) выделяют 4 класса ААП (табл. 14.1). ААП классифицируются в зависимости от набора электрофизиологических свойств, благодаря которым они вызывают изменения скорости деполяризации и реполяризации клеток проводящей системы сердца.
В качестве ААП в практике используют и другие ЛС, которые по набору своих электрофизиологических свойств не могут быть отне-
Таблица 14.1
Классификация антиаритмических препаратов
сены ни в одну из групп классификации Вогана Вильямса. К ним относятся дигоксин (см. гл. «Сердечные гликозиды»), соли магния и калия, аденозин, карбомазепин и некоторые другие.
Электрофизиологические свойства препаратов определяют сходство их антиаритмического эффекта, но не фармакодинамические характеристики, которые у ААП, находящихся в одной группе, могут значительно различаться.
БЛОКАТОРЫ БЫСТРЫХ НАТРИЕВЫХ КАНАЛОВ. ПРЕПАРАТЫ I КЛАССА
Механизм действия
Основной характеристикой ААП I класса является их способность блокировать быстрые натриевые каналы. Вместе с тем многие из них оказывают блокирующее действие и на калиевые каналы (прокаинамид, хинидин, в меньшей степени пропафенон, дизапирамид), хотя и более слабое, чем препараты III-го класса. Взаимодействие препаратов с натриевыми каналами происходит во время потенциа-
ла действия (систолического сокращения), когда натриевые каналы открыты. В период потенциала покоя (диастолы) происходит постепенная диссоциация этой связи. При повышении ЧСС и укорочении диастолы препараты не успевают полностью выйти из связи с натриевыми каналами. Это приводит к их накоплению в каналах и, как следствие, усилению их блокады. Такое взаимоотношение между ЧСС и выраженностью антиаритмического действия называется прямой частотной зависимостью, т.е. чем выше ЧСС, тем сильнее натрийблокирующее действие препаратов. При постоянной деполяризации кардиомиоцитов, например при ишемии, диссоциация препаратов с каналами снижается, поэтому действие блокаторов медленных натриевых каналов более выражено в ишемизированной ткани.
Выраженность антиаритмического эффекта препаратов I класса зависит от скорости, с которой происходит высвобождение препарата из связи с натриевым каналом. Если препарат быстро диссоциирует из этой связи (быстрая кинетика связывания), блокада натриевого канала может быть слабой, а изменения скорости проведения минимальными. Скорость диссоциации комплекса «препарат-канал» характеризуется константой времени восстановления (τ восст.), равной времени, за которое восстанавливается примерно 63% каналов. При большой скорости восстановления каналов (малые значения τ восст.) высокая степень блокады натриевых каналов достигается
Таблица 14.2
Характеристика натрий-блокирующего действия ААП группы I
 лишь
при тахикардии или на фоне ишемии. При высоких значениях τ восст.
степень блокады каналов остается примерно одинаковой и в систолу, и в
диастолу даже при нормальной ЧСС и вне зависимости от наличия ишемии.
Соответственно выраженности натрий-блокирующего действия препараты I-го
класса подразделяются на 3 подкласса: IА, IB, и IC (табл. 14.2).
лишь
при тахикардии или на фоне ишемии. При высоких значениях τ восст.
степень блокады каналов остается примерно одинаковой и в систолу, и в
диастолу даже при нормальной ЧСС и вне зависимости от наличия ишемии.
Соответственно выраженности натрий-блокирующего действия препараты I-го
класса подразделяются на 3 подкласса: IА, IB, и IC (табл. 14.2).
Препараты класса IА, блокируя быстрые натриевые каналы, замедляют фазу 0 потенциала действия и умеренно замедляют скорость проведения импульса в тканях с быстрым потенциалом действия. Благодаря блокаде калиевых каналов удлиняется потенциал действия и рефрактерность. Препараты способны прекращать циркуляцию волны возбуждения за счет снижения проводимости при наличии анатомического контура повторного входа возбуждения (re-entry). Эти электрофизиологические эффекты проявляются как в предсердной, так и желудочковой тканях, поэтому препараты класса I А имеют потенциальную эффективность как при предсердных, так и желудочковых тахиаритмиях. Препараты способны подавлять автоматизм синусового узла, что чаще проявляется при его патологии.
ААП класса IB оказывают относительно малое воздействие на быстрые натриевые каналы при нормальных частотах сердечного ритма, а значит, и на скорость проведения. Их основной эффект состоит в уменьшении продолжительности потенциала действия и, как следствие, укорочении рефрактерных периодов. Однако при высокой частоте сердечного ритма, а также на фоне ишемии миокарда, гипокалиемии или ацидоза некоторые препараты, например, лидокаин, могут существенно замедлять деполяризацию и скорость проведения импульса. На предсердия ААП IB влияют незначительно (за исключением фенитоина), и поэтому полезны только для лечения желудочковых аритмий. Препараты подавляют автоматизм синусового узла.
Для ААП класса IC характерно выраженное действие на быстрые натриевые каналы, так как они обладают медленной кинетикой связывания, что определяет существенное замедление скорости проведения даже при нормальных частотах сердечного ритма. Влияние этих препаратов на реполяризацию незначительное. Препараты класса IC оказывают сопоставимый эффект на предсердную и желудочковую ткани и полезны как при предсердных, так и желудочковых тахиаритмиях. Препараты подавляют автоматизм синусового узла. В отличие от других препаратов IC класса пропафенон способствует небольшому увеличению рефрактерных периодов во всех тканях
сердца. Кроме того, пропафенон имеет умеренно выраженное β-блокирующее и кальций-блокирующее свойства.
Фармакокинетика
Большинство препаратов 1 класса достаточно хорошо и полно всасываются. Медленной и вариабельной абсорбцией отличается фенитоин (табл. 14.3).
В плазме крови препараты в значительной степени связываются преимущественно с альбуминами. Хинидин, лидокаин и пропафенон связываются также и с a 1 -кислым гликопротеидом - белком острой фазы воспаления. При инфаркте миокарда и других острых состояниях концентрация этого белка увеличивается, что приводит к снижению доли свободной фракции препаратов. В таких случаях для достижения антиаритмического эффекта могут потребоваться более высокие дозы препаратов. Связывание дизопирамида с белком плазмы насыщаемо и зависит от введенной дозы - чем выше доза, тем меньше связь с белками. Поэтому при небольшом увеличении общего количества дизопирамида концентрация свободного препарата может увеличиваться значительно. В норме связь фенитоина с белками плазмы достигает 90%. При гипоальбуминемии доля связанного фенитоина может снижаться до 80%, а концентрация свободного препарата удваивается. В этом случае требуется контролировать концентрацию свободного, а не общего фенитоина. Слабой связью с белком отличается прокаинамид.
Несмотря на достаточно полное всасывание, лидокаин, пропафенон, морицизин и лаппаконитин подвергаются выраженной метаболизации при первом прохождении через печень, в результате чего их биодоступность снижается. Значительный, но непостоянный эффект первого прохождения является причиной того, что лидокаин не назначается внутрь. Выраженный эффект первого прохождения через печень определяет нелинейную кинетику пропафенона. При повышении его дозы происходит насыщение одного из ферментов, метаболизирующих препарат, и дальнейшее повышение дозы пропафенона может привести к резкому скачку сывороточной концентрации. Угнетение этого фермента возможно и при совместном назначении пропафенона с хинидином или флуоксетином. Насыщаемый метаболизм с теми же самыми последствиями характерен и для фенитоина. Биодоступность хинидина, дизопирамида, мексилетина, прокаинамида и фенитоина превышает 80%.
Фенитоин является индуктором микросомальных окислительных ферментов печени, чем определяются многие эффекты взаимодействия этого препарата.
В процессе биотрансформации хинидина, прокаинамида, дизопирамида, лидокаина, пропафенона, морицизина и лаппаконитина образуются активные метаболиты, способные в большей или меньшей степени усиливать или продлевать антиаритмическое действие исходных препаратов. Некоторые из них имеют другие фармакологические свойства. Так, активный метаболит дизапирамида обладает выраженным холинолитическим действием. N-ацетилпрокаинамид - активный метаболит прокаинамида, проявляет антиаритмические свойства препаратов III-го, а не I-го класса, имеет более длинный TS (6-10 ч) и не вызывает волчаночно-подобный синдром. Более длинные TS имеют и некоторые метаболиты мексилетина. Активные метаболиты лидокаина способны конкурировать с лидокаином за участки связывания в быстрых натриевых каналах, а также за ферменты печени, что отражается на активности и продолжительности действия лидокаина. Один из активных метаболитов лаппаконитина проникает через ГЭБ и определяет побочные эффекты: двоение в глазах, головную боль, головокружение; второй метаболит обладает слабым вазодилатирующим действием.
Хинидин, лидокаин, мексилетин, пропафенон и морицизин практически полностью элиминируются печенью, остальные препараты I группы - печенью и почками.
Из-за высокой экскреции почками в неизмененном виде дозы дизопирамида и прокаинамида при почечной недостаточности необходимо снижать. Тяжелые заболевания печени вызывают задержку элиминации лидокаина и пропафенона, что также требует снижения их дозировок.
Применение
Подгруппа IA. Хинидин, прокаинамид, дизопирамид, аймалин прежде всего используют для купирования мерцательной аритмии и профилактики рецидивов, лечении трепетания предсердий (малоэффективны), пароксизмальной наджелудочковой тахикардии, частой предсердной и желудочковой экстрасистолии, желудочковой тахикардии. Эффективность этих препаратов для купирования недавно возникшего пароксизма мерцательной аритмии высока, однако
Таблица 14.3
Некоторые показатели фармакокинетики ААП I класса
 * - зависит от дозы; ** - практически сразу при в/в введении; *** - при медленной метаболизации TS равен 10-32 ч.
* - зависит от дозы; ** - практически сразу при в/в введении; *** - при медленной метаболизации TS равен 10-32 ч.
использование их для профилактики повторных пароксизмов не может предотвратить рецидивов аритмии более чем у половины больных.
Подгруппа IB. Лидокаин, мексилетин, фенитоин применяют для лечения желудочковой экстрасистолии у больных, инфарктом миокарда. Они относятся к препаратам выбора для лечения желудочковой экстрасистолии вследствие гликозидной интоксикации. Кроме того, эти препараты используют при аритмиях центрального генеза и нарушениях сердечного ритма, возникающих при анестезии и операциях на сердце. В отличие от других препаратов этой группы фенитоин имеет более широкие показания. Препарат эффективен не только при желудочковых, но и наджелудочковых аритмиях, вызванных интоксикацией дигиталисом либо другой этиологии, а также применяется у больных с синдромом врожденного удлинения интервала QT.
Подгруппа IC Этмозин, этацизин, пропафенон, лаппаконитин используют как для профилактики, так и для лечения наджелудочковых и желудочковых аритмий. Их эффективность сравнима с эффективностью препаратов I A класса.
Препараты с малой константой восстановления (I В группа) неэффективны при мерцательной аритмии и трепетании предсердий, тогда как препараты I А и I С групп могут быть полезны. Возможно, это обусловлено их способностью блокировать калиевые каналы.
По данным большинства исследователей, блокаторы медленных натриевых каналов предотвращают пароксизмы реципрокной желудочковой тахикардии у 20-40% больных. Сочетание препаратов с большой и малой константой восстановления может быть эффективнее и безопаснее монотерапии этими же препаратами, даже в тех случаях, когда ни один из них по отдельности не действует.
Нежелательные эффекты
Большая часть побочных эффектов ААП связана с их основными электорофизиологическими действиями. Благодаря удлинению АВ проводимости многие ААП I А класса могут вызвать атриовентрикулярную и внутрижелудочковую блокады. Вероятность их развития повышается с увеличением дозы. Пропафенон и фенитоин также могут нарушать проводимость. Лидокаин не вызывает развития брадикардии и блокад, поскольку не удлиняет АВ проведение.
Пропафенон обладает угнетающим действием на синусовый узел и может вызывать слабость синусового узла, а при быстром введении - преходящую остановку сердца. В редких случаях возможна АВ диссоциация. Удлинение интервала QT характерно для препаратов IА класса и обусловливает риск развития желудочковой тахикардии типа «пируэт». Фенитоин и морицизин способны укорачивать продолжительность интервала QT, другие препараты I В и I С классов мало влияют на него.
Аритмогенный эффект
ААП I класса, помимо антиаритмического, способны вызывать аритмогенный эффект, т.е. могут сами провоцировать аритмии, в том числе опасные для жизни. Это свойство всех ААП напрямую связано с их основными механизмами действия, а именно с изменением скорости проведения и продолжительности рефрактерных периодов. Так, изменение скорости проведения в различных участках петли реентри благоприятствует циркуляции волны возбуждения по контуру повторного входа. Чаще других усугубление реципрокных аритмий вызывают препараты 1С класса (пропафенон, флекаинид), так как они выражено замедляют скорость проведения. В несколько меньшей степени это свойство выражено у препаратов 1А класса (хинидин), еще меньше у препаратов 1В класса. Развитие желудочковых тахикардий по механизму повторного входа возбуждения наиболее вероятно у пациентов с заболеваниями сердца на фоне ишемии миокарда и при значительном (на 20-25%) расширении комплекса QRS.
При брадикардии удлинение потенциала действия может привести к появлению триггерной активности (псевдоавтоматизма) на фоне ранней последеполяризации и развитию желудочковой тахикардии типа «пируэт». Этот вид аритмий вызывают ААП IА класса, поскольку именно они способны блокировать калиевые каналы и вызывать удлинение потенциала действия. Возможны и другие аритмогенные эффекты. При назначении ААП IА класса может возникнуть улучшение проведение через а-в узел, обусловленное наличием у них м-холинолитического эффекта. Возникающее при этом повышение частоты желудочковых сокращений особенно опасно при трепетании предсердий. Холинолитический эффект выражен у хинина и в меньшей степени у дизопирамида.
Препараты IВ класса редко оказывают аритмогенное действие.
Гемодинамические эффекты ААП 1 класса
Большинство ААП оказывают влияние на показатели гемодинамики, что в зависимости от их выраженности ограничивает возможности их применения, выступая как побочные эффекты. Выраженным гипотензивным действием обладают препараты 1А класса, благодаря способности блокировать α-адренорецепторы. Этот эффект проявляется особенно ярко при в/в введении препаратов. Исключением является дизопирамид, который способен вызывать повышение тонуса артериол. Дизопирамид, а также пропафенон и другие препараты IC класса обладают достаточно выраженным отрицательным инотропным эффектом, из-за которого их не рекомендуют назначать больным с сердечной недостаточностью. Прокаинамид оказывает значительно более слабое действие на сократимость миокарда. Наименьшее влияние на уровень АД и сократимость миокарда оказывает лидокаин. Выраженное отрицательное инотропное действие наблюдается только при его высокой концентрации в плазме крови.
Антихолинергическое действие, присущее препаратам IА группы, проявляется улучшением проведения через а-в узел, сухостью во рту, нарушением аккомодации, затруднением мочеиспускания, особенно у пожилых больных с гипертрофией предстательной железы. Антихолинергическое действие в меньшей степени выражено у прокаинамида.
Пропафенон может вызывать бронхоспазм, что обусловлено его способностью блокировать β-адренорецепторы бронхов.
Лечение препаратами I А и I С классов может сопровождаться неблагоприятными явлениями со стороны желудочно-кишечного тракта, такими как тошнота, рвота, диарея, нарушение функции печени, внутрипеченочный холестаз.
Основными побочными действиями I В группы являются нежелательные эффекты со стороны ЦНС, которые включают головокружение, сонливость, судороги, нарушения слуха, тремор и пр. Наименьшее количество побочных реакций наблюдается при применении терапевтических доз лидокаина. Однако в токсических дозах лидокаин, обладая свойствами местных анестетиков, может вызывать судороги, обмороки и даже остановку дыхания. Препараты IА класса могут вызывать головные боли и двоение в глазах.
Нежелательные явления центрального генеза - головные боли, нарушения зрения, вкуса, парестезии, нарушения координации, могут развиваться и при лечении препаратами IС класса.
Помимо перечисленных эффектов, отдельные препараты I класса способны вызывать аллергические реакции (дизопирамид, пропафенон, фенитоин, аймалин, хинидин); агранулоцитоз (фенитоин, пропафенон, аймалин); лейкопению (фенитоин, пропафенон); тромбоцитопении (фенитоин, пропафенон, хинидин); лекарственную лихорадку (прокаинамид, хинидин).
Противопоказания
Общими противопоказаниями практически для всех ААП являются наличие атриовентрикулярной блокады II-III степени и других нарушений проводимости, брадикардии (за исключением лидокаина и морицизина), синдрома слабости синусового узла (кроме IА), сердечной недостаточности II-III стадии и гипотонии (кроме лидокаина и лаппаконитина) и кардиогенном шоке (кроме аймалина, фенитоина и лаппаконитина). Применение ААП IА класса противопоказано при удлинении интервала QT более 440 мс.
При миастении не назначают хинидин, прокаинамид, лидокаин и пропафенон. Применение хинидина, прокаинамида, лаппаконитина и морицизина противопоказано при повышенной к ним индивидуальной чувствительности. При бронхиальной астме и ХОБЛ не назначают хинидин, прокаинамид и пропафенон.
Дизопирамид и хинидин, благодаря холинолитическому действию, могут ухудшить состояние больных с глаукомой и аденомой предстательной железы. Прокаинамид противопоказан у больных системной красной волчанкой, мексилетин - при паркинсонизме, пропафенон не следует использовать у больных с выраженными электролитными нарушениями, лидокаин, мексилетин и фенитоин - при наличии у больного в анамнезе эпилептиформных судорог.
Большинство препаратов I класса противопоказаны при тяжелой печеночной и почечной недостаточности, а также при беременности. Фенитоин может оказывать тератогенный эффект. Многие препараты не назначают или назначают с осторожностью кормящим женщинам.
Взаимодействия
ААП имеют достаточно широкий спектр лекарственных взаимодействий как фармакодинамического, так и фармакокинетического характера.
Многие индукторы микросомальных ферментов печени (фенобарбитал, фенитоин, рифампицин) ускоряют метаболизм препаратов IА группы, а также лидокаина, мексилетина и пропафенона, снижая их концентрации в плазме крови. Алкоголь, индуцируя активность ферментов печени, снижает концентрацию прокаинамида, а изониазид и хлорамфеникол - концентрацию мексилетина.
Препараты, ингибирующие ферменты печени, замедляют скорость метаболизма многих ААП. Так, амиодарон повышает плазменные концентрации хинидина, прокаинамида, фенитоина и этацизина. На фоне приема циметидина повышаются концентрации прокаиамида, лидокаина, пропафенона и морицизина.
Сами ААП способны потенцировать эффекты друг друга при совместном назначении. Хинидин увеличивает концентрацию аймалина, пропафенона и этацизина. Фенитоин повышает концентрации хинидина, дизопирамида, лидокаина и мексилетина. Сам мексилетин способен усиливать побочные эффекты лидокаина. Пропафенон снижает выведение метопролола и пропранолола, поэтому их дозы при применении пропафенона следует уменьшить.
Широк круг взаимодействий ААП и с другими препаратами. Лидокаин потенцирует действие внутривенных анестетиков, снотворных и седативных препаратов, а также миорелаксантов. Хинидин и пропафенон повышают плазменные концентрации дигоксина и вафарина, что необходимо учитывать при совместном назначении. Многие ААП (мексилетин, пропафенон, морицизин, фенитоин) повышают концентрацию теофиллина в крови. Лаппаконитин усиливает эффекты недеполяризующих миорелаксантов, дизопирамид повышает кардиодепрессивный эффект препаратов с отрицательным инотропным действием, морицизин - побочные эффекты ингибиторов МАО, хинидин - действие холинолитических средств. Прокаинамид потенцирует действие антиаритмических, холинолитических и цитостатических средств, а также миорелаксантов.
БЛОКАТОРЫ КАЛИЕВЫХ КАНАЛОВ. ПРЕПАРАТЫ III КЛАССА
Механизм действия
Общий механизм антиаритмического эффекта препаратов класса III заключается в удлинении потенциала действия путем блокирова-
ния калиевых каналов, опосредующих процесс реполяризации, и в увеличении таким образом рефрактерных периодов сердечной ткани. Конечным эффектом является подавление реципрокных аритмий. Препараты способны подавлять автоматизм (амиодарон в большей, а бретилий в меньшей степени, чем другие), вызывать последеполяризацию и удлинять интервал QT. В отличие от других представителей этой группы ибутилид удлиняет потенциал действия преимущественно путем блокады входящих натриевых потоков, а не выходящих калиевых.
Выраженность блокады калиевых каналов, вызываемой препаратами III класса, характеризуется обратной частотной зависимостью. Это обусловлено тем, что в отличие от АПП I класса, которые связываются с натриевыми каналами в период их открытия, АПП III класса взаимодействуют с закрытыми калиевыми каналами. При медленном ритме фаза 4 потенциала действия удлиняется, и калиевые каналы находятся в закрытом состоянии более длительное время, чем при частом ритме. Поэтому время контакта препаратов с местом связывания, а следовательно, и эффект увеличиваются при медленном ритме и уменьшаются при частом. Амиодарон, в отличие от других препаратов группы, связывается преимущественно с открытыми калиевыми каналами, поэтому его эффект практически не имеет частотной зависимости.
Все представители этого класса препаратов взаимодействуют и с другими каналами или рецепторами, что вносит свой вклад в их эффективность и токсичность. Так, соталол блокирует β-адренорецепторы, бретилий препятствует обратному захвату норадреналина окончаниями симпатических нейронов, ибутилид и амиодарон блокирует натриевые каналы, кроме того, амиодарон в некоторой степени блокирует кальциевые каналы и вызывает неконкурентную блокаду β-адренорецепторов, обладая, таким образом, свойствами всех 4 классов.
Препараты III класса повышают порог развития фибрилляции желудочков, оказывая антифибрилляторное действие.
Фармакокинетика
Все препараты III класса характеризуются неполным всасыванием из ЖКТ, что снижает их биодоступность (табл. 14.4). Исключение составляет соталол, чья биодоступность, благодаря хорошей всасы-
Таблица 14.4
Некоторые показатели фармакокинетики ААП III класса
 ваемости
из ЖКТ, составляет почти 100%. Низкая биодоступность ибутилида
объясняется выраженным эффектом первого прохождения через печень.
ваемости
из ЖКТ, составляет почти 100%. Низкая биодоступность ибутилида
объясняется выраженным эффектом первого прохождения через печень.
Препараты в разной мере связываются с белками плазмы: 99,9% амиодарона находится в связанном состоянии, тогда как соталол и бретилий почти не связываются с альбуминами плазмы.
Амиодарон, бретилат и ибутилид способны проникать во многие органы и ткани. Это особенно характерно для амиодарона, который благодаря выраженной липофильности накапливается в печени, жировой ткани, коже, легких, миокарде, щитовидной железе и скелетной мускулатуре. В отличие от них соталол имеет низкий объем распределения и слабо проходит через тканевые барьеры.
Препараты с разной скоростью и в разном объеме метаболизируются в печени. Соталол и бретилий практически не подвергаются метаболизации в печени и экскретируются почками в неизмененном виде. Быстро и достаточно полно метаболизируются ибутилид и нибентан. Они экскретируются почками в основном в виде неактивных соединений. Период полувыведения этих препаратов составляет несколько часов. Амиодарон также почти полностью метаболизируется в печени и выводится из организма в виде неактивных метаболитов. Однако благодаря способности кумулировать в тканях амиодарон элиминируется очень медленно. Его период полувыведения варьирует в широких пределах от 2 недель до 3 мес при постоянном прием, а при однократном в/в введении составляет в среднем 14 ч.
Применение
Несмотря на общность основного электрофизиологического механизма, препараты Ш класса не взаимозаменяемы. Амиодарон является универсальным антиаритмическим средством, применяемым для купирования как желудочковых, так и наджелудочковых (в том числе на фоне WPW) аритмий. Амиодарон эффективен также для поддержания синусового ритма у больных с мерцательной аритмией.
Соталол также может применяться при всех типах тахиаритмий. Его эффективность при желудочковых аритмиях не уступает большинству препаратов I класса, хотя и ниже, чем у амиодарона.
Нибентан и ибутилид эффективны для лечения предсердных пароксизмальных аритмий: трепетания или фибрилляции предсер-
дий. Внутривенное введение препаратов быстро восстанавливает синусовый ритм. Эффективность нибентана и ибутилида при трепетании предсердий несколько выше, чем при фибрилляции. Лечение этими препаратами следует проводить только при постоянном мониторировании ЭКГ и при наличии условий для проведения экстренной кардиоверсии в случае развития аритмогенных эффектов. Лечение препаратами наиболее успешно в первые несколько дней после начала пароксизма, в более поздние сроки их эффективность заметно ниже.
Бретилия тозилат применяется только для лечения пароксизмальных желудочковых аритмий, вызванных оперативным вмешательством на сердце и при остановке сердца вследствие фибрилляции желудочков. Препарат оказывает эффект при желудочковых аритмиях, рефрактерных к действию других ААП, а также аритмии типа «пируэт». Бретилий понижает порог дефибрилляции (снижает необходимую для дефибрилляции мощность разряда) и предупреждает рецидив фибрилляции желудочков у больных с выраженной сердечной патологией.
Нежелательные эффекты
Благодаря удлинению АВ проводимости амиодарон и соталол могут вызвать брадикардию, а благодаря подавлению автоматизма синусового узла ухудшать состояние при СССУ. Брадикардия редко возникает при назначении бретилия, ибутилида и нибентана, поскольку препараты практически не удлиняют АВ проведения и не влияют на автоматизм синусового узла.
Аритмогенный эффект препаратов III класса напрямую связан с их основным электрофизиологическим свойством - способностью удлинять потенциал действия. На фоне значительного удлинения потенциала действия может возникнуть ранняя последеполяризация, которая при достаточной выраженности по механизму триггерной активности приводит к развитию полиморфной желудочковой тахикардии типа «пируэт». Благодаря обратной частотной зависимости удлинение потенциала действия при назначении препаратов III класса наиболее выражено при брадикардии. Ранняя последеполяризация часто возникает при низкой внеклеточной концентрации калия и на фоне стимуляции α- и β-адренорецепторов. У больных с мерцательной аритмией желу-
дочковая тахикардия типа «пируэт» может возникать при снижении ЧСС после восстановления ритма. Для возникновения данной формы тахиаритмии наличие сердечной патологии не обязательно. Чаще дозозависимое удлинение интервала QT и тахикардия типа «пируэт» наблюдаются при применении соталола, ибутилида и нибентана, практически никогда - при применении бретилия тозилата. Хотя амиодарон, так же как и другие препараты III группы, вызывает блокаду калиевых каналов и соответственно удлиняет интервал QT, при его в/в введении редко наблюдается развитие желудочковой тахикардии.
Из-за высокого риска развития аритмогенного эффекта в первые часы после назначения ибутилида, нибентана и дофетилида необходимо мониторирование ЭКГ.
Гемодинамические эффекты
Бретилия тозилат, соталол и амиодарон способны снижать уровень АД. В наибольшей степени этот эффект выражен у бретилия, который по своему механизму действия является симпатолитическим средством. Бретилий накапливается в периферических адренергических нервных окончаниях, и его первичный эффект связан с высвобождением норадреналина из нервных окончаний, что в течение нескольких минут может сопровождаться повышением АД и тахикардией с риском развития желудочковой аритмии. Часто, на фоне нестабильной гемодинамики, это действие остается незамеченным. В дальнейшем бретилий блокирует выброс норадреналина, развивается адренергическая блокада нейронов и довольно часто артериальная гипотония, в ряде случаев требующая введение инфузионных растворов. Соталол может вызывать снижение АД благодаря своему неселективному β-блокирующему действию. Снижение АД часто наблюдается и при в/в введении амиодарона, что обусловлено его вазодилатирующими свойствами, связанными с неконкурентной блокадой α-адренорецепторов. При в/в введении (5-10 мг/кг) амиодарон может вызывать снижение сократимости миокарда, однако при длительном применении отрицательный инотропный эффект не выявляется даже у больных с тяжелой ХСН. Соталол, благодаря способности блокировать β-адренорецепторы сердца, снижает сократимость миокарда, особенно при низких значениях сердечного выброса. Другие препараты III класса не влияют на сократимость миокарда.
Амиодарон и соталол могут вызывать бронхоспазм, что обусловлено их способностью блокировать β-адренорецепторы бронхов. Многие нежелательные действия амиодарона зависят не только от величины суточной дозы, но и от общей комулятивной (курсовой) дозы препарата, что связано с накоплением препарата в тканях. При длительной терапии амиодароном возрастает риск развития таких осложнений, как легочный фиброз (потенциально летальное состояние), гепатит, периферическая нейропатия, фотосенсибилизация, нарушение функции щитовидной железы (за счет входящего в структуру амиодарона йода), отложения пигмента в роговице и коже.
Противопоказания
ААП III класса противопоказаны при удлинении корригированного интервала QT более 440-500 мс, гипокалиемии, гипомагниемии, выраженной синусовой брадикардии, на фоне которых повышается риск развития желудочковой тахикардии типа «пируэт». Хотя амиодарон, так же как и другие препараты III группы, вызывает блокаду калиевых каналов и соответственно удлиняет интервал QT, при его в/в введении редко наблюдается развитие желудочковой тахикардии. Поэтому небольшое удлинение QT не является показанием к прекращению его введения. Амиодарон и соталол не следует назначать при а-в блокадах, а соталол при декомпенсированной сердечной недостаточности. При бронхиальной астме противопоказан соталол, а амиодарон должен назначаться с осторожностью. Амиодарон противопоказан также при заболеваниях легких и нарушениях функции щитовидной железы. Противопоказанием к назначению бретилия тозилата служит артериальная гипотензия, аортальный стеноз, гипертрофическая кардиомиопатия.
Взаимодействия
Амиодарон значительно подавляет печеночную и почечную элиминацию многих других препаратов. Применение амиодарона у больных, получающих одновременно дигоксин, способствует вытеснению последнего из связи с белками и повышению его плазменной концентрации. Амиодарон у больных, получающих варфарин, теофиллин, хинидин, прокаинамид, уменьшает их клиренс. В результате действие указанных препаратов усиливается. Одновременное
использование амиодарона и β-блокаторов увеличивает риск возникновения гипотонии и брадикардии.
Бретилий увеличивает токсичность сердечных гликозидов, усиливает прессорное действие вводимых внутривенно катехоламинов (норэпинефрина, добутамина). Бретилий может потенцировать гипотензивное действие используемых одновременно вазодилататоров. Параллельное назначение бретилия с другими антиаритмическими препаратами иногда снижает его эффективность.
Для снижения риска развития аритмогенного эффекта ибутилид не назначают одновременно с ААП IA и III классов. Потенцировать аритмогенный эффект ибутилида могут также фенотиазиновые производные, трициклические и тетрациклические антидепрессанты и некоторые антигистаминные средства, способные удлинять интервал. Антагонисты кальция и β-блокаторы повышают риск развития брадикардии и а-в блокады.
Соталол усиливает гипертенвивное действие ингибиторов МАО и норэпинефрина, усиливает нейромышечную блокаду тубокурарина, повышает концентрацию лидокаина и флекаинида, снижает концентрацию теофиллина и β2 -стимуляторов.
В свою очередь гипотензивный и брадикардитический эффект соталола может потенцироваться другими ЛС, обладающими такими же эффектами (СГ, симпатолитики, антагонисты кальция, трициклические антидепрессанты, фенотиазины, барбитураты, наркотические анальгетики, диуретики, галоперидол, другие вазодилататоры). Сочетание соталола с амиодароном повышает риск развития аритмогенных эффектов. Одновременное применение соталола и производных сульфонилмочевины может усилить гипогликемическое действие последних.
ААП, НЕ ВОШЕДШИЕ В КЛАССИФИКАЦИЮ ВОГАНА ВИЛЬЯМСА
Аденозин
Аденозин, эндогенный нуклеозид, является блокатором пуриновых (аденозиновых) рецепторов.
Угнетение А 1 -пуриновых рецепторов приводит к открытию холинозависимых калиевых каналов в кардиомиоцитах предсердий,
синусового узла и а-в узла, что вызывает укорочение потенциала действия, гиперполяризацию, снижение автоматизма синусового узла и скорости проведения в а-в узле. Кроме того, аденозин увеличивает рефрактерность а-в узла и подавляет позднюю последеполяризацию, возникающую в ответ на адренергические воздействия. Последние эффекты обусловлены подавлением электорофизиологического действия внутриклеточного цАМФ, уровень которого повышается при адренергической стимуляции, и уменьшением входа ионов кальция в клетку.
Описанные механизмы приводят к торможению проведения через АВ-узел, перерыву в механизме реентри в АВ-узле и восстановлению синусового ритма при пароксизмах наджелудочковой тахикардии, в том числе при синдроме WPW. Однако у больных с мерцанием и трепетанием предсердий при наличии дополнительного пучка проведения аденозин увеличивает проводимость по этому пути. Эффективность аденозина зависит от патогенеза аритмии. При предсердной аритмии, вызванной повторным входом возбуждения в синусовом узле или триггерной активностью, аденозин проявляет купирующий эффект, а при предсердной тахикардии, обусловленной повышенным автоматизмом, препарат вызывает только преходящее подавляющее действие.
Через блокаду А 2 -пуриновых рецепторов аденозин может повышать тонус бронхиол, вызывать дилатацию периферических артерий, в том числе коронарных (А 2 -пуриновые рецепторы гладких мышц сосудов) и угнетать ЦНС. Однако все эффекты аденозина кратковременны.
Фармакокинетика
Действие аденозина при быстром в/в введении начинается приблизительно через 10 с. Сразу после попадания в кровоток аденозин захватывается эритроцитами и эндотелиальными клетками сосудов, в которых он быстро метаболизируется путем дезаминирования и фосфорилирования с образованием электрофизиологически неактивных метаболитов инозина и аденозинмонофосфата. Так как метаболизм препарата не связан с печенью, наличие печеночной недостаточности не оказывает влияния на период полувыведения аденозина, который равен примерно 10 с. Аденозин экскретируется почками в виде неактивных соединений. Преобладающим конечным метаболитом является мочевая кислота.
Побочные эффекты аденозина незначительны вследствие кратковременности его действия. Препарат может вызвать артериальную гипотензию (главным образом при медленной в/в инфузии). При увеличении дозы аденозина возможно развитие выраженной брадикардии, которая быстро проходит после прекращения инфузии или в/в введения атропина. Применение аденозина в больших дозах может вызвать угнетение активности синусового узла и автоматизма желудочков, и, как следствие этого, преходящее выпадение сердечных циклов.
Среди других побочных эффектов аденозина - способность вызывать диспноэ, гипервентиляцию, бронхоспазм, уменьшать легочное сосудистое сопротивление. Подобно нитроглицерину и нитропруссиду натрия, хотя и в значительно меньшей степени, аденозин может увеличивать внутрилегочное шунтирование и снижать SaO 2 в результате подавления легочной гипоксической вазоконстрикции. Введение аденозина может сопровождаться кратковременным сужением почечных сосудов, снижением почечного кровотока, скорости клубочковой фильтрации и диуреза. Возможны также аллергические реакции, гиперемия лица, повышенное потоотделение, боли в грудной клетке, нижней челюсти, горле или руках.
Противопоказания
Исходя из возможных нежелательных действий, аденозин не назначают при AV блокаде степени и СССУ (за исключением пациентов с искусственным водителем ритма), и при желудочковой тахикардии.
Взаимодействия
Эффекты аденозина ослабляют ксантины (теофиллин, кофеин), так как они являются конкурентными антагонистами аденозина. Дипиридамол усиливает его эффекты. Карбамазепин может усилить а-в блокаду, вызванную аденозином.
Магния сульфат
Механизм действия и фармакологические эффекты
Механизм антиаритмического действия магния неизвестен. Существует предположение, что он влияет на входящие кальциевые токи, определяющие триггерную активность на фоне ранней последеполяризации.
Сульфат магния обладает многими другими эффектами на органы и системы организма: оказывает седативное, снотворное, наркотическое (в больших дозах), противосудорожное, токолитическое действие, понижает возбудимость дыхательного центра, угнетает нервно-мышечную передачу, повышает диурез, обладает слабительным и желчегонным (при приеме внутрь) эффектами.
Фармакокинетика
Всасывание магния из ЖКТ неполно, вариабельно, в значительной степени зависит от содержания его в пище. Поэтому для экстренного лечения сердечных аритмий магний вводится в/в.
Магний способен проникать через ГЭБ и плацентарный барьер, а также в материнское молоко, где его концентрации в 2 раза превышают таковые в плазме. Выведение осуществляется почками со скоростью, пропорциональной его концентрации в плазме и уровню клубочковой фильтрации. Концентрация магния в сыворотке крови может не отражать его содержание в организме.
Применение
В качестве ААП магний преимущественно используется для лечения полиморфной желудочковой тахикардии типа «пируэт». Это определяется быстротой действия сульфата магния при в/в введении, высокой эффективностью даже при отсутствии гипомагниемии и относительной безопасностью. Магний также применяется при аритмиях, вызванных гликозидной интоксикацией, при которых он устраняет подавление натрий-калиевого насоса, вызываемое СГ. Поскольку сульфат магния способен замедлять проведение по а-в узлу, его применяют для купирования суправентрикулярных тахиаритмий, в которых а-в узел играет ключевую роль. Магний назначают внутрь для профилактики гипомагниемии, однако данных о том, что длительный прием магния внутрь оказывает непосредственное антиаритмическое действие, нет.
Побочное действие
Нежелательные эффекты препарата обусловлены превышением нормальной концентрации ионов магния в организме. Ранние клинические признаки и симптомы гипермагниемии: брадикардия, диплопия, внезапный «прилив» крови к коже лица, головная боль, снижение АД, тошнота, одышка, смазанность речи, рвота, астения.
Кроме того, возможны гипергидроз, тревожность, глубокая седация, полиурия, атония матки. Гипермагниемия сопровождается снижением глубоких сухожильных рефлексов, удлинением интервала P-Q и расширением комплекса QRS на ЭКГ. В высоких концентрациях происходит утрата глубоких сухожильных рефлексов, угнетение дыхательного центра, нарушение проводимости сердца и его остановка. Для лечения передозировки в/в медленно вводят раствор CaCl2 или кальция глюконата - 5-10 мл 10%, проводят оксигенотерапию, вдыхание карбогена, искусственное дыхание, перитонеальный диализ или гемодиализ, симптоматическую терапию.
Противопоказания
Сульфат магния не назначают при артериальной гипотензии, угнетении дыхательного центра, выраженной брадикардии, AV блокаде, при тяжелой ХПН (КК менее 20 мл/мин) и в предродовом периоде (за 2 ч до родов).
Взаимодействие
При совместном применении магния сульфата для парентерального введения с другими вазодилататорами возможно усиление гипотензивного эффекта. Совместное назначение барбитуратов, наркотических анальгетиков и других ЛС, угнетающих ЦНС, повышает вероятность угнетения дыхательного центра. Сердечные гликозиды увеличивают риск нарушения проводимости и AV блокады (особенно при одновременном в/в введении солей кальция). Миорелаксанты и нифедипин могут усилить нервно-мышечную блокаду.
Препараты калия
Механизм действия и фармакологические эффекты
Введение в организм калия вызывает снижение проводимости и возбудимости миокарда, а в высоких дозах - угнетение сократительной активности миокарда и автоматизма. Препараты калия оказывают и другие действия на организм: в малых дозах расширяют коронарные сосуды, а в больших - суживают их, улучшают сократимость скелетных мышц, оказывают умеренное диуретическое действие (в высоких дозах).
Фармакокинетика
Соли калия легко и полно всасываются при приеме внутрь и относительно быстро выводятся почками.
Применение
Препараты калия показаны при повышении автоматизма а-в узла или миокарда желудочков (даже при нормальном уровне калия в сыворотке), если нет выраженной а-в блокады. Профилактически соли калия вводят при низком содержании калия в плазме крови, поскольку состояние гипокалиемии сопряжено с повышенным риском развития аритмий вследствие возникновения ранних и поздних последеполяризаций и усиления эктопической активности, что особенно выражено на фоне сердечных гликозидов. Нормализация уровня калия при этих состояниях снижает опасность развития аритмий, что дает основание использовать соли калия для лечения и профилактики дигиталисной интоксикации. Препараты калия могут применяться также для профилактики аритмии у больных с острым инфарктом миокарда и для лечения экстрасистолии.
Побочные действия
Появление нежелательных эффектов связано с развитием гиперкалиемии. Ранними признаками интоксикации являются парастезии конечностей, замедление а-в проводимости, парадоксальное увеличение экстросистол, снижение АД, которые обычно появляются при концентрации ионов калия в сыворотке крови более 6 мэкв/л. Более тяжелыми симптомами гиперкалиемии являются паралич мускулатуры и остановка сердца, развивающиеся при концентрации калия 9-10 мэкв/л.
Противопоказания
Препараты калия не назначают при гиперкалиемии, полной а-в блокаде, надпочечниковой недостаточности, ХПН, сопутствующей терапии калийсберегающими диуретиками, а также при метаболических нарушениях (ацидоз, гиповолемия с гипонатриемией).
Взаимодействие
Препараты калия, СГ и другие ААП оказывают синергическое действие на а-в проводимость и возбудимость сердца.
Так как блокада натриевых каналов влияет на распространение потенциалов действия во всем организме, то неудивительно, что местные анестетики способны давать системные токсические эффекты. Помимо побочных эффектов, характерных для всех местных анестетиков, существуют еще и индивидуальные, свойственные только отдельным препаратам.
Токсичность местного анестетика часто прямо пропорциональна его мощности. Безопасные максимальные дозы анестетиков указаны в табл. 14-1. Сочетание местных анестетиков оказывает аддитивное действие: например, раствор, содержащий половину токсической дозы лидокаина и половину токсической дозы бупивакаина, вызывает полноценный стопроцентный токсический эффект.
А. Сердечно-сосудистая система. Местные анестетики угнетают автоматизм сердца, увеличивая длительность спонтанной деполяризации (спонтанная деполяризация - это IV фаза потенциала действия в клетках водителей ритма), уменьшают продолжительность рефрактерного периода. Высокие дозы анестетиков угнетают также сократимость и проводимость. Действие местных анестетиков на сердце обусловлено как прямым влиянием на мембрану кардиомиоцитов (т. е. блокадой натриевых каналов), так и опосредованными механизмами (подавление активности вегетативной нервной системы). Расслабление гладких мышц вызывает умеренную артериолодилатацию. Возникающее сочетание брадикардии, блокады сердца и артериальной гипотонии может привести к остановке сердца. Аритмии и депрессия кровообращения - это распространенные симптомы при передозировке местных анестетиков.
Низкие дозы лидокаина позволяют эффективно устранить некоторые виды желудочковых аритмий. Стандартные дозы лидокаина для в/в введения практически не вызывают депрессии миокарда и артериальной гипотонии. Лидокаин, введенный в дозе 1,5 мг/кг в/в за 1-3 мин до ларингоскопии и интубации трахеи, ослабляет обусловленный этой манипуляцией подъем артериального давления.
При случайном введении бупивакаина в просвет кровеносного сосуда возникают тяжелые токсические эффекты: артериальная гипотония, АВ-блока-да и желудочковые аритмии (например, фибрилля-ция желудочков). Факторы риска - беременность, гипоксемия и респираторный ацидоз. Электрофизиологические исследования показали, что бупивакаин угнетает деполяризацию намного сильнее, чем лидокаин. Бупивакаин блокирует натриевые каналы в мембранах клеток сердца и влияет на функцию митохондрий; высокая степень связывания с белками значительно затрудняет и удлиняет лечение.
Ропивакаин, относительно новый местный ане-стетик амидного типа, имеет сходные с бупивакаи-ном физико-химические характеристики за исключением того, что растворяется в жирах в 2 раза хуже. Мощность, начало и продолжительность действия идентичны для обоих анестетиков (хотя вызванная ропивакаином моторная блокада немного слабее). Терапевтический индекс ропивака-ина шире, риск тяжелых аритмий на 70 % ниже по сравнению с бупивакаином. Ропивакаин менее токсичен, потому что он хуже растворяется в жирах, а также представляет собой стереоизомер (бу-пивакаин - рацемическая смесь стереоизомеров).
Влияние кокаина на сердце не похоже на эффекты остальных местных анестетиков (в России кокаин запрещен к применению в медицинской практике.- Примеч. пер.). В норме терминали ад-ренергических нервов повторно поглощают норад-реналин из синаптической щели после высвобождения (так называемый обратный захват). Кокаин угнетает обратный захват норадреналина, потенцируя эффекты симпатической нервной системы. Кокаин может вызвать артериальную гипертензию и эктопические желудочковые ритмы. Аритмоген-ный потенциал делает кокаин противопоказанным при анестезии галотаном. Вызванные кокаином аритмии следует лечить адреноблокаторами и антагонистами кальция. При орошении кокаин вызывает вазоконстрикцию сосудов кожи или слизистых оболочек.
Б. Система дыхания. Лидокаин угнетает ги-поксический драйв (т. е. увеличение вентиляции при снижении PaO 2).
К апноэ может привести блокада диафрагмального или межреберных нервов, а также прямое угнетающее влияние местных анестетиков на дыхательный центр в продолговатом мозге (например, после ретробульбарного введения). Местные анестетики расслабляют гладкие мышцы бронхов. Лидокаин (1,5 мг/кг в/в) устраняет рефлекторный бронхоспазм, возникающий в ряде случаев при интубации.В. Центральная нервная система. Центральная нервная система особенно чувствительна к токсическим эффектам местных анестетиков. У бодрствующих больных неврологические симптомы часто служат первыми признаками передозировки местных анестетиков. Ранние неврологические симптомы включают онемение вокруг рта, парестезии языка и головокружение. Сенсорные расстройства проявляются шумом в ушах и неясностью зрения. Возбуждение ЦНС (например, беспокойство, возбуждение, нервозность, паранойя) часто сменяется депрессией (например, спутанная речь, головокружение, утрата сознания). Мышечные подергивания свидетельствуют о начале тонико-клонических судорог. Часто наступает остановка дыхания. Возбуждение ЦНС обусловлено избирательным торможением ингибиторных влияний. Бензодиазепины и гипервентиляция уменьшают мозговой кровоток, что снижает количество препарата, вступающего в контакт с клетками головного мозга, и, следовательно, повышает порог развития судорог, обусловленных токсическим действием местных анестетиков. Тиопентал (1-2 мг/кг в/в) быстро и эффективно
устраняет эти судороги. Необходимо обеспечить полноценную вентиляцию и оксигенацию.
Лидокаин (1,5 мг/кг в/в) уменьшает мозговой кровоток, а также ослабляет подъем внутричерепного давления при интубации трахеи у больных с внутричерепной гипертензией. Инфузию лидокаина или прилокаина применяют для потенцирования общей анестезии, потому что эти местные анестетики снижают МАК ингаляционных анестетиков на 40 %.
Кокаин стимулирует ЦНС и вызывает чувство эйфории.
Передозировка кокаина проявляется беспокойством, рвотой, тремором, судорогами и дыхательной недостаточностью. Как правило, местные анестетики вызывают преходящую, кратковременную блокаду нейро-нальной функции. Тем не менее непреднамеренное введение большого количества хлорпрокаина в субарахноидальное пространство (вместо эпиду-рального) вызывает устойчивый неврологический дефект. Нейротоксичность обусловлена низким рН раствора хлорпрокаина, а также прямым действием содержащегося в нем стабилизатора - бисульфата натрия (в настоящее время новые препараты хлопрокаина вместо бисульфата натрия содержат другой стабилизатор - этилендиамин-тетраацетат, ЭДТА). При эпидуральном введении хлорпрокаин иногда вызывает сильную боль в спине, особенно при использовании больших количеств (> 40 мл) и при дополнительной инфильтрации анестетиком подкожной клетчатки. Считают, что боль обусловлена низким рН раствора и специфическим действием ЭДТА. Введение повторных доз 5 % раствора лидокаина и 0,5 % раствора тетра-каина при длительной спинномозговой анестезии, осуществляемой через катетер малого диаметра, может вызвать синдром конского хвоста. Депонирование анестетиков вокруг структур конского хвоста постепенно приводит к нарастанию их концентрации до токсической, что и вызывает стойкое неврологическое повреждение.Г. Иммунная система. Истинные реакции гиперчувствительности к местным анестетикам (в отличие от системной токсичности при передозировке) представляют собой редкое явление. Местные анестетики эфирного типа, будучи производными парааминобензойной кислоты - известного аллергена, вызывают аллергию чаще, чем амидные анестетики. Некоторые амидные анестетики выпускаются в многодозных флаконах, содержащих стабилизатор метилпарабен - вещество, по структуре напоминающее парааминобензойную кислоту. Редкие аллергические реакции к амидным анестетикам в подавляющем большинстве случаев обусловлены именно метилпарабеном. Симптомы и лечение лекарственной аллергии описаны в гл. 47.
Д. Скелетные мышцы. В/м введение местных анестетиков (например, при инъекции в триггер-ные точки) дает миотоксический эффект (бупива-кин > лидокаин > прокаин). Гистологически повреждение выглядит как чрезмерное сокращение миофибрилл, сменяющееся литической дегенерацией, отеком и некрозом. Регенерация занимает 3-4 нед. Одновременное введение стероидов или адреналина утяжеляет течение мионекроза.
(два занятия)
Занятие 1-е
ПРИРОДА ВОЗБУЖДЕНИЯ
1. Что называют раздражимостью и возбудимостью?
Раздражимость – свойство живой материи активно изменять характер своей жизнедеятельности при действии раздражителя. Возбудимость – свойство некоторых тканей генерировать потенциал действия.
2. Каково соотношение понятий “возбудимость” и “раздражимость”? Какие ткани в физиологии называют возбудимыми, какие – невозбудимыми?
Возбудимость – это частный случай раздражимости. Возбудимыми называют ткани, клетки которых способны генерировать потенциал действия, а невозбудимыми – клетки которых не способны к генерации потенциала действия.
3. Клетки каких тканей организма являются возбудимыми, каких – невозбудимыми?
Возбудимыми – нервной и мышечной, невозбудимыми – эпителиальной и соединительной тканей.
4. Дайте определение понятию "раздражитель".
Раздражитель – это изменение внешней или внутренней среды организма, воспринимаемое клетками и вызывающее ответную реакцию.
5. Назовите два вида основных раздражителей и их разновидности.
Физические (электрические, механические, температурные, световые) и химические (различные соединения и газы).
6. Перечислите основные особенности электрического раздражителя.
Универсальность, простота дозировки по силе, длительности, крутизне нарастания и частоте стимулов, простота включения и выключения.
7. Опишите второй опыт Гальвани, доказывающий наличие “животного электричества”.
Готовят препарат задней лапки лягушки с седалищным нервом, набрасывают седалищный нерв лягушки на мышцу бедра так, чтобы он одновременно касался поврежденного и неповрежденного участков мышцы, и наблюдают сокращение мышц конечности.
8. Опишите опыт вторичного тетануса Маттеуччи.
Готовят два нервно-мышечных препарата лягушки, накладывают нерв второго препарата на мышцу первого; ритмичное раздражение нерва первого препарата вызывает тетаническое сокращение обеих мышц.
9. Назовите непосредственную причину наличия потенциала покоя, следствием чего она является?
Неодинаковая концентрация анионов и катионов по обе стороны клеточной мембраны, что является следствием различной проницаемости мембраны для разных ионов и активного транспорта ионов с помощью ионных помп.
10. Что называют мембранным потенциалом (потенциалом покоя)? Какова его величина?
Разность электрических потенциалов между внутренней и наружной сторонами клеточной мембраны. Равен 50 90 мВ.
11. Нарисуйте схему (график) мембранного потенциала покоя возбудимой клетки.
–момент внедрения электрода в клетку.
12. Где преимущественно находятся (в межклеточной жидкости или в цитоплазме) ионы натрия, калия и хлора? Положительно или отрицательно заряжены внутренняя и наружная среды клетки относительно друг друга?
Ионы натрия и хлора – в межклеточной жидкости, ионы калия – внутриклеточно. Внутренняя отрицательно, наружная – положительно.
3. Перечислите основные анионы, находящиеся в клетке и играющие важную роль в происхождении потенциала покоя. Какова причина подобного распределения этих ионов?
Глютамат, аспартат, органический фосфат, сульфат. Клеточная мембрана непроницаема для них.
14.В клетку или из клетки перемещаются ионы калия и натрия в покое? Почему при этом не нарушается их концентрационный градиент?
Ионы калия выходят из клетки, ионы натрия входят в клетку. Потому что постоянно работает натрий-калиевая помпа и переносит такое же число ионов натрия и калия обратно, поддерживая их концентрационный градиент.
15. Каким образом можно экспериментально доказать существование активного транспорта натрия?
Путем введения в клетку радиоактивного изотопа натрия и его появления во внеклеточной среде (выведение вопреки концентрационному градиенту). Блокирование процесса синтеза АТФ исключает выведение натрия.
16. Что понимают под проницаемостью клеточной мембраны? От чего она зависит?
Свойство мембраны пропускать воду, заряженные и незаряженные частицы согласно законам диффузии и фильтрации. Зависит от наличия различных каналов и их состояния ("ворота" открыты или закрыты), от растворимости частиц в мембране, от размеров частиц и каналов.
17. Что понимают под ионной проводимостью через клеточную мембрану? От чего она зависит?
Способность ионов проходить через клеточную мембрану. Зависит от проницаемости клеточной мембраны и от концентрационного и электрического градиентов ионов.
18. Проницаемость клеточной мембраны для калия или для натрия в состоянии покоя больше? Какой ион и почему преимущественно создает потенциал покоя?
Проницаемость для ионов калия больше, чем для ионов натрия. Ион калия, т.к. он выходит из клетки в большем количестве, чем входит Na + в клетку, а отрицательные крупномолекулярные анионы из клетки не выходят вообще.
19. Какова роль различных ионов и поверхностных зарядов клеточной мембраны в формировании потенциала покоя?
Потенциал покоя – алгебраическая сумма электрических зарядов, создаваемых всеми ионами, находящимися в клетке и вне клетки, а также поверхностных зарядов самой мембраны.
20. Какой опыт доказывает основную роль ионов калия в обеспечении существования потенциала покоя? Опишите его сущность.
Опыт с перфузией гигантского аксона кальмара солевыми растворами. При уменьшении концентрации калия в перфузате потенциал покоя уменьшается, при увеличении концентрации калия потенциал покоя увеличивается.
21. Напишите уравнение Нернста, по которому можно рассчитать величину равновесного потенциала для отдельных ионов.
E = RT/ zF ln Co / Ci, где Со и Ci – внешняя и внутренняя концентрация ионов соответственно; R – универсальная газовая постоянная; T – абсолютная температура; F – постоянная Фарадея; z – заряд иона.
22. Что такое калиевый равновесный потенциал?
Величина мембранного потенциала, при которой перемещения ионов калия в клетку и из клетки равны в количественном отношении.
23. Назовите виды ионного транспорта через клеточную мембрану. Поясните их сущность.
Активный транспорт (с затратой энергии АТФ) с помощью белков-переносчиков и пассивный транспорт (без непосредственной затраты энергии АТФ) согласно законам диффузии.
24. Что является источником энергии для работы ионных насосов? За счет каких трех путей этот источник энергии восстанавливается?
Аденозинтрифосфорная кислота (АТФ). Первый путь – расщепление креатинфосфата, второй – анаэробный гликолиз, третий – аэробное окисление.
25. Опишите структурно-функциональную организацию ионного потенциалзависимого канала.
Канал образован белковыми молекулами, которые пронизывают всю толщу мембраны; он имеет "ворота", представляющие собой белковые молекулы, способные менять свою конформацию под влиянием электрического поля ("ворота" открыты или закрыты).
26. Как экспериментально доказать роль отдельных ионных каналов в формировании ПП и развитии ПД?
Путем применения специфических блокаторов ионных каналов для предотвращения пассивного движения соответствующих ионов в клетку или из клетки, о чем судят по изменению величины трансмембранного потенциала.
27. Приведите основные классификации ионных каналов.
1) По возможности управления их функцией- управляемые и неуправляемые (каналы “утечки” ионов); 2) в зависимости от управляющего стимула - потенциало-, хемо- и механочувствительные; 3) в зависимости от проницаемости каналов для разных ионов - ионоселективные и не обладающие селективностью.
28. Перечислите основные разновидности ионоселективных каналов для K + , Na + , Са 2+ .
Для калия – медленные управляемые и неуправляемые, быстрые потенциалчувствительные. Для натрия – медленные неуправляемые и быстрые потенциалчувствительные. Для кальция – медленные и быстрые потенциалчувствительные.
29. Укажите функциональные различия управляемых и неуправляемых каналов для ионов Na + и К + в нервных клетках и в клетках скелетных мышц.
Через управляемые каналы ионы проходят очень быстро только, когда открыты их "ворота", через неуправляемые – постоянно и медленно (каналы утечки ионов).
30. Назовите специфические блокаторы натриевых и калиевых управляемых каналов.
Тетродотоксин (ТТХ) – для натриевых каналов, тетраэтиламмоний (ТЭА) – для калиевых.
31. Как и почему изменится величина потенциала покоя, если проницаемость клеточной мембраны станет одинаково высокой для всех ионов, а натриево-калиевая помпа будет продолжать работать?
Потенциал покоя значительно уменьшится вследствие выравнивания концентрации различных ионов вне- и внутри клетки и будет соответствовать уровню, создаваемому только Na/К насосом – 5 – 10 мВ.
32. Что называют потенциалом действия? (Отразите причину его возникновения).
Электрический процесс, выражающийся в быстром колебании мембранного потенциала вследствие перемещения ионов в клетку и из клетки, способный распространяться без декремента (без затухания).
33. Нарисуйте схему (график) потенциала действия скелетного мышечного волокна, обозначьте его фазы, назовите их.

а – фаза деполяризации; б – фаза инверсии; в – фаза реполяризации.
34. Какое свойство клеточной мембраны обеспечивает возникновение потенциала действия, за счет какого механизма оно реализуется?
Способность изменять проницаемость для ионов при действии раздражителя. Реализуется за счет активации и инактивации ионных каналов.
35. Укажите примерные значения длительности и амплитуды потенциалов действия нервного волокна и волокна скелетной мышцы.
У нервного волокна – 1 мс, у мышечного – до 10 мс с учетом замедления реполяризации в конце ее. Амплитуды примерно равны 100 – 130 мВ.
36.Назовите фазы потенциала действия, дайте соответствующие пояснения.
Фаза деполяризации – уменьшение заряда до нуля; инверсии (овершут) – изменение знака заряда на обратный; реполяризации – восстановление исходного заряда.
37.Что такое следовые потенциалы? Какие виды следовых потенциалов Вам известны?
Медленное изменение мембранного потенциала после фазы реполяризации. Гиперполяризационный (положительный) и деполяризационный (отрицательный) следовые потенциалы.
38.С помощью каких методических приемов изучают ионные токи через мембрану?
Методом фиксации потенциала и блокады ионных каналов.
39.Как изменяется ионная проводимость для Na + и К + при возбуждении клетки (развитии потенциала действия)? Каково соотношение во времени этих изменений?
Сначала повышается для ионов Na + и очень быстро возвращается к норме; потом более медленно повышается для К + и также медленно возвращается к норме.
40.Что такое критический уровень деполяризации клеточной мембраны (КУД)?
Минимальный уровень деполяризации мембраны, при котором возникает потенциал действия.
41.Опишите опыт, доказывающий, что для возникновения потенциала действия необходимы ионы натрия.
Аксон помещают в среды с различной концентрацией натрия. При уменьшении концентрации натрия потенциал действия уменьшается.
42.Что называют активацией и инактивацией ионных каналов?
Повышение проницаемости мембраны клетки для ионов (открытие "ворот") называют активацией, ее снижение (закрытие “ворот”) – инактивацией.
43.Движение какого иона и в каком направлении через клеточную мембрану обеспечивает фазу деполяризации потенциала действия в нервных клетках и клетках исчерченных мышц? Затрачивается ли при этом энергия АТФ?
44.Что является условием и движущей силой для входа натрия в клетку в фазу деполяризации потенциала действия?
Условие – увеличение проницаемости клеточной мембраны для Na + ; движущая сила – концентрационный и электрический градиенты для Na + .
45.Движение какого иона и в каком направлении через клеточную мембрану обеспечивает фазу инверсии потенциала действия? Затрачивается ли при этом энергия АТФ?
Движение ионов натрия внутрь клетки. Энергия АТФ не затрачивается.
46.Что является условием и движущей силой для входа натрия в клетку в фазу инверсии потенциала действия?
Условием – повышенная проницаемость клеточной мембраны для натрия; движущей силой – концентрационный градиент для Na + .
47.Какое влияние и в какие фазы потенциала действия оказывает концентрационный градиент на вход натрия внутрь клетки?
Обеспечивает вход натрия в клетку в фазу деполяризации и восходящей части инверсии.
48.В какие фазы потенциала действия электрический градиент способствует или препятствует входу натрия внутрь клетки?
В фазу деполяризации способствует, а в фазу инверсии – препятствует.
49.Движение какого иона и в каком направлении через мембрану клетки обеспечивает нисходящую часть потенциала действия? Затрачивается ли при этом энергия АТФ?
Движение ионов калия из клетки. Энергия АТФ не затрачивается.
50.Укажите условие и движущую силу, обеспечивающие выход ионов калия из клетки во время ее возбуждения.
Условие – увеличение проницаемости клеточной мембраны для ионов калия; движущая сила – концентрационный и частично электрический градиенты.
51.Что является движущей силой, обеспечивающей выход ионов калия из клетки в нисходящую фазу инверсии потенциала действия?
Концентрационный и электрический градиенты.
52.Какое влияние на выход ионов калия из клетки оказывают концентрационный и электрический градиенты К + в фазу реполяризации потенциала действия, т.е. после фазы инверсии?
Концентрационный градиент обеспечивает выход калия из клетки, электрический – препятствует.
53.В какие фазы потенциала действия концентрационный и электрический градиенты обеспечивают выход ионов калия из клетки или препятствуют ему?
Концентрационный градиент обеспечивает выход К + в фазу инверсии и реполяризации, электрический – в фазу инверсии способствует, а в фазу реполяризации препятствует.
54.Каковы причины замедления фазы деполяризации в конечной ее части и следовой гиперполяризации?
Уменьшение проницаемости клеточной мембраны для калия в конце фазы реполяризации. Все еще повышенная проницаемость для калия по сравнению с исходным уровнем.
55.Опишите устройство микроэлектрода.
Микроэлектрод – это микропипетка из стекла с диаметром кончика около 0,5 мкм, заполненная 3М раствором КСl с погруженной в него хлорированной серебряной проволокой.
56.С какой целью применяют монополярные электроды при исследовании электрических явлений в клетке? Каковы соотношения размеров активного и индифферентного электродов при монополярном способе регистрации и стимуляции?
Применяют для регистрации потенциала покоя и потенциала действия (монофазного). В обоих случаях активный электрод значительно (в 10 – 100 раз) меньше, чем индифферентный электрод.
57.Охарактеризуйте электроды при биполярном способе регистрации и стимуляции. С какой целью применяется биполярный способ регистрации потенциалов?
В обоих случаях используются два активных электрода одинакового размера. Применяют для регистрации процессов распространения возбуждения.
58.Перечислите свойства локального потенциала. Как изменяется возбудимость ткани при его возникновении?
Не распространяется, способен к суммации, величина определяется силой подпорогового раздражителя. Возбудимость повышается.
59.Перечислите свойства распространяющегося возбуждения. Какие раздражения (по силе) вызывают локальный потенциал и потенциал действия?
Распространяется, не суммируется, величина не зависит от силы раздражителя. Локальный потенциал возникает при действии подпороговых раздражителей, потенциал действия – при действии пороговых или сверхпороговых раздражителей.
60.Как изменяется фаза нарастания потенциала действия и его амплитуда при действии различной концентрации блокаторов натриевых каналов?
С увеличением концентрации блокаторов снижается крутизна нарастания и амплитуда потенциала действия, вплоть до полного его отсутствия.
18.1. Класс I - блокаторы натриевых каналов
Прежнее название этой группы препаратов - мембраностабилизирующие средства. В настоящее время блокаторы натриевых каналов принято разделять на 3 подкласса: IA, IB и IC Между ними существует ряд различий в механизме действия, применении и влиянии на параметры сердца.
Класс1А
К этому классу противоаритмических препаратов относят хинидин и хинидиноподобные средства (прокаинамид и дизопирамид).
Эти ЛВ блокируют натриевые и калиевые каналы и тем самым пролонгируют фазы 0, 3 и 4 потенциала действия (рис. 18-6). Это приводит к снижению автоматизма, проводимости и увеличению ЭРП. Хинидиноподобные средства действуют на все отделы сердца, поэтому они эффективны как при желудочковых, так и при суправентрикулярных экстрасистолиях и тахиаритмиях.
Общие побочные эффекты этой группы препаратов:
Снижение сократимости миокарда;
Снижение атриовентрикулярной проводимости;
Снижение АД;
Ваголитическое и проаритмическое (аритмогенное) действие. Последнее обусловлено несколькими причинами.
Пролонгирование потенциала действия повышает риск появления ранней последеполяризации, которая в свою очередь приводит к возникновению аритмии torsades de pointes (русские названия: «пируэт» «скручивание пиков», «пробежка», «танец на пуантах», «веретено»).
Рис. 18-6. Влияние хинидина на потенциал действия волокна Пуркинье
Ваголитическое действие хинидиноподобных средств повышает уровень автоматизма синусового узла, тем самым облегчая проведение импульсов через атриовентрикулярное соединение и усиливая аритмию желудочков.
Угнетение проводимости при reentry-аритмиях может привести к циркуляции возбуждения по более коротким траекториям, что в свою очередь способствует учащению повторного входа и усилению аритмии.
Хинидин (Хинипэк*, Кинидин Дурулес*) - алкалоид коры хинного дерева (правовращающий изомер хинина). В медицинской практике препарат используют в виде хинидина сульфата. Он хорошо всасывается из ЖКТ, что обусловливает его применение внутрь. Биодоступность в среднем составляет 70-80%. Максимальная концентрация препарата в крови достигается через 2-3 ч, а связывание с белками плазмы происходит на 60-80%. Метаболизируется хинидин в печени, выводится почками (около 20% в неизмененном виде); период полуэлиминации составляет 6-7 ч. Почечная экскреция препарата увеличивается при изменении реакции мочи в кислую сторону.
Снижает автоматизм, проводимость и увеличивает ЭРП кардиомиоцитов желудочков;
Подавляет автоматизм водителей ритма (в большей степени атриовентрикулярного и в меньшей - синусового узла);
Умеренно снижает скорость проведения возбуждения по атриовентрикулярному узлу и сократимость миокарда (в терапевтических дозах);
Оказывает ваголитическое (антихолинергическое) действие, угнетая передачу возбуждения с блуждающего нерва на сердце, и таким образом вызывая повышение уровня автоматизма синоатриального узла и умеренную тахикардию;
Расширяет периферические сосуды (блокирует α-адренорецепторы), тем самым вызывая умеренное снижение АД.
Хинидин эффективен при желудочковых и наджелудочковых нарушениях сердечного ритма. Его назначают при постоянной и пароксизмальной формах мерцательной аритмии предсердий, пароксизмальной тахикардии, экстрасистолии.
Побочные эффекты хинидина:
Снижение сократимости миокарда, артериальная гипотензия, атриовентрикулярный блок;
Тошнота, рвота, диарея;
Головокружение, звон в ушах, нарушения слуха, зрения;
Тромбоцитопения.
В 5% случаев хинидин оказывает аритмогенное действие, приводя к возникновению желудочковых нарушений ритма типа «пируэт».
Прокаинамид (новокаинамид*) воздействует на электрофизиологические механизмы работы сердца аналогично хинидину. В отличие от последнего он меньше снижает сократимость миокарда, обладает менее выраженными антихолинергическими свойствами и не блокирует α-адренорецепторы, однако обладает умеренным ганглиоблокирующим действием. Так же, как хинидин, прокаинамид применяют при желудочковых и наджелудочковых тахиаритмиях и экстрасистолии.
Препарат назначают не только внутрь, но и внутривенно (при необходимости быстрого достижения эффекта). При применении внутрь прокаинамид всасывается быстрее, чем хинидин. Биодоступность составляет 75-95%. Препарат незначительно связывается с белками плазмы крови (15-20%). Метаболизируется в печени с образованием активного метаболита - N-ацетилпрокаинамида. По скорости метаболизма среди пациентов выделяют медленных и быстрых «ацетиляторов», существенно различающихся по продолжительности действия препарата. Прокаинамид выводится почками в неизмененном виде и в виде метаболитов. Активный метаболит экскретируется медленнее, чем сам препарат, и при нарушении функции почек может кумулировать в организме.
Побочные эффекты:
Снижение АД (вследствие ганглиоблокирующего действия), нарушение проводимости;
Тошнота, рвота, диарея;
Судороги;
Аллергические реакции в виде лихорадки, болей в суставах и мышцах, кожной сыпи, реже в виде агранулоцитоза или синдрома, подобного системной красной волчанке;
Нервно-психические расстройства (редко).

Дизопирамид (ритмодан*, ритмилен*) - аналог хинидина, обладает выраженными антиаритмическими свойствами. Показания к применению те же. Препарат снижает сократимость миокарда, а так же обладает сильным М-холиноблокирующим действием. Хорошая всасываемость из кишечника (биодоступность 80%) позволяет применять препарат внутрь. Вещество связывается с белками плазмы крови, метаболизируется в печени. Выводится в основном почками (период полуэлиминации 6-8 ч).
Побочные эффекты:
Значительное снижение сократимости миокарда, атриовентрикулярный блок, аритмогенное действие;
Сухость во рту, паралич аккомодации, обстипация (запор), задержка мочеиспускания (в связи с выраженной М-холиноблокирующей активностью).
Класс IB
Препараты этого класса имеют ряд существенных отличий.
Это селективные блокаторы натриевых каналов, пролонгирующие только фазы 0 и 4. Они угнетают проводимость и автоматизм волокон Пуркинье и сократительных кардиомиоцитов. Препараты класса IB блокируют натриевые каналы в инактивированном
состоянии и имеют скорость ассоциации/диссоциации менее 1 сек, что не превышает продолжительности нормального потенциала действия. Таким образом, не урежая сердечного ритма, они препятствуют генерации и проведению внеочередных импульсов.
Препараты класса IB не блокируют калиевые каналы и не пролонгируют реполяризацию. Напротив, при их применении отмечено некоторое укорочение фазы 3 и ЭРП.
Препараты класса IB не изменяют ток кальция (ни прямо, ни опосредованно). Поэтому они воздействуют только на желудочки, не влияя на водители ритма, и не снижают сократимость миокарда. Это обусловливает применение данных препаратов только при желудочковых экстрасистолиях.
Лидокаин (ксикаин*, ксилокаин*), блокируя натриевые каналы клеточных мембран, обладает местноанестезирующим и противо- аритмическим действием. Он уменьшает проводимость и автоматизм волокон Пуркинье и рабочих кардиомиоцитов, подавляя эктопические очаги в желудочках. Его считают препаратом выбора при желудочковых аритмиях, возникающих после инфаркта миокарда. Это обусловлено тем, что, оказывая противоаритмическое действие, лидокаин не влияет на сократимость, которая в этом случае обычно снижена.
Препарат вводят внутривенно капельно, так как при пероральном применении он обладает низкой биодоступностью. На 50-80% лидо- каин связывается с белками плазмы крови, метаболизируется в основном в печени. Период полураспада мал - около 2 ч. При патологии печени скорость метаболизма лидокаина снижается.
Препарат легко переносится, но возможны побочные эффекты:
Нарушения со стороны ЦНС (сонливость, спутанность сознания, судорожные реакции);
Артериальная гипотензия, снижение атриовентрикулярной проводимости.
Мексилетин - структурный аналог лидокаина, эффективный при приеме внутрь (биодоступность 90-100%). Действует длительно (период полуэлиминации 12-16 ч). Возможно и внутривенное введение препарата. Применяют при желудочковых аритмиях.
Побочные эффекты:
Брадикардия, артериальная гипотензия, нарушение атриовентрикулярной проводимости, аритмии;
Тошнота, рвота;
Неврологические нарушения.

Фенитоин (дифенин *) первоначально применяли в качестве противоэпилептического средства. Позже у него было обнаружено антиаритмическое действие. Фенитоин считают препаратом выбора при желудочковых аритмиях, вызванных сердечными гликозидами. Это связано с тем, что оказывая антиаритмическое действие, он не уменьшает положительный инотропный эффект данных кардиотонических средств.
Фенитоин медленно всасывается из ЖКТ, в крови связывается с белками плазмы на 80-96%. Метаболизируется в печени, метаболиты выводятся в основном почками. В связи с замедленной экскрецией из организма (период полуэлиминации составляет 24-30 ч) возможна кумуляция препарата.
Из побочных эффектов отмечают атаксию, нистагм, диплопию, гиперпластический гингивит (гиперплазию десен).
Класс IС
Как и препараты класса IA, эти вещества действуют и на желудочки и на водители ритма. Однако применяют их только при вентрикулярных аритмиях, угрожающих жизни и резистентных (устойчивых) к другим противоаритмическим средствам. Такая специфическая ниша препаратов класса IC обусловлена их выраженной проаритмической активностью. Кроме того отдельные представители этой группы могут сильно угнетать сократимость и атриовентрикулярную проводимость.
П р о п а ф е н о н - типичный представитель этого класса веществ. Блокирует натриевые и в некоторой степени кальциевые каналы, а также обладает небольшой β-адреноблокирующей активностью. Препарат применяют при желудочковых аритмиях в случае неэффективности других антиаритмических средств. Вводят внутрь и внутривенно. При пероральном применении хорошо всасывается из кишечника, однако интенсивно метаболизируется при первом прохождении через печень (биодоступность варьирует от 4 до 40%).
По метаболизму пропафенона в зависимомти от генетических особенностей выделяют 2 группы пациентов:
Быстро метаболизирующих препарат (более 90%);
Медленно метаболизирующих препарат (около 10%).
В результате образуются 2 фармакологически активных вещества. Побочные эффекты:
Тошнота, рвота, запор, сухость во рту;
Нарушение сна;
Брадикардия;
Бронхоспазм;
Выраженное аритмогенное действие.
Флекаинид* выраженно угнетает проводимость в атриовентрикулярном узле, пучке Гиса и волокнах Пуркинье, незначительно снижает уровень автоматизма синусного узла, практически не увеличивает ЭРП в желудочках и мало влияет на сократимость миокарда. Препарат применяют в виде флекаинида ацетата при вентрикулярных аритмиях в случае неэффективности других антиаритмических средств. Вводят внутрь, иногда внутривенно. При применении внутрь максимальную концентрацию в плазме отмечают через 3-4 ч после приема. Флекаинид практически не изменяется при первом прохождении через печень. 75-85% препарата связываются с белками плазмы.
Побочные эффекты:
Проаритмическое действе (отмечают в 5-15% случаев);
Тошнота, головная боль, головокружение;
Нарушение зрения.
Морацизин (этмозин*) - производное фенотиазина, препарат смешанного типа действия, обладает свойствами блокаторов натриевых каналов всех трех классов: IC, IB, IA. Он угнетает проводимость в атри- овентрикулярном узле, пучке Гиса и волокнах Пуркинье, мало влияет на автоматизм синусового узла и сократимость миокарда. Морацизин эффективен при желудочковых и наджелудочковых нарушениях ритма. Однако из-за выраженного аритмогенного действия его применяют только при вентрикулярных аритмиях, рефрактерных к другим ЛС. Вводят внутрь (биодоступность составляет около 40%) и внутривенно. На 95% связывается с белками плазмы, период полуэлиминации - 2 ч.
Побочные эффекты:
Проаритмическое действие;
Головная боль;
Повышенная утомляемость и слабость;
Диарея и др.

Этацизин * близок по химическому строению к морацизину. Он блокирует не только натриевые, но и кальциевые каналы. Применяют аналогично морацизину, назначают внутрь и внутривенно. Побочные эффекты более выражены и проявляются чаще (в особенности при внутривенном введении).