Хроническое легочное сердце пропедевтика. Легочное сердце патогенез
1. АКТУАЛЬНОСТЬ ТЕМЫ
Хроническое легочное сердце (ХЛС) - клинико-функциональный симптомокомплекс, развивающийся на фоне различных бронхолегочных заболеваний, приводящих в конечном итоге к развитию легочной гипертензии.
Фактически развитие ХЛС знаменует собой «смену статуса легочного больного на сердечного» и требует соответственно смещения акцентов при ведении больного.
Эффективность лечения ХЛС во многом зависит от своевременной постановки диагноза. Однако диагностика легочного сердца на ранних этапах, когда данное состояние сохраняет потенциальную обратимость, - весьма трудная проблема. В то же время лечение больных с хроническим декомпенсированным легочным сердцем представляет собой сложную, порой малоперспективную задачу. В связи с этим важное практическое значение приобретает умение своевременно заподозрить и диагностировать ХЛС с учетом его основных этиологических факторов.
2. ЦЕЛЬ ЗАНЯТИЯ
Уметь диагностировать ХЛС и составлять программу ведения больных ХЛС на основании знания основных звеньев патогенеза, клинических проявлений, лабораторно-инструментальных признаков, наиболее информативных методов диагностики, принципов лечения больных ХЛС.
3. ВОПРОСЫ ДЛЯ ПОДГОТОВКИ К ЗАНЯТИЮ
1. Понятие «хроническое легочное сердце», определение.
2. Патогенез ХЛС.
3. Классификация ХЛС.
4. Клинические симптомы ХЛС.
5. Диагностические критерии ХЛС.
6. Принципы лечения больных с ХЛС.
7. Прогноз.
4. ТЕСТОВЫЕ ЗАДАНИЯ ИСХОДНОГО УРОВНЯ
1. Назовите основные механизмы развития легочной гипертонии
при ХОБЛ:
A. Альвеолярная гипоксия.
Б. Альвеолярная гиперкапния.
B. Редукция капиллярного ложа вследствие деструкции альвеол. Г. Наличие артерио-венозных анастомозов в легких.
Д. Замедление кровотока в малом круге кровообращения.
2. Какие клинические признаки могут свидетельствовать о развитии у больного ХОБЛ ХЛС?
A. Цианоз.
Б. Одышка, усиливающаяся при физической нагрузке.
B. Бронхиальная обструкция. Г. Эпигастральная пульсация. Д. Сонливость.
3. Назовите симптомы правожелудочковой недостаточности:
А. Тахикардия при физической нагрузке, сохраняющаяся более 10 мин после прекращения нагрузки.
Б. Гепатоюгулярный рефлюкс (симптом Плеша). В. Асцит.
Г. Увеличение селезенки. Д. Увеличение печени.
4. В анализе крови у больных с ХЛС обнаруживают:
A. Повышение острофазовых воспалительных маркеров. Б. Снижение СОЭ.
B. Эритроцитоз.
Г. Гипопротеинемию.
Д. Гиперхолестеринемию.
5. Аускультативная картина ХЛС включает:
A. Систолический шум над мечевидным отростком. Б. Акцент II тона над легочной артерией.
B. Систолический шум на верхушке.
Г. Усиление I тона в проекции трехстворчатого клапана. Д. Все вышеуказанные аускультативные признаки.
6. ЭКГ-признаки гипертрофии правого желудочка:
A. Появление высокого остроконечного зубца Ρ
Б. Высокий зубец R в V1, V2; глубокий зубец S в левых грудных отведениях.
B. Полная или неполная блокада правой ножки пучка Гиса. Г. Отклонение электрической оси сердца вправо.
7. Гипертрофия правого желудочка развивается при следующих заболеваниях:
A. Стеноз левого атриовентрикулярного отверстия. Б. Стеноз клапанов легочной артерии.
B. Недостаточность аортальных клапанов. Г. Субаортальный стеноз.
Д. Дефект межпредсердной перегородки.
8. При развитии правожелудочковой недостаточности у больных с хроническим легочным сердцем патогенетически оправдано назначение:
A. Нитратов.
Б. Высоких доз антагонистов кальция.
B. Ингибиторов АПФ.
Г. Антагонистов альдостерона. Д. Сердечных гликозидов.
9. Объективные клинические признаки гипертрофии правого желудочка:
A. Разлитой сердечный толчок.
Б. Систолическая прекардиальная и эпигастральная пульсация.
B. Расширение границ сердца вправо. Г. Появление патологического III тона. Д. Выбухание области сердца.
10. Выберите верные утверждения относительно ХЛС:
A. Хронические заболевания легких служат причиной развития ХЛС у 80-90 % больных.
Б. Для больных с ХЛС характерна одышка, усиливающаяся при физической нагрузке.
B. Эритроцитоз у больных ХЛС не требует коррекции.
Г. Резкое медикаментозное снижение легочной гипертонии может приводить к ухудшению газообменной функции легких. Д. Все вышеперечисленные утверждения верны.
11. Критерии диагноза «декомпенсированное хроническое легочное сердце» включают все нижеперечисленное, кроме:
A. Клинических признаков правожелудочковой недостаточности. Б. Застойных явлений в малом круге кровообращения.
B. Выявления легочной гипертензии.
Г. Наличия трикуспидальной регургитации II-III степени. Д. Наличия хронического легочного заболевания.
5. ОСНОВНЫЕ ВОПРОСЫ ТЕМЫ
5.1. Определение
Хроническое легочное сердце (ХЛС) - гипертрофия и/или дилятация правого желудочка в сочетании с легочной гипертензией, возникающие на фоне различных заболеваний, нарушающих структуру и/или функцию легких, за исключением случаев, когда изменения в легких сами являются результатом первичного поражения левых отделов сердца или врожденных пороков сердца и крупных кровеносных сосудов.
5.2. Этиология
По этиологической классификации, разработанной комитетом экспертов ВОЗ (1961), выделяют 3 группы патологических процессов, ведущих к формированию ХЛС:
Заболевания, ведущие к первичному нарушению прохождение воздуха в бронхах и альвеолах (ХОБЛ, бронхиальная астма, эмфизема легких, бронхоэктатическая болезнь, туберкулез легких, силикоз, легочный фиброз, гранулематозы легких различной этиологии, резекции легких и другие);
Заболевания, приводящие к ограничению движения грудной клетки (кифосколиоз, ожирение, плевральный фиброз, окостенение реберных сочленений, последствия торакопластики, миастения и др.);
Заболевания, сопровождающиеся поражением легочных сосудов (первичная легочная гипертензия, васкулит при системных заболеваниях, рецидивирующая ТЭЛА).
Основная причина - обструктивная болезнь легких, на долю которой приходится 70-80 % всех случаев развития ХЛС.
5.3. Классификация хронического легочного сердца (Вотчал Б.Е., 1964 г)
По степени компенсации:
Компенсированное;
Декомпенсированное. По происхождению:
Васкулярный генез;
Бронхолегочный генез;
Торакодиафрагмальный генез.
5.4. Патогенез хронического легочного сердца
В развитии ХЛС выделяют 3 стадии:
Прекапиллярная гипертензия в малом круге кровообращения;
Гипертрофия правого желудочка;
Правожелудочковая сердечная недостаточность.
В основе патогенеза ХЛС лежит развитие легочной гипертензии. Основные патогенетические механизмы:
Заболевания легких, поражение грудной клетки, позвоночника, диафрагмы. Нарушение вентиляции и механики дыхания. Нарушение бронхиальной проходимости (обструкция). Уменьшение дыхательной поверхности (рестрикция).
Генерализированная гипоксическая вазоконстрикция вследствие альвеолярной гиповентиляции (генерализированный рефлекс Эйлера-Лильестранда), т.е. наступает генерализованное повышение тонуса мелких легочных сосудов и развивается легочная артериальная гипертензия.
Гипертензивное влияние гуморальных факторов (лейкотриенов, ПгF 2 a , тромбоксана, серотонина, молочной кислоты).
Редукция сосудистого русла, склеротические и атеросклеротические изменения в ветвях легочных артерий и в легочном стволе.
Увеличение минутного объема кровообращения вследствие гиперкатехоламинемии, вызванной гипоксемией.
Увеличение вязкости крови вследствие эритроцитоза, развивающегося в ответ на хроническую гипоксемию.
Развитие бронхопульмональных аностомозов.
Повышение внутриальвеолярного давления при обструктивных бронхитах.
На ранних этапах формирования ХЛС преобладают компенсаторно-приспособительные реакции, однако длительное повы-
Рис. 7.1. Основные патогенетические механизмы развития хронического легочного сердца у больных хронической обструктивной болезнью легких
шение давления в легочной артерии приводит к гипертрофии, а с течением времени, при повторных обострениях бронхолегочной инфекции, нарастании обструкции - к дилатации и недостаточности правого желудочка.
5.5. Клиническая картина
Клинические проявления ХЛС включают симптомы:
Основного заболевания, приведшего к развитию ХЛС;
Дыхательной недостаточности;
Сердечной (правожелудочковой) недостаточности.
5.5.1. Жалобы
Одышка, усиливающаяся при физической нагрузке. В отличие от больных с левожелудочковой недостаточностью при декомпенсированном легочном сердце положение тела не влияет на степень одышки - больные свободно могут лежать на спине или на боку. Ортопноэ для них нетипично, так как отсутствует застой в легких, нет «обструкции» малого круга, как при недостаточности левых отделов сердца. Одышка долгое время обусловлена главным образом дыхательной недостаточностью, на нее не влияет применение сердечных гликозидов, она уменьшается при использовании бронхолитиков, кислорода. Выраженность одышки (тахипноэ) часто не связана со степенью артериальной гипоксемии, поэтому имеет ограниченное диагностическое значение.
Стойкая тахикардия.
Кардиалгии, развитие которых связано с метаболическими нарушениями (гипоксия, инфекционно-токсическое влияние), недостаточным развитием коллатералей, рефлекторным сужением правой коронарной артерии (пульмоно-коронарный рефлекс), уменьшением наполнения коронарных артерий при увеличении конечного диастолического давления в полости правого желудочка.
Аритмии чаще встречаются при обострении ХОБЛ, при наличии декомпенсации легочного сердца и у больных, страдающих сопутствующей ИБС, артериальной гипертензией, ожирением.
Неврологические симптомы (краниалгии, головокружение, сонливость, потемнение и двоение в глазах, нарушение речи, плохое сосредоточение мыслей, потеря сознания) связаны с расстройством церебрального кровообращения.
5.5.2. Объективные признаки
Диффузный «теплый» цианоз (дистальные отделы конечностей теплые вследствие сосудорасширяющего действия накапливающейся в крови углекислоты);
Набухание шейных вен вследствие затрудненного оттока крови к правому предсердию (шейные вены набухают лишь на выдохе, особенно у больных с обструктивными поражениями легких; при присоединении сердечной недостаточности они остаются вздутыми и на вдохе).
Утолщение концевых фаланг («барабанные палочки») и ногтей («часовые стекла»).
Отеки нижних конечностей, как правило, менее выражены и не достигают такой степени, как при первичных заболеваниях сердца.
Увеличение печени, асцит, положительный венный пульс, положительный симптом Плеша (гепатоюгулярный симптом - при нажатии на край печени становится очевидным набухание вен шеи).
Систолическая прекардиальная и эпигастральная пульсация (за счет гипертрофии правого желудочка).
Перкуторно определяется расширение абсолютной и относительной сердечной тупости правой границы сердца; перкуторный звук над рукояткой грудины - с тимпаническим оттенком, а над мечевидным отростком становится притупленно-тимпаническим или совсем глухим.
Глухость тонов сердца.
Акцент второго тона над легочной артерией (при повышении давления в ней более чем в 2 раза).
Появление систолического шума над мечевидным отростком или слева от грудины при развитии относительной недостаточности клапанов.
5.5.3. Лабораторные данные
В клиническом анализе крови у больных с ХЛС определяют эритроцитоз, высокий гематокрит, замедление СОЭ.
В биохимическом анализе крови при развитии декомпенсации по правожелудочковому типу возможны увеличение остаточного азота, билирубина, гипоальбуминемия, гиперглобулинемия.
5.5.4. Рентгенологические признаки
Нормальная или увеличенная тень сердца в боковой проекции.
Относительное увеличение дуги ПЖ в левом (втором) косом положении.
Дилатация общего ствола легочной артерии в правом (первом) косом положении.
Расширение главной ветви легочной артерии более 15 мм в боковой проекции.
Увеличение разницы между шириной тени главных сегментарных и субсегментарных ветвей легочной артерии.
Линии Керли (Kerley) - горизонтальные узкие затемнения над реберно-диафрагмальным синусом. Полагают, что они возникают вследствие расширения лимфатических сосудов и утолщения межлобулярных щелей. При наличии линии Керли легочное капиллярное давление превышает 20 мм рт.ст. (в норме - 5-7 мм рт.ст).
5.5.5. Электрокардиографические признаки
Наблюдают признаки гипертрофии и перегрузки правых отделов сердца.
Прямые признаки гипертрофии:
Зубец R в Vi более 7 мм;
Отношение R/S в V более 1;
Собственное отклонение в V - 0,03-0,05 с;
Форма qR в Vi;
Неполная блокада правой ножки пучка Гиса, если R более 10 мм;
Полная блокада правой ножки пучка Гиса, если R более 15 мм;
Картина перегрузки правого желудочка в V1-V2. Косвенные признаки гипертрофии:
Грудные отведения:
Зубец R в V5 менее 5 мм;
Зубец S в V5 более 7 мм;
Отношение R/S в V5 менее 1;
Зубец S в V 1 менее 2 мм;
Полная блокада правой ножки пучка Гиса, если R менее 15 мм;
Неполная блокада правой ножки пучка Гиса, если R менее 10 мм;
Стандартные отведения:
- Р-pulmonale во II и III стандарстных отведениях ЭКГ;
Отклонение ЭОС вправо;
Тип S1S2S3.
5.5.6. Эхокардиогарфичекие признаки
Гипертрофия правого желудочка (толщина его передней стенки превышает 0,5 см).
Дилатация правых отделов сердца (конечный диастолический размер правого желудочка более 2,5 см).
Парадоксальное движение межжелудочковой перегородки в диастолу в сторону левых отделов.
«Д»-образная форма правого желудочка.
Трикуспидальная регургитация.
Систолическое давление в легочной артерии, определяемое при ЭхоКГ, в норме составляет 26-30 мм рт.ст. Выделяют степени легочной гипертензии:
I - 31-50 мм рт.ст.;
II - 51-75 мм рт.ст.;
III - 75 мм рт.ст. и выше.
5.5.7. Морфологические признаки
Увеличение толщины стенки правого желудочка (более 5 мм).
Увеличение массы правого желудочка: более 70 г у мужчин, более 60 г у женщин.
Желудочковый индекс более 0,6 (в норме масса правого желудоч- ка/масса левого желудочка - 0,4-0,6).
Гипертрофия папиллярных мышц правого желудочка, которая вызывает синдром относительной недостаточности трехстворчатого клапана.
5.6. Лечение
Основные принципы лечения больных ХЛС:
Профилактика и лечение лежащих в его основе заболеваний легких.
Медикаментозное снижение легочной гипертензии. Однако резкое медикаментозное снижение легочной гипертонии может приводить к ухудшению газообменной функции легких и увеличению шунта венозной крови, поскольку умеренная легочная гипертония у больных с ХЛС является компенсаторным механизмом вентиляционно-перфузионной дисфункции.
Лечение правожелудочковой недостаточности.
Основная цель лечения больных ХЛС - улучшение показателей транспорта кислорода для снижениия уровня гипоксемии и улучшения контрактильной способности миокарда правых отделов сердца, что достигается за счет снижения резистентности и вазоконстрикции легочных сосудов.
Лечение и профилактика основного заболевания, например ХОБЛ: бронхолитики - антихолинергические препараты (атровент*, беро-
дуал*), селективные Р2-агонисты (беротек*, сальбутамол), метилксантины, муколитики. При обострении процесса - антибактериальные препараты, по необходимости - кортикостероиды.
На всех этапах течения ХЛС патогенетическим методом лечения служит длительная оксигенотерапия - ингаляция воздуха, обогащенного кислородом (30-40 % кислород), через носовой катетер. Скорость потока кислорода - 2-3 л в минуту в покое и 5 л в минуту при нагрузке. Критерии для назначения длительной оксигенотерапии: РаО2 менее 55 мм рт.ст. и сатурация кислорода (насыщенность эритроцита кислородом, S А О 2) менее 90 %. Длительную оксигенотерапию следует назначать как можно раньше с целью коррекции нарушений газового состава крови, снижения артериальной гипоксемии и предупреждения нарушений гемодинамики в малом круге кровообращения, что позволяет приостановить прогрессирование легочной гипертензии и ремоделирование легочных сосудов, повышает выживаемость и улучшает качество жизни больных.
Антагонисты кальция вызывают дилатацию сосудов малого и большого кругов кровообращения, в связи с чем относятся к прямым легочным вазодилятаторам. Тактика назначения антагонистов кальция: лечение начинают с малых доз препарата, постепенно увеличивая суточную дозу, доводя до максимально переносимой; назначают нифедипин - 20-40 мг/сут, адалат * - 30 мг/сут, дилтиазем - от 30-60 мг/сут до 120-180 мг/сут, исрадин^ - 2,5-5,0 мг/сут, верапамил - от 80 до 120-240 мг/сут и др. Курс терапии составляет от 3-4 нед до 3-12 мес. Дозу препарата подбирают с учетом уровня давления в легочной артерии и дифференцированного подхода к побочным эффектам, возникающим при назначении антагонистов кальция. Не следует ожидать немедленного эффекта при применении антагонистов кальция.
Нитраты вызывают дилатацию артерий малого круга кровообращения; уменьшают постнагрузку на правый желудочек вследствие венулодилатации, снижают постнагрузку на ПЖ вследствие уменьшения гипоксической вазоконстрикции ЛА; снижают давление в ЛП и уменьшают посткапиллярную легочную гипертензию за счет уменьшения КДД в ЛЖ. Среднетерапевтическая доза: нитросорбид - 20 мг 4 раза в день.
Ингибиторы АПФ значительно улучшают выживаемость и прогноз жизни у больных с застойной сердечной недостаточностью, в том числе и у больных с ХЛС, поскольку результат применения
ИАПФ - снижение артериолярного и венозного тонуса, уменьшение венозного возврата крови к сердцу, снижение диастолического давления в легочной артерии и правом предсердии, увеличение сердечного выброса. Назначают каптоприл (капотен*) в суточной дозе 75-100 мг, рамиприл - 2,5-5 мг/сут и др., доза зависит от изначального уровня АД. При развитии побочных эффектов или непереносимости ИАПФ могут быть назначены антагонисты рецепторов АТ II (лозартан, валсартан и пр.).
Простагландины - группа лекарственных препаратов, которые позволяют успешно снижать давление в легочной артерии при минимальном влиянии на системный кровоток. Ограничением к их применению служит необходимость длительного внутривенного введения, так как простагландин Е1 обладает коротким периодом полужизни. Для длительной инфузии применяют специальный портативный насос, соединенный с катетером Хикмана, который устанавливают в яремной или подключичной вене. Дозы препарата варьируют от 5 нг/кг в минуту до 100 нг/кг в минуту.
Окись азота действует аналогично эндотелийрелаксирующему фактору. При курсовом ингаляционном применении NO у больных ХЛС наблюдают снижение давления в легочной артерии, повышение парциального давления кислорода в крови, уменьшение легочного сосудистого сопротивления. Однако нельзя забывать о токсическом влиянии NO на организм человека, что требует соблюдения четкого режима дозирования.
Простациклин (или его аналог - илопрост) применяют в качестве вазодилататора.
Диуретики назначают при появлении отеков, сочетая их с ограничением потребляемой жидкости и соли (фуросемид, лазикс * , калийсберегающие диуретики - триамтерен, комбинированные препараты). Следует учитывать, что диуретики способны вызывать сухость слизистой бронхов, снижать мукозный индекс легких и ухудшать реологические свойства крови. На начальных стадиях развития ХЛС при задержке жидкости в организме вследствие гиперальдостеронизма, обусловленного стимулирующим действием гиперкапнии на клубочковую зону коры надпочечников, целесообразно изолированное назначение антагонистов альдостерона (верошпирон * - 50-100 мг утром ежедневно или через день).
Вопрос о целесообразности применения сердечных гликозидов в лечении больных с ХЛС остается спорным. Считается, что сердечные
гликозиды, обладая положительным инотропным действием, приводят к более полному опорожнению желудочков, увеличивают сердечный выброс. Однако у данной категории больных без сопутствующей патологии сердца сердечные гликозиды существенно не улучшают показатели гемодинамики. На фоне приема сердечных гликозидов у больных ХЛС чаще наблюдают симптомы дигиталисной интоксикации.
Важная составляющая лечения - коррекция гемореологических нарушений.
Используют антикоагулянты с целью лечения и профилактики тромбозов, тромбоэмболических осложнений. В условиях стационара в основном применяют гепарин в суточной дозе 5 000-20 000 ЕД подкожно под контролем лабораторных показателей (времени свертывания крови, активированного парциального тромбопластинового времени). Из пероральных антикоагулянтов предпочтение отдается варфарину, который назначают в индивидуально подобранной дозе под контролем МНО.
Также применяют антиагреганты (ацетилсалициловая кислота, курантил *), гирудотерапию.
Профилактические мероприятия должны быть направлены на соблюдение режима труда и отдыха. Необходим полный отказ от курения (в том числе пассивного), по возможности избегание переохлаждения и профилактика острых респираторных вирусных инфекций.
5.7. Прогноз
Длительность легочной гипертензии (от ее появления до летального исхода) ориентировочно составляет 8-10 лет и более. 30-37 % больных с недостаточностью кровообращения и 12,6 % всех больных с сердечнососудистыми заболеваниями умирают от декомпенсации ХЛС.
6. КУРАЦИЯ БОЛЬНЫХ
Задачи курации:
Формирование навыков опроса и осмотра больных с хроническим легочным сердцем;
Формирование навыков постановки предварительного диагноза ХЛС на основании данных опроса и осмотра пациента;
Формирование навыков составления плана обследования и лечения больного ХЛС.
Курация больных является самостоятельной работой студентов. Студенты лично или в группе из 2-3 человек проводят опрос, осмотр, обсуждение состояния больного, формируют предварительный и клинический диагноз, составляют план обследования, лечения, определяют прогноз заболевания.
Результаты работы учащиеся докладывают всей группе, коллективно их обсуждают.
7. КЛИНИЧЕСКИЙ РАЗБОР БОЛЬНОГО
Задачи клинического разбора:
Демонстрация методики осмотра и опроса больных с ХЛС;
Контроль у студентов навыков осмотра и опроса больных с ХЛС;
Демонстрация методики постановки диагноза ХЛС на основании данных опроса и осмотра больных;
Демонстрация методики составления плана обследования;
Демонстрация составления плана лечения.
Клинический разбор проводится преподавателем или студентами под непосредственным руководством преподавателя. В ходе занятия разбираются наиболее типичные и/или сложные с диагностической и/или лечебной точки зрения клинические примеры. В конце разбора формулируется структурированный предварительный или окончательный диагноз, составляется план обследования и лечения пациента.
8. СИТУАЦИОННЫЕ ЗАДАЧИ
Клиническая задача? 1
Больной Д., 54 года, поступил в терапевтическое отделение с жалобами на одышку в покое, усиливающуюся при незначительной физической нагрузке, кашель с отделением скудной гнойной мокроты, общую слабость.
Из анамнеза заболевания известно: считает себя больным в течение 1,5 мес, когда на фоне ОРВИ у больного усилился кашель с выделением мокроты гнойного характера, появилось «свистящее» дыхание, сохранялся субфебрилитет, что больной расценил как обострение хронического бронхита курильщика. В результате проведенной антибиотикотерапии температура нормализовалась, однако продолжал
беспокоить кашель. Пациент отметил снижение толерантности к физической нагрузке (появлялась одышка), а также увеличение отеков нижних конечностей.
Данные объективного осмотра. При аускультации сердца выслушивается систолический шум вдоль левого края грудины и акцент II тона над легочным стволом. ЧСС - 102 в минуту, АД - 140/80 мм рт.ст. Нижний край печени выступает на 4 см из-под реберной дуги. Плотные отеки стоп, голеней.
Клинический анализ крови: эритроциты - 6,0х10 11 /л, Hb - 170 г/л, лейкоциты - 12,2х10 9 /л, палочкоядерные лейкоциты - 10 %, СОЭ - 7 мм/ч.
Электрокардиография: синусовая тахикардия, S-тип ЭКГ, высокий остроконечный P во II, III, avF отведениях, преобладающий R в V1, V2, глубокий S в левых грудных отведениях.
Данные эхокардиографического исследования: аорта в восходящем отделе - 35 мм в диаметре. Левые отделы сердца не расширены. Левое предсердие - 36 мм в диаметре, левый желудочек - 45 мм в диаметре. Толщина межжелудочковой перегородки - 9 мм, толщина задней стенки левого желудочка - 9 мм. ФВ левого желудочка - 62 %. Створки аортального, митрального и легочного клапанов не изменены, подвижность створок не ограничена. Ствол легочной артерии дилатирован. Правые отделы сердца расширены. Правый желудочек - 52 мм в диаметре, правое предсердие: по горизонтали - 51 мм в диаметре, по вертикали - 55 мм в диаметре. Толщина стенки правого желудочка - 12 мм.
При допплерографии определяется митральная и легочная регургитация II степени, трикуспидальная регургитация II степени и легочная гипертензия (систолическое давление в легочной артерии - 38,5 мм рт.ст.).
2. Дайте оценку полученным результатам объективного обследования больного.
Клиническая задача? 2
Пациент Л., 37 лет, поступил в терапевтическое отделение с жалобами на сильную прибавку в весе в течение 7 лет, утомляемость, выраженную сонливость, эпизоды внезапного засыпания, храп во
сне, одышку в покое смешанного характера, усиливающуюся при физической нагрузке.
Объективный осмотр. Рост - 173 см. Вес - 110 кг. Кифоз грудного отдела. Отеки стоп, голеней. Теплый диффузный цианоз. Над легкими дыхание везикулярное, хрипов нет. ЧД - 19 в минуту. Тоны сердца ритмичны, глухие, ЧСС - 96 в минуту. АД - 140/88 мм рт.ст.
Общий анализ крови: Hb - 174 г/л, лейкоциты - 5,5 х10 9 /л, эритроциты - 6,7х10 11 /л, тромбоциты - 350 000. СОЭ - 4 мм/ч. Увеличение протромбиновой активности плазмы, снижение фибринолитической активности плазмы, усиление адгезии тромбоцитов.
Исследование газов крови: PO2 - 92 мм рт.ст., PCO2 - 46 мм рт.ст.
Рентгенография органов грудной клетки: высокое стояние диафрагмы, обеднение сосудистого рисунка. Относительное увеличение дуги ПЖ в левом косом положении. Дилатация общего ствола ЛА в правом косом положении. В боковой проекции определяется усиленный кифоз грудного отдела позвоночника.
Исследование функции внешнего дыхания: ЖЕЛ снижена, ФЖЕЛ1 снижена, индекс Тифно - выше 70 %.
На электрокардиограмме: синусовая тахикардия, отклонение ЭОС резко вправо, блокада левой задней ветви пучка Гиса, блокада правой ножки пучка Гиса. Амплитуды RV1 + SV5 - более 10,5. Слабоотрицательные зубцы Т в V1-V2.
ЭхоКГ. Левые отделы сердца не расширены. Левое предсердие - 36 мм в диаметре, левый желудочек - 45 мм в диаметре. Толщина межжелудочковой перегородки - 12 мм, толщина задней стенки левого желудочка - 13 мм. ФВ левого желудочка - 60 %. Створки аортального, митрального и легочного клапанов не изменены, подвижность створок не ограничена. Правые отделы сердца расширены. Правый желудочек - 54 мм в диаметре, правое предсердие: по горизонтали - 49 мм в диаметре, по вертикали - 53 мм в диаметре. Толщина стенки правого желудочка - 10 мм.
При допплерографии определяется легочная регургитация II степени, трикуспидальная регургитация II степени и легочная гипертензия (систолическое давление в легочной артерии - 42,8 мм рт.ст.).
1. Сформулируйте предварительный диагноз.
2. Объясните патогенез нарушения дыхания при ожирении.
4. Составьте план лечения данного больного.
9. ИТОГОВЫЕ ТЕСТОВЫЕ ЗАДАНИЯ
Выберите один или несколько правильных ответов.
1. Назовите клинические признаки декомпенсированного ХЛС:
A. Диффузный цианоз.
Б. Периферические отеки.
B. Положительный венный пульс. Г. Снижение венозного давления.
Д. Систолический шум на верхушке сердца.
2. Выберите верные утверждения относительно легочной гипертонии:
A. Часто развивается у больных ХОБЛ.
Б. Наиболее информативным методом диагностики служит рентгенологическое исследование грудной клетки.
B. Основной патогенетический механизм - альвеолярная гипоксия. Основной клинический признак - набухание шейных вен на вдохе.
Г. Все вышеперечисленные утверждения верны.
3. При рентгенологическом исследовании органов грудной клетки у больных с ХЛС выявляют:
A. Увеличение конуса легочной артерии. Б. Аортальную конфигурацию сердца.
B. Митральную конфигурацию сердца. Г. Линии Керли.
Д. Все вышеперечисленное.
4. В формировании легочной гипертензии у больных ХОБЛ принимают участие:
A. Спазм легочных артериол. Б. Полицитемия.
B. Декомпенсация правого желудочка.
Г. Вазоактивные вещества, блокирующие синтез оксида азота. Д. Лечение ингаляционными кортикостероидами.
5. Назовите клинические признаки гипертрофии правого желудочка:
A. Расширение границ сердца вправо. Б. Акроцианоз.
B. Эпигастральная пульсация. Г. Пульсация печени.
Д. Систолический шум у мечевидного отростка.
6. Для постановки диагноза «хроническое легочное сердце» необходимо наличие всего нижеперечисленного, кроме:
A. Наличия у больного хронического легочного заболевания. Б. Выявления легочной гипертензии при ЭхоКГ.
B. Дефекта МЖП.
Г. ЭКГ-признаков гипертрофии правого желудочка. Д. Наличия высоких остроконечных зубцов Р во II и III стандартных отведениях.
7. В прогрессировании легочной гипертензии у больных ХОБЛ имеет значение:
A. Лечение ингаляционными кортикостероидами в сочетании с длительно действующими ®2-блокаторами.
Б. Повторные обострения бронхолегочной инфекции.
B. Тромбоз мелких ветвей легочной артерии. Г. Повышение внутригрудного давления.
Д. Вторичный эритроцитоз.
8. Лечение пациента с хроническим декомпенсированным легочным сердцем включает:
A. Диуретики.
Б. Ингибиторы АПФ.
B. Сердечные гликозиды.
Г. Антагонисты альдостерона. Д. Антагонисты кальция.
9. В клиническом анализе крови у пациентов с ХЛС обнаруживают:
A. Тромбоцитоз. Б. Эритроцитоз
B. Лейкоцитоз.
Г. Повышение СОЭ.
Д. Увеличение содержания гемоглобина.
10. Выберите неверные утверждения:
A. Гипертрофия правого желудочка приводит к повышению давления в легочной артерии.
Б. Уменьшение содержания углекислого газа в альвеолярном воздухе приводит к повышению тонуса мелких артерий и артериол легких.
B. ХЛС никогда не развивается при рестриктивных заболеваниях легких.
Г. Частое осложнение ХЛС - мерцание предсердий.
Д. Все утверждения неверны.
11. Какие лекарственные препараты снижают давление в легочной артерии?
A. Нитроглицерин. Б. Теофиллин.
B. Дигоксин. Г. Верапамил.
Д. Ипратропиума бромид.
12. Причинами декомпенсации ХЛС у больных ХОБЛ могут быть все нижеперечисленные, кроме:
A. Инфекционных обострений ХОБЛ. Б. Неинфекционных обострений ХОБЛ.
B. Тромбоэмболии ветвей легочной артерии. Г. Назначения препаратов теофиллина.
Д. Пароксизмов фибрилляции предсердий.
13. Причиной развития ХЛС может быть:
A. Вентильный пневмоторакс. Б. Ожирение.
B. Рецидивирующая тромбоэмболия мелких ветвей легочной артерии.
Г. Бронхиальная астма, леченная ингаляционными кортикостероидами.
Д. Кифосколиоз.
14. ЭхоКГ-признаками ХЛС являются все нижеперечисленные, кроме:
A. Толщина передней стенки правого желудочка превышает
Б. Конечный диастолический размер правого желудочка более 2,5 см.
B. Митральная регургитация.
Г. Трикуспидальная регургитация. Д. Дилатация правого предсердия.
15. Назовите характерные электрокардиографические признаки
A. Амплитуды S V 1 + R V 5 более 38 мм. Б. Отклонение ЭОС вправо.
B. Полная или неполная блокада правой ножки пучка Гиса. Г. Высокий зубец Р во II и III стандартных отведениях.
Д. Широкий зубец Р в I и II стандартных отведениях.
16. Аускультативная картина ХЛС включает в себя:
A. Мягкий систолический шум на верхушке.
Б. Систолический шум над мечевидным отростком.
B. Ослабление I тона в проекции трехстворчатого клапана. Г. Акцент II тона над легочной артерией.
Д. Дополнительный тон на верхушке.
17. У 62-летнего больного, страдающего ХОБЛ, хронической дыхательной недостаточностью, вторичным эритроцитозом, декомпенсированным легочным сердцем, развился сильный приступ загрудинных болей. Объективно: выраженный акроцианоз, число дыханий - 18 в минуту, ЧСС - 100 в минуту, АД - 120/80 мм рт.ст. До снятия ЭКГ необходимо купировать болевой приступ. Назначение какого препарата следует считать ошибочным?
A. Нитроглицерин под язык. Б. Морфин подкожно.
B. Анальгин* внутривенно. Г. Новокаин внутривенно. Д. Гепарин внутривенно.
18. Для больных с хроническим декомпенсированным легочным сердцем характерно:
A. Повышение системного АД.
Б. Повышение центрального венозного давления.
B. Тахикардия. Г. Брадикардия.
Д. Снижение пульсового давления.
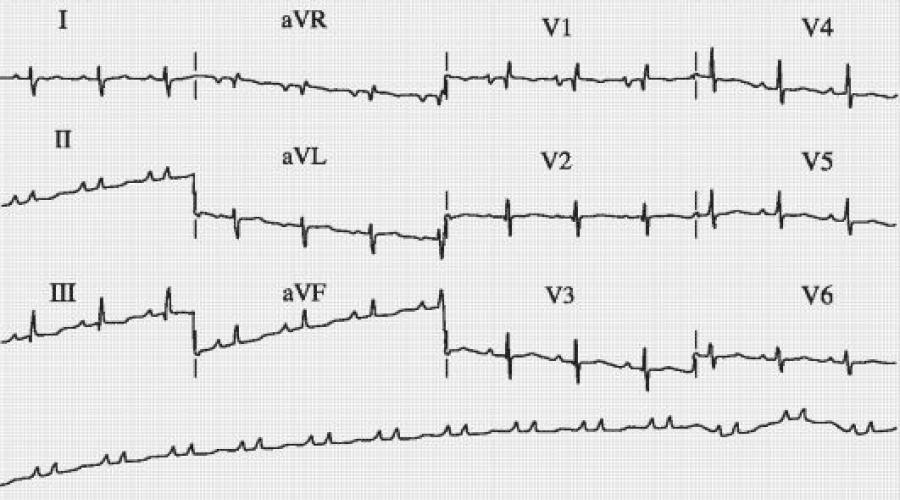
19. Признаками легочной гипертензии у больного ХОБЛ служат следующие ЭКГ-признаки (рис. 7.2):
A. Отклонение электрической оси сердца.
Б. Характер зубца Р во II стандартном отведении.
B. Соотношение зубцов R и S в отведении V 5 . Г. Наличие зубца R в отведении V 1 .
Д. Все вышеперечисленные признаки.
20. Тактика лечения пациента с ХЛС без признаков недостаточности правого желудочка включает:
A. Обязательное назначение ингибиторов АПФ. Б. Ограничение физической нагрузки.
B. Назначение осмотических диуретиков.
Г. Профилактику и лечение хронических заболеваний легких. Д. Назначение антагонистов кальция.
 Рис. 7.2.
(к вопросу 19).
Рис. 7.2.
(к вопросу 19).
21. Лечение ХЛС на ранних этапах при изолированной гипертензии малого круга кровообращения включает назначение:
A. Селективных ®-блокаторов. Б. Осмотических диуретиков.
B. Пролонгированных нитратов. Г. Антагонистов кальция.
Д. Антиагрегантов.
10. ЭТАЛОНЫ ОТВЕТОВ
10.1. Ответы на тестовые задания исходного уровня
10.2. Ответы на ситуационные задачи
Клиническая задача? 1
1. Хронический обструктивный бронхит, в стадии стихающего обострения. ХЛС, стадия декомпенсации. Хроническая сердечная недостаточность, III функциональный класс (по классификации NYHA).
2. Систолический шум вдоль левого края грудины выслушивается при возникновении недостаточности трикуспидального клапана. В данном случае имеет место относительная недостаточность вследствие дилатации правых камер сердца. Акцент II тона над легочным стволом характерен для легочной гипертензии.
3. На электрокардиограмме выявляют признаки нагрузки на правое предсердие, гипертрофии правого желудочка. При эхокардиографическом исследовании обращает на себя внимание интактное состояние левых отделов сердца при гипертрофии в сочетании с дилатацией преимущественно правых камер сердца, наличие легочной гипертензии.
4. Оксигенотерапия, бронхолитики (антихолинергические препараты - беродуал*, атровент*), невысокие дозы ИАПФ или антагонистов рецепторов АТ II под контролем АД, осмотические диуретики (фуросемид - 20-80 мг под контролем диуреза), антагонисты альдостерона (спиронолактон - 25-50 мг в сутки), антагонисты кальция, контроль АД и ЧСС.
Клиническая задача? 2
1. Синдром Пиквика. Ожирение III степени. Дыхательная недостаточность III степени. ХЛС, стадия декомпенсации. Хроническая сердечная недостаточность III функциональный класс (по классификации NYHA).
2. При чрезмерном ожирении происходят следующие нарушения функции дыхания:
Ограничивается подвижность грудной клетки;
Увеличивается кифоз грудного отдела позвоночника, что вызывает почти горизонтальное положение ребер и в связи с этим бочкообразную форму грудной клетки;
Уменьшается подвижность диафрагмы.
Все вышеперечисленные факторы фиксируют грудную клетку в инспираторном положении (как при эмфиземе), вследствие чего
ограничивается пассивный акт выдоха и уменьшается дыхательный объем (ДО) и резервный объем вдоха (РОВд). В результате развивается «поверхностное» дыхание, что приводит к ухудшению притока воздуха к легочным альвеолам. Учащение дыхательных движений - преходящая компенсаторная реакция. При уменьшении ДО на 40 % (250 мл) даже учащение дыхательных движений до 40 в минуту не может поддержать нормальный уровень вентиляции легочных альвеол, что приводит к более или менее устойчивой альвеолярной гиповентиляции.
3. Анализ газового состава крови говорит о наличии синдрома альвеолярной гиповентиляции. В клиническом анализе крови наблюдается вторичный абсолютный эритроцитоз. На электрокардиограмме - признаки легочной гипертензии, гипертрофии правого желудочка. При эхокардиографическом исследовании обнаружены гипертрофия в сочетании с дилатацией правых камер сердца, наличие легочной гипертензии. Спирограмма соответствует рестриктивному типу дыхательной недостаточности.
4. Рекомендуется низкокалорийная диета, ограничение животных жиров, потребление 1 г белка на 1 кг должной массы тела, достаточное количество углеводов для предупреждения кетоза, обогащение витаминами и минералами, снижение потребления поваренной соли. Показаны анорексигенные средства (диетрин®, изолипан®, минифаж®, фепранон*, теронак®), стимуляторы липолиза (диетпласт®). Необходимы консультации различных специалистов (эндокринолога, невролога, генетика и др.) для установления возможной причины ожирения. Следует назначить оксигенотерапию, антиагреганты (ацетисалициловая кислота - 75-125 мг/сут), осмотические диуретики (фуросемид под контролем суточного диуреза), ингибиторы АПФ или антагонисты рецепторов АТ II, антагонисты кальция под контролем
10.3. Ответы на итоговые тестовые задания
3. А, Г. 4.А, Б, Г.
20. А, Б, Г, Д.
Легочное сердце - клинический синдром поражения правого желудочка сердца, возникающий вследствие гипертензии в малом круге кровообращения.
Этиология, патогенез
Причиной гипертензии в малом круге кровообращения могут быть: 1) хронические и специфические заболевания бронхов и легких; 2) поражение легочных сосудов, воспалительные процессы или тромбоэмболия легочной артерии; 3) деформация грудной клетки или позвоночника, вызывающая нарушение механизма дыхания.
Патогенез возникновения легочного сердца сложен и зависит от этиологического фактора, приводящего к развитию данного заболевания. В основе патогенеза лежит гипертония в малом круге кровообращения (легочная гипертензия). Причинами повышения давления в системе легочной артерии могут быть либо орга-
нические поражения в системе мелких сосудов легких, либо функциональные механизмы. Органические поражения легочных сосудов при обтурации капилляров и прекапилляров возникают в связи с:
а) облитерацией или эмболией сосудов легких;
б) механическим сдавливанием легочной артерии извне;
в) пульмонэктомией, когда происходит значительное уменьшение сосудистого русла.
К функциональным механизмам относятся:
а) альвеолярная гипоксия, снижение концентрации кислорода и повышение концентрации углекислого газа в альвеолярном воздухе, что приводит к сужению артерий легких;
б) повышение концентрации в крови метаболитов, оказывающих прессорное действие на сосуды легких;
в) повышение давления воздуха в бронхиолах и альвеолах;
г) повышение вязкости крови;
д) увеличение минутного объема сердца.
Альвеолярная гипоксия развивается при всех хронических неспецифических заболеваниях легких и является одной из главных причин сужения легочных сосудов и уменьшения насыщения крови кислородом. При данной патологии происходит усиление образования в сосудах легких биологически активных веществ (молочной кислоты, гистамина, серотонина, лейкотриенов, тромбоксина), повышающих тонус сосудов легких. Это так называемый рефлекс Эйлера - Лильестранда - спазм артериол легких при уменьшении концентрации кислорода в альвеолярном воздухе.
В свою очередь, спазм сосудов легких приводит к развитию стойкой легочной гипертонии и в конечном итоге к формированию гипертрофии правых отделов сердца, сначала правого желудочка, затем правого предсердия. С течением времени имеющаяся артериальная гипоксемия приводит к некробиотическим и дистрофическим изменениям в сердечной мышце гипертрофированных правых отделов, что способствует быстрому прогрессированию сердечной недостаточности.
Клиническая картина
Клиническая картина легочного сердца представлена симптомами основного заболевания, послужившего причиной его возникновения, а также степенью выраженности легочной и сердечной (правожелудочковой) недостаточности. ВОЗ выделяет три основные группы заболеваний, приводящих к развитию легочного сердца:
1. Заболевания, первично влияющие на прохождение воздуха в легких и альвеолах:
а) хронический бронхит;
б) бронхиальная астма;
в) бронхоэктатическая болезнь, диффузный интерстициальный склероз легких с эмфиземой или без нее (туберкулез, саркоидоз, пневмокониоз, муковисцедоз, синдром Хаммена Рича, диффузный сетчатый пневмосклероз).
2. Заболевания, первично поражающие легочные сосуды:
а) первичная легочная гипертензия;
б) тромбозы и эмболии сосудов легких;
в) сдавливание ствола легочной артерии и легочных вен опухолями средостения и аневризмой;
г) узелковый периартериит и другие артерииты.
3. Заболевания, первично поражающие грудную клетку:
а) кифосколиоз;
б) торокопластика;
в) плевральный фиброз;
г) хронические легочно-мышечные заболевания (в частности, полиомиелит);
д) идиопатическая альвеолярная гиповентиляция.
При тромбоэмболиях ствола, крупных и мелких ветвей легочной артерии, при клапанном пневмотораксе, повторных, тяжелых приступах бронхиальной астмы развивается картина острого и подострого легочного сердца, для которой характерны острое начало, выраженная одышка, серая окраска кожных покровов, акроцианоз, боль за грудиной, нередко интенсивная, кашель, тахикардия, понижение артериального давления, вплоть до коллапса, у 20-30% больных кровохарканье.
На начальных стадиях хронического легочного сердца могут диагностироваться лишь признаки гипертрофии правого желудочка, впоследствии развивается картина легочно-сердечной недостаточности. Основным симптомом легочной И сердечной недостаточности является одышка, которая бывает весьма вариабельной. Усиление одышки обычно наблюдается при обострении хронического бронхолегочного заболевания. Часто больные с хроническими заболеваниями легких отмечают усиление одышки в горизонтальном положении, когда усиливаются вагусное влияние и спазм бронхов.
При декомпенсированном легочном сердце одышка становится постоянной. Она усиливается в горизонтальном положении и уменьшается в полусидячем. Однако одышка не может служить единственным симптомом при постановке данного диагноза, так как является признаком дыхательной недостаточности у больных с ХНЗЛ задолго до развития недостаточности кровообращения у больных с легочным сердцем. Некоторых пациентов беспокоит боль в области сердца неопределенного характера, она локализуется слева от грудины, весьма продолжительна и не купируется после приема валидола и нитроглицерина. Причиной боли является артериальная гипоксемия, оказывающая инфекционно-токсическое воздействие на мышцу сердца и приводящая к нарушению метаболических процессов в миокарде. Болевой синдром может быть также связан со спазмом коронарные артерий из-за пульмокоронарных рефлексов и развитием легочной гипертензии, приводящей к расширению ствола и крупных ветвей легочной артерии.
При осмотре больного обращает на себя внимание цианоз кожных покровов, который обычно бывает диффузным, увеличивается на кончиках пальцев, носу и мочках ушей. Цианоз «теплый» в отличие от «холодного» при первичном поражении сердца. У больных хроническим легочным сердцем обычно отсутствует прямая корреляционная связь между степенью одышки и цианоза. Цианоз появляется при снижении насыщения крови до 85-90%, по мере нарастания гипоксемии степень его увеличивается. Однимиз основных симптомов декомпенсированной правожелудочковои недостаточности является набухание шейных вен. Этот симптом отмечается примерно у 20% больных, связан с повышением внутригрудного давления и сочетается с увеличением печени и появлением отеков нижних конечностей. При легочной недостаточности набухание шейных вен происходит лишь при вдохе, а при сочетании легочной и сердечной недостаточности - как при вдохе, так и при выдохе. У некоторых больных отмечается усиление пульсации в эпигастральной области, обусловленное гипертрофией и перегрузкой правых отделов сердца. При дилатации правого желудочка может развиться относительная недостаточность предсердно-желудочкового клапана, что приводит к появлению систолического шума у мечевидного отростка грудины.
По мере развития сердечной недостаточности тоны сердца становятся глухими, появляется постоянная тахикардия, гипоксия может привести к повышению артериального давления. При декомпенсации заболевания у больных появляются периферические отеки, увеличение печени, основные признаки недостаточности кровообращения. Как правило, пастозность и отеки нижних конечностей отмечаются в период обострения бронхолегочного процесса, что позволяет диагностировать недостаточность кровообращения на ранних стадиях ее возникновения. При сочетании легочного сердце с атеросклеротическим кардиосклерозом или гипертонической болезнью нередко появляются асцит и гидроторакс.
Диагностика
Основываетсяна клинических данных, а также на методах и рентгенологического исследования. В этой фазе проявляются признаки легочной недостаточности и гипертрофии правых отделов сердца. При декомпенсации присоединяются симптомы недостаточности кровообращения, преимущественно по правожелудочковому типу. Перкуторно у больных с хроническим легочным сердцем над всей поверхностью легких определяется коробочный звук за счет эмфиземы. Она же определяет уменьшение границы относительной сердечной тупости, даже при выраженных признаках гипертрофии правых отделов сердца.
Аускультативная картина в легких зависит от выраженности эмфиземы, пневмосклероза и фазы процесса. Наиболее важный симптом поражения сердца -- глухость сердечных тонов, возникающая в связи с увеличением воздушности легких и нарушением сократимости миокарда. У больных с декомпенсированный легочным сердцем часто выслушиваются усиление II тона над легочной артерией и систолический шум над верхушкой сердца или в области мечевидного отростка. Усиление II тона связано с увеличением давления в системе легочной артерии, а систолический шум обусловлен дисфункцией мышцы сердца и относительной недостаточностью трехстворчатого клапана. При выраженной декомпенсации может выслушиваться систолический шум Грехема - Стилла во втором межреберье слева. При присоединении коронарного атеросклероза или кардиосклероза у больных могут отмечаться нарушения сердечного ритма.
В ОАК у таких больных могут определяться эритроцитоз как реакция на гипоксию, повышение гематокрита, увеличение вязкости крови, СОЭ при этом может оставаться нормальным даже при активном воспалительном процессе. В ОАМ (- гематурия, протеинурия, цилиндрурия, что помогает подтвердить недостаточность кровообращения. Рентгенологическое исследование подтверждает увеличение правых отделов сердца, расширение ствола и крупных ветвей легочной артерии сердца при обеднении периферического сосудистого рисунка, усиление пульсации в центре легких и ослабление ее в периферических отделах.
В практической медицине большое значение в диагностике хронического легочного сердца принадлежит электрокардиографии. На ЭКГ регистрируются признаки гипертрофии или перегрузки правых отделов сердца. Электрическая ось расположена вертикально, предсердная ось отклонена вправо. Смещение ее вправо больше чем на 60 градусов приводит к появлению отрицательного зубца Р в отведении aVL, примерно с такой же частотой встречается и P-pulmonale (высокий и заостренный зубец Р более2-2,5 мм во II, III, aVF отведениях при нормальной или несколько увеличенной его ширине).
Одним из популярных неинвазивных методов исследования является реография - определение колебаний кровенаполнения сосудов исследуемого участка тела, связанных по времени с сердечным циклом. Реологическими признаками легочного сердца являются: уменьшение угла наклона систолической волны, почти полное отсутствие диастолической и дикротических волн, низкая реологическая кривая, удлинение периода напряжения, максимального и медленного кровенаполнения.
Типичным признаком может выступать и неполная блокада правой ножки пучка Гиса. Иногда она сочетается с признаками гипертрофии миокарда правого желудочка.
Эхокардиографическая диагностика зависит от выраженности эмфиземы легких. Эхокардиографическими признаками легочного сердца являются снижение амплитуды волны «а» до 1 мм (соответствует систоле правого предсердия), уплощение створок клапана легочной артерии, увеличение амплитуды и скорости открытия створок клапана, появление систолического прикрытия створки.
Одним из ранних и информативных методов инструментальной диагностики легочного сердца является определение давления в легочной артерии (выше 45 мм. рт. ст.).
При формулировании диагноза указывают основное заболевание, послужившее причиной возникновения легочного сердца, степень выраженности легочной недостаточности (острая, подострая, хроническая) и стадию легочного сердца (компенсированное, декомпенсированное).
Дифференциальный диагноз представляет определенные трудности, особенно при разграничении легочно-сердечной и сердечной недостаточности.
См. таблицу «Основные клинические и дифференциально-диагностические признаки легочно-сердечной и сердечной недостаточности» (Мухарлямов Н. М., 1982 г.).
Основные клинические и дифференциально-диагностические признаки
легочно-сердечной и сердечной недостаточности
| Симптомы | Легочно-сердечная недостаточность | Сердечная недостаточность |
| Одышка | Чаще удлинение выдоха, особенно при физической нагрузке | Обычно вдох не удлинен |
| Цианоз | Выражен и распространен, конечности теплые | Преимущественно периферический (фаланги, нос), конечности холодные |
| Положение больного | Нередко горизонтальное | Полусидячее |
| Вздутие вен шеи | Усиливается при выдохе | Выражено одинаково при выдохе и вдохе |
| Мерцательная аритмия | Редко | Часто |
| Начало заболевания | Кашель, в анамнезе -простудные заболевания | В анамнезе - заболевания сердца; одышка, кашель возникают позже, связаны с застоем в легких |
| Тоны сердца | Глухие. Акцент 2 тона над легочной артерией | |
| Пульсация в эпигастральной области | Как правило | Редко |
| Характер поражения | Чаще обструктивный, реже обструктивно-рестриктивный | Обычно рестриктивный |
| Данные перкуссии и аускультации | Коробочный звук, рассеянные по всем полям, сухие, свистящие на фоне удлиненного выдоха | Влажные хрипы в нижних отделах, выдох может быть удлинен, коробочный звук редок |
| ЭКГ | Признаки гипертрофии правого желудочка (правограмма, легочный зубец Р). Блокада правой ножки пучка Гиса | Зависит от заболевания сердца. Отсутствие легочного зубца Р за исключением поздних стадий митрального стеноза |
| Рентгенологические признаки | Увеличение правых отделов сердца, расширение ствола и крупных ветвей легочной артерии, мелкие ветви сужены | При выраженной сердечной недостаточности диффузное увеличение всех отделов сердца |
Лечение
Оно зависит от течения процесса и основного заболевания, приводящего к данному осложнению. Так, при тромбоэмболии легочной артерии проводится неотложная тромболитическая терапия под контролем свертывания крови. Перед экстренной госпитализацией в стационар больному вводят наркотические анальгетики, начинают внутривенное капельное введение гепарина (20 000-30 000 ЕД), фибринолизина (40 000-60 000 ЕД) в сочетании с антигистаминными препаратами, сердечными гликозидами, эуфиллином, хлоридом калия, глюкокортикоидами или адреномиметиками, витамином В6. При возникновении пневмоторакса необходимы неотложные мероприятия. Для уменьшения болей и возможного плевропульмонального шока вводят наркотические анальгетики (1%-ный раствор морфина 1-2 мл подкожно), проводят пункцию плевральной полости с аспирацией воздуха. Осуществляют экстренную госпитализацию в стационар хирургического профиля.
Своевременная и индивидуально подобранная комплексная терапия позволяет сохранить трудоспособность больных. Традиционная схема лечения больных хроническим легочным сердцем включает:
1. Лечение основного заболевания, то есть ликвидация активного воспалительного процесса в легочной ткани путем назначения антибактериальных препаратов группы пенициллинов, макролидов, аминогликозидов, цефалоспоринов и др. При необходимости назначают противовирусные препараты ремантадин, ацикловир.
2. Восстановление бронхиальной проводимости, которое достигается с помощью адреномиметических средств (алупент, астмопент, сальбутамол, беротек, бриканил, ипрадол, фенотирол и др.). С этой целью могут быть назначены метилксантины (эуфиллин, теофиллин, теодер, теотард, теолонг) и холинолитики (беродуал, эудур и др.). Для уменьшения отека слизистой оболочки бронхов назначают глюкокортикоиды (преднизолон, триамцинолон), предпочтение отдают использованию глюкокортикоидов в форме аэрозолей (бекотид, бекламетазон).
Для разжижения бронхиального секрета назначают протеолитические ферменты (трипсин, химотрипсин, профезим). С цельюрегидрации секрета назначают минеральные соли, эфирные масла. Подавляют упорный непродуктивный кашель бромгексином, сиропом и таблетками синекода, ингаляциями лидокаина.
3. Коррекцию нарушенного иммунитета, которая достигается с помощью назначения тимозина, зиксорина, амиксина, иммунала и др.
4. Улучшение гемодинамики, лечение недостаточности кровообращения и легочной гипертензии. С этой целью назначают четыре группы препаратов:
а) сердечные гликозиды (дигоксин, строфантин, коргликон, конваллатоксин и др.);
б) периферические вазодилататоры (нитроглицерин, нитропруссид натрия, Молсидомин, гидралазин и др.). С целью уменьшения давления в легочной артерии назначают антагонисты ионов кальция (нифедипин, верапамил), ингибиторы ангиотензинпревращающего фермента (Эналаприл, капотен и др.) и вазодилататоры;
в) диуретики (фурасемид, гипотиазид, лазикс, альдактон и др.);
г) глюкокортикоиды, прогестерон для воздействия на основные звенья патогенеза легочно-сердечной недостаточности, а также проводят гравитационную хирургию крови (гемосорбция, эритроцитопоэз) и сердечно-легочную трансплантацию.
5. Уменьшение внутрисосудистого фибринообразования и тромбинообразования, которое достигается назначением аспирина, гепарина, фибринолизина, тромбокиназы, трентала, курантила.
6. Борьбу с гипоксемией и гиперкапнией, которая проводится при помощи оксигенотерапии - самого эффективного метода лечения хронического легочного сердца (проводится вдыхание 40-60%-ной смеси через носовой катетер со скоростью 6-9 л в минуту), гиперболической оксигенации, вспомогательной искусственной вентиляции легких. В восстановительном периоде широко назначаются массаж грудной клетки, лечебная физкультура для восстановления нормального типа дыхания. Показания к санаторно-курортному лечению при хроническом легочном сердце определяются основным заболеванием. Прогноз зависит от основного заболевания, характера легочного процесса.
Диспансеризация
С целью предупреждения развития легочного сердца необходимо проводить регулярную диспансеризацию, а также своевременную и адекватную терапию заболеваний, приводящих к данному осложнению. Больные подлежат диспансерному наблюдению не реже 1 раза в месяц, для них проводятся курсы поддерживающего и противорецидивного лечения амбулаторно и в стационаре. Показаниями к госпитализации являются острое и подострое легочное сердце, хроническое легочное сердце при нарастании симптомов дыхательной и правожелудочковой недостаточности, нарушения сердечного ритма, угрожающие жизни.
Развитию легочного сердца обязательно предшествует легочная гипертензия. Хотя высокий сердечный выброс, тахикардия, увеличенный объем крови могут вносить вклад в развитие легочной гипертензии, основную роль в патогенезе последней играет перегрузка правого желудочка вследствие увеличенного сопротивления легочному кровотоку на уровне мелких мышечных артерий и артериол. Увеличение сосудистого сопротивления может быть следствием анатомических причин или вазомоторных нарушений; чаще всего имеет место сочетание этих факторов (табл. 191-2). В отличие от ситуации, наблюдающейся при недостаточности левого желудочка, при легочной гипертензии сердечный выброс обычно в пределах нормы и повышен, периферический пульс напряженный, конечности теплые; все это имеет место на фоне явных признаков системного венозного застоя. Периферические отеки, осложняющие легочное сердце, обычно считают следствием сердечной недостаточности, однако это объяснение нельзя считать удовлетворительным, поскольку давление в легочном стволе редко превышает 65-80 кПа, за исключением тех случаев, когда наблюдается резкое ухудшение состояния при выраженной гипоксии и ацидозе.
Выше отмечалось, что увеличение работы правого желудочка, вызванное легочной гипертензией, может привести к развитию его недостаточности. Однако даже у больных со сниженным в результате легочной гипертензии ударным объемом правого желудочка его миокард способен нормально функционировать при устранении перегрузки.
Анатомическое увеличение сопротивления легочных сосудов. В норме в состоянии покоя легочный круг кровообращения способен поддерживать примерно такой же уровень кровотока, как и в системном круге кровообращения, при этом давление в нем составляет около 1/5 от среднего АД. Во время умеренной физической нагрузки увеличение общего кровотока в 3 раза вызывает лишь небольшое повышение давления в легочном стволе. Даже после пневмонэктомии сохранившаяся сосудистая сеть выдерживает достаточное увеличение легочного кровотока, реагируя на него лишь небольшим повышением давления в легочном стволе до тех пор, пока в легких отсутствуют фиброз, эмфизема или изменения сосудов. Аналогично ампутация большей части легочного капиллярного русла при эмфиземе обычно не вызывает легочную гипертензию.
Однако, когда сосудистый резерв легких истощается вследствие прогрессирующего уменьшения площади и растяжимости легочной сосудистой сети, даже небольшое увеличение легочного кровотока, связанное с повседневной жизненной активностью, может привести к появлению значительной легочной гипертензии. Необходимым условием этого является существенное уменьшение площади поперечного сечения легочных резистивных сосудов. Уменьшение площади легочного сосудистого русла — это следствие обширного сужения и обструкции мелких легочных артерий и артериол и сопровождающего этот процесс уменьшения растяжимости не только самих сосудов, но и окружающей их сосудистой ткани.
Таблица 191-2. Патогенетические механизмы при хронической легочной гипертензии и легочном сердце
Патогенетический механизм
Учебники, методички, атласы
Акушерство и Гинекология
Анатомия
Биология
Внутренние болезни
Гистология
Дерматология
Инфекционные болезни
Кардиология
Медицинская генетика
Неврология
Офтальмология
- Легочное сердце: этиология, патогенез, классификация.
ЛЕГОЧНОЕ СЕРДЦЕ — патологическое состояние, характеризующееся гипертрофией и дилатацией (а затем и недостаточностью) правого желудочка сердца вследствие артериальной легочной гипертензии при поражениях системы дыхания.
Этиология. Различают:
1) васкулярную форму легочного сердца — при легочных васкулитах, первичной легочной гипертензии, горной болезни, тромбоэмболии легочных артерий;
2) бронхолегочную форму, наблюдавшуюся при диффузном поражении бронхов и легочной паренхимы — при бронхиальной астме, бронхиолите, хроническом обструктивном бронхите, эмфиземе легких, диффузном пневмосклерозе и фиброзах легких в исходе неспецифических пневмоний, туберкулезе, при пневмокониозе, саркоидозе, синдроме Хам-мена — Рича и др;
3) торакодиафрагмальную форму легочного сердца, развивающуюся при значительных нарушениях вентиляции и кровотока в легких вследствие деформации грудной клетки (кифосколиозы и др.), патологии плевры, диафрагмы (при торакопластике, массивном фибротораксе, пикквикском синдроме и т. п.).
Патогенез. Ведущее значение имеет легочная артериальная гипертензия, обусловленная патологическим повышением сопротивления кровотоку при гипертонии легочных артериол — первичной (при первичной легочной гипертензии) или в ответ на альвеолярную гипоксию (при горной болезни, нарушениях вентиляции альвеол у больных с бронхиальной обструкцией, кифосколиозом и др.) либо вследствие анатомического уменьшения просвета артериального легочного русла за счет склероза, облитерации (в зонах пневмосклероза, легочного фиброза, при васкулитах), тромбоза или тромбоэмболии, после хирургического иссечения (при пульмонэктомии). При дыхательной недостаточности у больных с обширным поражением паренхимы легких патогенетическое значение имеет и нагрузка сердца вследствие компенсаторного повышения объема кровообращения за счет усиленного венозного возврата крови к сердцу.
Классификация. По особенностям развития выделяют острое легочное сердце, развивающееся за несколько часов или дней (например, при массивной тромбоэмболии легочных артерий, клапанном пневмотораксе), подострое (развивается за недели, месяцы при повторных тромбоэмболиях легочных артерий, первичной легочной гипертензии, лимфо-генном карциноматозе легких, тяжелом течении бронхиальной астмы, бронхиолитов) и хроническое, формирующееся на фоне многолетней дыхательной недостаточности.
В развитии хронического легочного сердца выделяют три стадии: 1 стадия (доклиническая) характеризуется транзиторной легочной гипертензией с признаками напряженной деятельности правого желудочка, которые выявляются только при инструментальном исследовании; II стадия определяется по наличию признаков гипертрофии правого желудочка и стабильной легочной гипертензии при отсутствии недостаточности кровообращения; III стадия, или стадия декомпенсированного легочного сердца (синоним: легочно-сердечная недостаточность), наступает со времени появления первых симптомов недостаточности правого желудочка.
Клинические проявления. Острое легочное сердце проявляется болью за грудиной, резко учащенным дыханием, падением АД, вплоть до развития коллапса, пепельно-серым диффузным цианозом, расширением границы сердца вправо, иногда появлением подложечной пульсации; нарастающей тахикардией, усилением и акцентом II тона сердца над легочным стволом; отклонением электрической оси сердца вправо и электрокардиографическими признаками перегрузки правого предсердия; повышением венозного давления, набуханием шейных вен, увеличением печени, нередко сопровождающимся болями в правом подреберье.
Хроническое легочное сердце до стадии декомпенсации распознается по симптомам гиперфункции, затем гипертрофии правого желудочка на фоне артериальной гипертензии, выявляемых вначале с помощью ЭКГ рентгенологического исследования грудной клетки и других инструментальных методов, а в последующем и по клиническим признакам: появлению выраженного сердечного толчка (сотрясение передней грудной стенки при сокращениях сердца), пульсации правого желудочка, определяемой пальпаторно за мечевидным отростком, усилению и постоянному акценту II тона сердца над стволом легочной артерии при нередком усилении I тона над нижней частью грудины. В стадии декомпенсации появляется правожелудочковая недостаточность: тахикардия;
акроцианоз; набухание шейных вен, сохраняющееся на вдохе (их набухание только на выдохе может быть обусловлено бронхиальной обструкцией) никтурия; увеличение печени, периферические отеки (см. Сердечная недостаточность).
Лечение. Проводятся лечение основного заболевания (ликвидация пневмоторакса, тромболитическая терапия или хирургическое вмешательство при тромбоэмболии легочных артерий, терапия бронхиальной астмы и т. д.), а также меры, направленные на устранение дыхательной недостаточности. По показаниям применяют бронхолитики, отхаркивающие средства, дыхательные аналептики, оксигенотерапию. Декомпенсация хронического легочного сердца у больных с бронхиальной обструкцией является показанием к постоянной терапии глюкокортикоидами (преднизолон и др.), если они эффективны. С целью снижения артериальной легочной гипертензии при хроническом легочном сердце могут быть применены эуфиллин (в/в, в свечах); в ранних стадиях-нифедипин (адалат, коринфар); в стадии декомпенсации кровообращения — нитраты (нитроглицерин, нитросорбид) под контролем содержания кислорода в крови (возможно усиление гипоксемии). При развитии сердечной недостаточности показано лечение сердечными гликозидами и мочегонными средствами, которое проводится с большой осторожностью из-за высокой чувствительности миокарда к токсическому действию гликозидов на фоне гипоксии и гипокалигистии, обусловленных дыхательной недостаточностью. При гипокапиемии применяют панангин, хлорид калия.
Если диуретики применяются часто, преимущества имеют калийсберегающие препараты (триампур, альдактон и др.).
Во избежание развития фибрилляции желудочков сердца внутривенное введение сердечных гликозидов нельзя сочетать с одновременным введением эуфиллина, препаратов кальция (антагонисты по влиянию на гетеротопный автоматизм миокарда). При необходимости коргликон вводят в/в капельно не ранее чем через 30 мин после окончания введения зуфиллина. По той же причине не следует вводить в/в сердечные гликозиды на фоне интоксикации адреномиметиками у больных с бронхиальной обструкцией (астматический статус и др.). Поддерживающая терапия дигоксином или изо-ланидом у больных с декомпенсированным хроническим легочным сердцем подбирается с учетом снижения толерантности к токсическому действию препаратов в случае нарастания дыхательной недостаточности.
Профилактика состоит в предупреждении, а также своевременном и эффективном лечении болезней, осложняющихся развитием легочного сердца. Больные хроническими бронхолегочными заболеваниями подлежат диспансерному наблюдению с целью предупреждения обострении и проведения рациональной терапии дыхательной недостаточности. Большое значение имеет правильное трудоустройство больных с ограничением физической нагрузки, способствующей возрастанию легочной гипертензии.
- Коарктация аорты: клиника, диагностика, лечение.
оарктация аорты (КА) это врождённое сужение аорты, степень которого может достигать полного перерыва.
В изолированном виде порок встречается нечасто (в 18% случаев). Обычно он сочетается с другими аномалиями (двустворчатый аортальный клапан, открытый артериальный проток, дефект межжелудочковой перегородки и др.).
Типичные места сужения аорты чуть выше и ниже отхождения открытого артериального протока (соответственно, инфантильный и взрослый типы КА). КА может иметь и атипичное расположение, даже на уровне брюшного отдела аорты, но это бывает крайне редко. Сужение в области коарктации может колебаться от умеренного (более 5 мм) до выраженного (менее 5 мм). Иногда имеется точечное отверстие не более 1 мм. Протяжённость участка сужения также варьирует и может быть как очень небольшой 1 мм, так и протяжённой 2 см и более.
Выделяют четыре типа коарктации аорты:
изолированное сужение аорты
сужение аорты в сочетании с открытым артериальным протоком
сужение аорты в сочетании с дефектом межжелудочковой перегородки
сужение аорты в сочетании с другими пороками развития сердца.
Выделяют пять периодов естественного течения коарктации аорты.
I период критический, возраст до 1 года, симптоматика недостаточности кровообращения (обычно по малому кругу), также зависящая от сопутствующих аномалий; высокая смертность.
II период приспособления, возраст 15 лет, уменьшение симптомов недостаточности кровообращения, которые к концу периода обычно представлены лишь одышкой и повышенной утомляемостью.
III период компенсации, возраст 515 лет, различные варианты течения, нередко бессимптомные.
IV период относительной декомпенсации, возраст полового созревания, нарастание симптоматики недостаточности кровообращения.
V период декомпенсации, возраст 2040 лет, симптомы артериальной гипертензии и её осложнений, тяжёлая недостаточность кровообращения по обоим кругам.
Жалобы У детей раннего возраста преобладает симптоматика недостаточности кровообращения по малому кругу (одышка, ортопноэ, сердечная астма, отёк лёгких) При постдуктальном варианте КА может манифестировать кардиогенным шоком при закрытии ОАП У более старших детей преобладает симптоматика артериальной гипертензии (нарушения мозгового кровоснабжения, головные боли, носовые кровотечения) и, значительно реже, снижения кровотока дистальнее сужения аорты (перемежающаяся хромота, абдоминальные боли, связанные с ишемией кишечника) Симптомы сопутствующих аномалий
Преобладание физического развития плечевого пояса при тонких ногах (атлетическое телосложение) у детей старшей возрастной группы Пульсация межрёберных артерий Цианоз при сочетании КА с ВПС, сопровождающимися сбросом крови справа налево Ослабление пульсации на артериях нижних конечностей Разница АД на верхних и нижних конечностях более 20 мм рт.ст Запаздывание пульсовой волны на нижних конечностях по сравнению с верхними Усиленный верхушечный толчок Усиленная пульсация сонных артерий Систолический шум над основанием сердца, проводящийся по левому краю грудины, в межлопаточную область и на сонные артерии Щелчок систолического изгнания на верхушке и основании сердца Аускультативная симптоматика может отсутствовать вовсе Симптомы сопутствующих аномалий
ЭКГ Признаки гипертрофии и перегрузки правых (60% грудных детей), левых (20% грудных детей) или правых и левых (5% грудных детей) отделов Ишемические изменения конечной части желудочкового комплекса (50% грудных детей без фиброэластоза и 100% детей с фиброэластозом миокарда), в 15% случаев признаки гипертрофии миокарда отсутствуют См. также Проток артериальный открытый, Стеноз клапана аорты, Дефект межжелудочковой перегородки.
Рентгенография органов грудной клетки Выбухание дуги лёгочной артерии Кардиомегалия У детей старшего возраста тень, образованная дугой аорты и её расширенной нисходящей частью, может принимать форму цифры 3. Эти же изменения придают пищеводу, наполненному барием, вид буквы Е Узурацию рёбер, вызванную давлением расширенных межрёберных и внутренних грудных сосудов, обнаруживают у пациентов старше 5 лет
ЭхоКГ Гипертрофия миокарда и дилатация полостей сердца зависят от степени сужения аорты и сопутствующих аномалий В трети случаев клапан аорты двухстворчатый Визуализация стеноза, определение его степени. анатомического варианта (локальный, диффузный, тандемный) и отношение к ОАП Измерение трансстенотического градиента давления Детям старших возрастных групп и взрослым проводят чреспищеводную ЭхоКГ.
Медикаментозная терапия. Консервативное лечение постоперационных больных предполагает коррекцию систолической гипертензии, сердечной недостаточности, профилактику тромбоза аорты. В дальнейшем при ведении гаких больных должен решаться вопрос о назначении антиатеросклеротической терапии для предотвращения возможной рекоарктации. Профилактика инфекционного эндокардита. При лечении кардиогенного шока применяют стандартные схемы. При постдуктальном или невыясненном варианте КА, даже при закрытом ОАП, проводят инфузию ПгЕ1 (алпростадил) 0,050,1 мг/кг/мин. После стабилизации гемодинамики проводят неотложную оперативную коррекцию. При лечении артериальной гипертензии у взрослых предпочтение отдают ингибиторам АПФ и антагонистам кальция. В послеоперационном периоде может развиться временное усугубление гипертензии, при котором назначают b-адреноблокаторы и нитропруссид.
Хирургическое лечение Показания Оперативному лечению подлежат все пациенты с КА в возрасте до 1 года
- Осложнения инфаркта миокарда. Кардиогенный шок.
Три групп s осложнения ИМ:
Нарушение ритма и проводимости.
Нарушение насосной функции сердца (острая лево-, правожелудочковая недостаточность, аневризма, расширение зоны инфаркта).
Другие осложнения: эпистенокардический перикардит, тромбоэмболии, ранняя постинфарктная стенокардия, синдром Дреслера.
истинный кардиогенный шок (при поражение больше 40% миокарда) — АД меньше 80 мм рт. ст.
Кардиоге́нный шок крайняя степень левожелудочковой недостаточности, характеризующаяся резким снижением сократительной способности миокарда (падением ударного и минутного выброса), которое не компенсируется повышением сосудистого сопротивления и приводит к неадекватному кровоснабжению всех органов и тканей, прежде всего жизненно важных органов. Чаще всего он развивается как осложнение инфаркта миокарда, реже миокардита или отравления кардиотоксическими субстанциями. При этом, возможны четыре различных механизма, вызывающих шок:
Расстройство насосной функции сердечной мышцы;
Тяжелые нарушения сердечного ритма;
Тампонада желудочков выпотом или кровотечением в сердечную сумку;
Шок вследствие массивной эмболии легочной артерии, как особая форма КШ
Патогенез
Тяжёлое нарушение сократительной функции миокарда с дополнительным присоединением усугубляющих ишемию миокарда факторов.
Активация симпатической нервной системы вследствие падения сердечного выброса и снижения АД приводит к учащению ритма сердца и усилению сократительной деятельности миокарда, что увеличивает потребность сердца в кислороде.
Задержка жидкости из-за снижения почечного кровотока и увеличение ОЦК, что усиливает преднагрузку на сердце, способствует отёку лёгких и гипоксемии.
Увеличение ОПСС из-за вазоконстрикции, приводящее к увеличению постнагрузки на сердце и увеличению потребности миокарда в кислороде.
Нарушение диастолического расслабления левого желудочка миокарда из-за нарушения его наполнения и снижения податливости, что вызывает увеличение давления в левом предсердии и способствует усилению застоя крови в лёгких.
Метаболический ацидоз вследствие длительной гипоперфузии органов и тканей.
Клинические проявления
Артериальная гипотензия систолическое АД менее 90 мм рт.ст. или на 30 мм рт.ст. ниже обычного уровня в течение 30 мин и более. Сердечный индекс менее 1,8-2 л/мин/м2.
Нарушение периферической перфузии почек олигурия, кожи бледность, повышенная влажность
ЦНС загруженность, сопор.
Отёк лёгких, как проявление левожелудочковой недостаточности.
При обследовании больного обнаруживают холодные конечности, нарушение сознания, артериальную гипотензию (среднее АД ниже 50-60 мм рт.ст.), тахикардию, глухие тоны сердца, олигурию (менее 20 мл/мин). При аускультации лёгких могут быть выявлены влажные хрипы.
Дифференциальная диагностика
Необходимо исключить другие причины артериальной гипотензии: гиповолемию, вазовагальные реакции, электролитные нарушения (например, гипонатриемию), побочные эффекты лекарств, аритмии (например, пароксизмальные наджелудочковые и желудочковые тахикардии).
Основная цель терапии повышение АД.
Лекарственная терапия
АД следует повышать до 90 мм рт.ст. и выше. Используют следующие лекарственные средства, которые предпочтительнее вводить через дозаторы:
Добутамин (селективный b 1-адреномиметик с положительным инотропным эффектом и минимальным положительным хронотропным эффектом, то есть эффект увеличения ЧСС выражен незначительно) в дозе 2,5-10 мкг/кг/мин
Допамин (обладает более выраженным положительным хронотропным эффектом, то есть может увеличить ЧСС и соответственно потребность миокарда в кислороде, несколько усугубив тем самым ишемию миокарда) в дозе 2-10 мкг/кг/мин с постепенным увеличением дозы каждые 2-5 мин до 20-50 мкг/кг/мин
Норэпинефрин в дозе 2-4 мкг/мин (до 15 мкг/мин), хотя он, наряду с усилением сократимости миокарда, в значительной степени увеличивает ОПСС, что также может усугубить ишемию миокарда.
В основе развития легочного сердца не зависимо от причины лежит легочная артериальная гипертензия , формирование которой обусловлено несколькими патогенетическими механизмами.
Патогенез острого легочного сердца (на примере ТЭЛА). В формировании ОЛС участвуют два патогенетических механизма:
– «механическая» обструкция сосудистого русла,
– гуморальные изменения.
«Механическая» обструкция сосудистого русла возникает вследствие обширной обструкции артериального русла легких (на 40–50%, что соответствует включению в патологический процесс 2–3 ветвей легочной артерии), что увеличивает общее легочное сосудистое сопротивление (ОЛСС). Увеличение ОЛСС сопровождается повышением давления в легочной артерии, препятствующей выбросу крови из правого желудочка, уменьшению наполнения левого желудочка, что суммарно приводит к снижению минутного объема крови и падению артериального давления (АД).
Гуморальные нарушения , возникающие в первые часы после обструкции сосудистого русла, в результате выброса биологически активных субстанций (серотонина, простагландинов, катехоламинов, выделение конвертазы, ангиотензинпревращающего фермента, гистамин), приводят к рефлекторному сужению мелких ветвей легочной артерии (генерализованная гипертоническая реакция легочных артерий), что еще больше увеличивает ОЛСС.
Первые часы после ТЭЛА характеризуются особенно высокой легочной артериальной гипертензией, быстро приводящей к перенапряжению правого желудочка, его дилатации и декомпенсации.
Патогенез хронического легочного сердца (на примере ХОБЛ). Ключевыми звеньями патогенеза ХЛС являются:
– гипоксическая легочная вазоконстрикция,
– нарушения бронхиальной проходимости,
– гиперкапния и ацидоз,
– анатомические изменения легочного сосудистого русла,
– гипервискозный синдром,
– увеличение сердечного выброса.
Гипоксическая легочная вазоконстрикция . Регуляция кровотока в системе малого круга кровообращения осуществляется благодаря рефлексу Эйлера–Лильестранда , который обеспечивает адекватное соотношение вентиляции и перфузии легочной ткани. При уменьшении концентрации кислорода в альвеолах благодаря рефлексу Эйле-ра-Лильестранда рефлекторно закрываются прекапиллярные сфинктеры (возникает вазоконстрикция), что приводит к ограничению кровотока в этих участках легкого. В результате чего местный легочный кровоток приспосабливается к интенсивности легочной вентиляции, и нарушений вентиляционно-перфузионных соотношений не происходит.
Нарушения бронхиальной проходимости. Неравномерность легочной вентиляции вызывает альвеолярную гипоксию, обусловливает нарушения вентиляционно-перфузионных соотношений и приводит к генерализованному проявлению механизма гипоксической легочной вазоконстрикции. Развитию альвеолярной гипоксии и формированию ХЛС больше подвержены больные, страдающие хроническим обструктивным бронхитом и бронхиальной астмой с преобладанием признаков дыхательной недостаточности («синие одутловатики»). У пациентов с преобладанием ре-стриктивных нарушений и диффузными поражениями легких (―розовые пыхтельщики) альвеолярная гипоксия выражена значительно меньше.
Гиперкапния не прямо, а опосредовано влияет на возникновение легочной гипертензии путем:
– появления ацидоза и, соответственно, рефлекторной вазоконстрикции,
– снижения чувствительности дыхательного центра к СО2, что усугубляет нарушения вентиляции легких.
Анатомические изменения легочного сосудистого русла, вызывающие повыше-ние ОЛСС, заключаются в развитии:
– гипертрофии медии легочных артериол (за счет пролиферации гладкой му-скулатуры сосудистой стенки),
– запустевании артериол и капилляров,
– тромбозе микроциркуляторного русла,
– развитии бронхопульмональных анастомозов.
Гипервискозный синдром у больных с ХЛС развивается вследствие вторичного эритроцитоза. Этот механизм участвует в формировании легочной артериальной гипертензии при любом типе дыхательной недостаточности, проявляющейся выраженным цианозом. У больных ХЛС повышение агрегации форменных элементов крови и вязкости крови затрудняет кровоток по сосудистому руслу легких. В свою очередь повышение вязкости и замедление кровотока способствуют образованию пристеночных тромбов в ветвях легочной артерии. Вся совокупность гемостазиологических нарушение проводит к увеличению ОЛСС.
Увеличение сердечного выброса обусловлено:
– тахикардией (увеличение сердечного выброса при значительной бронхиальной обструкции достигается возрастанием не ударного объема, а частоты сердечных сокращений, поскольку повышение внутригрудного давления препятствует венозному притоку крови в правый желудочек);
– гиперволемией (одной из возможных причин гиперволемии является гиперкапния, способствующая увеличению концентрации альдостерона в крови и, соответствен-но, задержке Nа+ и воды).
Непременной составной частью патогенеза легочного сердца являются раннее развитие дистрофии миокарда правого желудочка и изменения гемодинамики.
Развитие дистрофии миокарда определяется тем, что укорочение диастолы при тахикардии и повышение внутрижелудочкового давления приводит к снижению кро-вотока в мышце правого желудочка и, соответственно энергодефициту. У ряда больных развитие миокардиодистрофии связано с интоксикацией из очагов хронической инфекции в дыхательных путях или паренхиме легких.
Гемодинамические изменения наиболее характерны для больных с развернутой клинической картиной ХЛС. Основными из них являются:
– гипертрофия правого желудочка (ХЛС характеризуется постепенным и медленным развитием, поэтому сопровождается развитием гипертрофии миокарда правого желудочка. ОЛС развивается в результате внезапного и значительного повышения давления в легочной артерии, что приводит к рез-кому расширению правого желудочка и истончению его стенки, поэтому гипертрофия правых отделов сердца развиться не успевает).
– снижение систолической функции правых отделов сердца с развитием застоя крови в венозном русле большого круга кровообращения,
– увеличение объема циркулирующей крови,
– снижение сердечного выброса и уровня АД.
Таким образом, при бронхолегочной патологии стойкая легочная гипертензия формируется вследствие органического сужения просвета легочных сосудов (за счет облитерации, микротромбоза, сдавления сосудов, снижения способности легких к растяжению) и функциональных изменений (вызванных нарушениями механики дыхания, вентиляции альвеол и гипоксией). И если при бронхолегочной патологии в основе уменьшения суммарного сечения сосудов легких лежит спазм артериол вследствие развития рефлекса Эйлера-Лильестранда, то у больных с васкулярной формой ЛС первично возникает органические изменения (сужение или закупорка) сосуда вследствие тромбозов и эмболий, некротизирующего ангиита. Схематически патогенез можно представить следующим образом (табл. 1).
В основе развития легочного сердца не зависимо от причины лежит легочная артериальная гипертензия, формирование которой обусловлено несколькими патогенетическими механизмами.
Патогенез острого легочного сердца (на примере ТЭЛА). В формировании ОЛС участвуют два патогенетических механизма:
- - «механическая» обструкция сосудистого русла,
- - гуморальные изменения.
«Механическая» обструкция сосудистого русла возникает вследствие обширной обструкции артериального русла легких (на 40-50%, что соответствует включению в патологический процесс 2-3 ветвей легочной артерии), что увеличивает общее легочное сосудистое сопротивление (ОЛСС). Увеличение ОЛСС сопровождается повышением давления в легочной артерии, препятствующей выбросу крови из правого желудочка, уменьшению наполнения левого желудочка, что суммарно приводит к снижению минутного объема крови и падению артериального давления (АД).
Гуморальные нарушения, возникающие в первые часы после обструкции сосудистого русла, в результате выброса биологически активных субстанций (серотонина, простагландинов, катехоламинов, выделение конвертазы, ангиотензинпревращающего фермента, гистамин), приводят к рефлекторному сужению мелких ветвей легочной артерии (генерализованная гипертоническая реакция легочных артерий), что еще больше увеличивает ОЛСС.
Первые часы после ТЭЛА характеризуются особенно высокой легочной артериальной гипертензией, быстро приводящей к перенапряжению правого желудочка, его дилатации и декомпенсации.
Патогенез хронического легочного сердца (на примере ХОБЛ). Ключевыми звеньями патогенеза ХЛС являются:
- - гипоксическая легочная вазоконстрикция,
- - нарушения бронхиальной проходимости,
- - гиперкапния и ацидоз,
- - анатомические изменения легочного сосудистого русла,
- - гипервискозный синдром,
- - увеличение сердечного выброса.
Гипоксическая легочная вазоконстрикция. Регуляция кровотока в системе малого круга кровообращения осуществляется благодаря рефлексу Эйлера-Лильестранда, который обеспечивает адекватное соотношение вентиляции и перфузии легочной ткани. При уменьшении концентрации кислорода в альвеолах благодаря рефлексу Эйлера-Лильестранда рефлекторно закрываются прекапиллярные сфинктеры (возникает вазоконстрикция), что приводит к ограничению кровотока в этих участках легкого. В результате чего местный легочный кровоток приспосабливается к интенсивности легочной вентиляции, и нарушений вентиляционно-перфузионных соотношений не происходит.
При хронических заболеваниях легких длительная альвеолярная гиповентиляция вызывает генерализованное повышение тонуса легочных артериол, ведущее к развитию стабильной легочной гипертензии. Кроме того, существует мнение, согласно которому в механизме формирования гипоксической легочной вазоконстрикции участвуют эндотелиальные факторы: эндотелины и ангиотензин II прямо стимулируют сокращение гладкой мускулатуры сосудистой стенки, тогда как снижение синтеза простагландина PgI2 и эндотелиального расслабляющего фактора (NO) усиливает вазоконстрикцию легочных артериол.
Нарушения бронхиальной проходимости. Неравномерность легочной вентиляции вызывает альвеолярную гипоксию, обусловливает нарушения вентиляционно-перфузионных соотношений и приводит к генерализованному проявлению механизма гипоксической легочной вазоконстрикции. Развитию альвеолярной гипоксии и формированию ХЛС больше подвержены больные, страдающие хроническим обструктивным бронхитом и бронхиальной астмой с преобладанием признаков дыхательной недостаточности («синие одутловатики»). У пациентов с преобладанием рестриктивных нарушений и диффузными поражениями легких (розовые пыхтельщики) альвеолярная гипоксия выражена значительно меньше.
Гиперкапния не прямо, а опосредовано влияет на возникновение легочной гипертензии путем:
- - появления ацидоза и, соответственно, рефлекторной вазоконстрикции,
- - снижения чувствительности дыхательного центра к СО2, что усугубляет нарушения вентиляции легких.
Анатомические изменения легочного сосудистого русла, вызывающие повышение ОЛСС, заключаются в развитии:
- - гипертрофии медии легочных артериол (за счет пролиферации гладкой мускулатуры сосудистой стенки),
- - запустевании артериол и капилляров,
- - тромбозе микроциркуляторного русла,
- - развитии бронхопульмональных анастомозов.
Гипервискозный синдром у больных с ХЛС развивается вследствие вторичного эритроцитоза. Этот механизм участвует в формировании легочной артериальной гипертензии при любом типе дыхательной недостаточности, проявляющейся выраженным цианозом. У больных ХЛС повышение агрегации форменных элементов крови и вязкости крови затрудняет кровоток по сосудистому руслу легких. В свою очередь повышение вязкости и замедление кровотока способствуют образованию пристеночных тромбов в ветвях легочной артерии. Вся совокупность гемостазиологических нарушение проводит к увеличению ОЛСС.
Увеличение сердечного выброса обусловлено:
- - тахикардией (увеличение сердечного выброса при значительной бронхиальной обструкции достигается возрастанием не ударного объема, а частоты сердечных сокращений, поскольку повышение внутригрудного давления препятствует венозному притоку крови в правый желудочек);
- - гиперволемией (одной из возможных причин гиперволемии является гиперкапния, способствующая увеличению концентрации альдостерона в крови и, соответственно, задержке Nа+ и воды).
Непременной составной частью патогенеза легочного сердца являются раннее развитие дистрофии миокарда правого желудочка и изменения гемодинамики.
Развитие дистрофии миокарда определяется тем, что укорочение диастолы при тахикардии и повышение внутрижелудочкового давления приводит к снижению кровотока в мышце правого желудочка и, соответственно энергодефициту. У ряда больных развитие миокардиодистрофии связано с интоксикацией из очагов хронической инфекции в дыхательных путях или паренхиме легких.
Гемодинамические изменения наиболее характерны для больных с развернутой клинической картиной ХЛС. Основными из них являются:
- - гипертрофия правого желудочка (ХЛС характеризуется постепенным и медленным развитием, поэтому сопровождается развитием гипертрофии мио-карда правого желудочка. ОЛС развивается в результате внезапного и значительного повышения давления в легочной артерии, что приводит к рез-кому расширению правого желудочка и истончению его стенки, поэтому гипертрофия правых отделов сердца развиться не успевает).
- - снижение систолической функции правых отделов сердца с развитием застоя крови в венозном русле большого круга кровообращения,
- - увеличение объема циркулирующей крови,
- - снижение сердечного выброса и уровня АД.
Таким образом, при бронхолегочной патологии стойкая легочная гипертензия формируется вследствие органического сужения просвета легочных сосудов (за счет облитерации, микротромбоза, сдавления сосудов, снижения способности легких к растяжению) и функциональных изменений (вызванных нарушениями механики дыхания, вентиляции альвеол и гипоксией). И если при бронхолегочной патологии в основе уменьшения суммарного сечения сосудов легких лежит спазм артериол вследствие развития рефлекса Эйлера-Лильестранда, то у больных с васкулярной формой ЛС первично возникает органические изменения (сужение или закупорка) сосуда вследствие тромбозов и эмболий, некротизирующего ангиита. Схематически патогенез можно представить следующим образом (табл. 1)