Клетки лангерганса находятся. Клетки лангерганса
Читайте также
Не следует путать с клетками Лангерганса - клетками эпидермальных тканей.
Островки Лангерганса - скопления гормон-продуцирующих (эндокринных) клеток, преимущественно в хвосте поджелудочной железы. Открыты в 1869 году немецким патологоанатомом Паулем Лангергансом (1849-1888). Островки составляют приблизительно 1…2 % массы поджелудочной железы. Поджелудочная железа взрослого здорового человека насчитывает около 1 миллиона островков (общей массой от одного до полутора граммов), которые объединяют понятием орган эндокринной системы .
Историческая справка
Пауль Лангерганс, будучи студентом-медиком, работая у Рудольфа Вирхова, в 1869 году описал скопления клеток в поджелудочной железе, отличавшиеся от окружающей ткани, названные впоследствии его именем. В 1881 году К. П. Улезко-Строганова впервые указала на эндокринную роль этих клеток. Инкреаторная функция поджелудочной железы была доказана в Страсбурге (Германия) в клинике крупнейшего диабетолога Наунина Mering и Minkowski в 1889 году - открыт панкреатический диабет и впервые доказана роль поджелудочной железы в его патогенезе. Русский учёный Л. В. Соболев (1876-1919) в диссертации «К морфологии поджелудочной железы при перевязке её протока при диабете и некоторых других условиях» показал, что перевязка выводного протока поджелудочной железы приводит ацинозный (экзокринный) отдел к полной атрофии, тогда как панкреатические островки остаются нетронутыми. На основании опытов Л. В. Соболев пришёл к выводу: «функцией панкреатических островков является регуляция углеводного обмена в организме. Гибель панкреатических островков и выпадение этой функции вызывает болезненное состояние - сахарное мочеизнурение».
В дальнейшем благодаря ряду исследований, проведенных физиологами и патофизиологами в различных странах (проведение панкреатэктомии, получение избирательного некроза бета-клеток поджелудочной железы химическим соединением аллоксаном), получены новые сведения об инкреаторной функции поджелудочной железы.
В 1907 году Lane & Bersley (Чикагский университет) показали различие между двумя видами островковых клеток, которые они назвали тип A (альфа-клетки) и тип B (бета-клетки).
В 1909 году бельгийский исследователь Ян де Мейер предложил называть продукт секреции бета-клеток островков Лангерганса инсулином (от лат. insula - островок). Однако прямых доказательств продукции гормона, влияющего на углеводный обмен, обнаружить не удавалось.
В 1921 году в лаборатории физиологии профессора J. Macleod в Торонтском университете молодому канадскому хирургу Фредерику Бантингу и его ассистенту студенту-медику Чарлзу Бесту удалось выделить инсулин.
В 1962 году Марлин и соавторы обнаружили, что водные экстракты поджелудочной железы способны повышать гликемию. Вещество, вызывающее гипергликемию, назвали «гипергликемическим-гликогенолитическим фактором». Это был глюкагон - один из основных физиологических антагонистов инсулина.
В 1967 году Донатану Стейнеру и соавторам (Чикагский университет) удалось обнаружить белок-предшественник инсулина - проинсулин. Они показали, что синтез инсулина бета клетками начинается с образования молекулы проинсулина, от которой в последующем по мере необходимости отщепляется С-пептид и молекула инсулина.
В 1973 году Джоном Энсиком (Вашингтонский университет), а также рядом учёных Америки и Европы была проведена работа по очистке и синтезу глюкагона и соматостатина.
В 1976 году Gudworth & Bottaggo открыли генетический дефект молекулы инсулина, обнаружив два типа гормона: нормальный и аномальный. последний является антагонистом по отношению к нормальному инсулину.
В 1979 году благодаря исследованиям Lacy & Kemp и соавторов появилась возможность пересадки отдельных островков и бета-клеток, удалось отделить островки от экзокринной части поджелудочной железы и осуществить трансплантацию в эксперименте. В 1979-1980 гг. при трансплантации бета-клеток преодолён видоспецифический барьер (клетки здоровых лабораторных животных имплантированы больным животным другого вида).
В 1990 году впервые выполнена пересадка панкреатических островковых клеток больному сахарным диабетом.
Типы клеток
Альфа-клетки
Основная статья: Альфа-клетка
- Альфа-клетки составляют 15…20 % пула островковых клеток - секретируют глюкагон (естественный антагонист инсулина).
Бета-клетки
Основная статья: Бета-клетка
- Бета-клетки составляют 65…80 % пула островковых клеток - секретируют инсулин (с помощью белков-рецепторов проводит глюкозу внутрь клеток организма, активизирует синтез гликогена в печени и мышцах, угнетает глюконеогенез).
Дельта-клетки
Основная статья: Дельта-клетка
- Дельта-клетки составляют 3…10 % пула островковых клеток - секретируют соматостатин (угнетает секрецию многих желез);
ПП-клетки
Основная статья: PP-клетка
- ПП-клетки составляют 3…5 % пула островковых клеток - секретируют панкреатический полипептид (подавляет секрецию поджелудочной железы и стимулирует секрецию желудочного сока).
Эпсилон-клетки
Основная статья: Эпсилон-клетка
- Эпсилон-клетки составляют <1 % пула островковых клеток - секретируют грелин («гормон голода» - возбуждает аппетит).
Строение островка
Панкреатический островок является сложно устроенным функциональным микроорганом с определенным размером, формой и характерным распределением эндокринных клеток. Клеточная архитектура островка влияет на межклеточное соединение и паракринную регуляцию, синхронизирует высвобождение инсулина.
Долгое время считалось, что островки человека и экспериментальных животных сходны как по строению, так и по клеточному составу. Работы последнего десятилетия показали, что у взрослых людей преобладающим типом строения островков является мозаичный, при котором клетки всех типов перемешаны по всему островку, в отличие от грызунов, для которых характерен плащевой тип строения клеток, при котором бета-клетки формируют сердцевину, а альфа-клетки находятся на периферии. Однако, эндокринная часть поджелудочной железы имеет несколько типов организации: это могут быть единичные эндокринные клетки, их небольшие скопления, небольшие островки (диаметром < 100 мкм) и крупные (зрелые) островки.
Небольшие островки имеют у человека и грызунов одинаковое строение. Зрелые островки Лангерганса человека обладают выраженной упорядоченной структурой. В составе такого островка, окруженного соединительнотканной оболочкой, можно выявить дольки, ограниченные кровеносными капиллярами. Сердцевину долек составляет массив бета-клеток, на периферии долек в непосредственной близости с кровеносными капиллярами находятся альфа- и дельта-клетки. Таким образом, клеточная композиция островка зависит от его размера: относительное число альфа-клеток увеличивается вместе с размером островка, в то время как относительное число бета-клеток уменьшается.
Исследования клеток Лангерганса показывают, что волны деполяризации легко распространяются от одной клетки к другой. При высокой концентрации глюкозы в среде краситель распространялся в большем числе соседних клеток, чем при низкой концентрации
Островки в поджелудочной железе были обнаружены в 1860 г. Лангергансом, однако он даже не представлял себе, какова их функция…
Когда Орци и др. обнаружили в клетках панкреатических островков соматостатин , это привело к переоценке всей микроанатомии островков. Было установлено, что альфа-, бета- и дельта-клетки в клетках Лангерганса человека и крысы расположены определенным образом. В поверхностном корковом слое альфа- и дельта-клетки лежат вперемешку и прилегают к наружному слою бета-клеток. «Мозговой слой», или сердцевина островка, полностью состоят из бета-клеток. В нормальных панкреатических островках бета-клетки составляют большую часть – 60%, альфа-клетки – 25%, а дельта-клетки – 10% всей клеточной популяции.
В некоторых условиях обычное соотношение типов клеток меняется. При гипертрофии клеток Лангерганса, вызванной ожирением или постоянным введением глюкокортикоидов, доля бета-клеток возрастает, а других – наоборот, снижается. В то же время при ювенильном диабете число бета-клеток снижено, тогда как количество глюкагон- и соматостатин-секретирующих клеток увеличено. С другой стороны, при диабете взрослых уменьшается число соматостатин-секретирующих клеток. Показано, что в корковом слое клеток Лангерганса вблизи двенадцатиперстной кишки синтезируется и четвертый пептид. Это вещество получило название «панкреатический полипептид»; его мол. масса – примерно 4200. Функция панкреатического полипептида неизвестна, но при диабете отмечена гиперплазия синтезирующих его клеток.
Взаимодействия между клетками Лангерганса
Взаимодействия между клетками Лангерганса чрезвычайно разнообразны: одни клетки образуют с соседними плотные контакты, тогда как другие соединяются щелевыми контактами. Щелевые контакты обладают низким сопротивлением и обеспечивают непрерывность цитоплазмы соседних клеток; через них вещества с мол. массой до 800 могут свободно перемещаться из клетки в клетку. Такие щели существуют не только между клетками одного типа (бета-бета), но и между клетками разных типов (альфа-дельта; aльфа-бета), и поэтому многие клетки могут одновременно получать общую информацию и реагировать на нее совместно (как клеточная колония).
Исследования клеток Лангерганса показывают, что волны деполяризации легко распространяются от одной клетки к другой. При высокой концентрации глюкозы в среде краситель распространялся в большем числе соседних клеток, чем при низкой концентрации. Это указывает на усиление межклеточной коммуникации в присутствии секреторного стимула. В панкреатических островках гормоны клеток одного типа влияют на секреторную активность клеток другого типа. К известным потенциально паракринным эффектам гормонов поджелудочной железы относятся следующие: ингибирует секреторную активность альфа-клеток; глюкагон стимулирует секреторную активность бета- и дельта-клеток; соматостатин ингибирует секреторную активность альфа- и бета-клеток.
На основании морфологических и функциональных взаимоотношений островковых клеток Орци, Унгер и их сотр. предположили, что островок Лангерганса представляет собой маленький орган, все клетки которого координированно отвечают на многие секреторные и ингибиторные стимулы. Согласно этой точке зрения, гормональная реакция панкреатического островка – это комплекс ответных реакций всех клеток Лангерганса не только на поступающие к ним гуморальные и нервные сигналы, но и а паракринные влияния, которые они оказывают друг на друга. Островок Лангерганса не только работает лучше искусственной железы, ну и служит микроминиатюрным средством, обеспечивающим большинству людей независимое существование в течение всей жизни.
Размещение объявлений - бесплатно и регистрация не требуется. Но есть премодерация объявлений.
Клетки Лангерганса
Клетки Лангерганса, именуемые в честь их первооткрывателя – П. Лангерганса, в настоящее время признаются подтипом дендритных клеток (до недавнего времени их причисляли к тканевым макрофагам кожного покрова). Данные клетки содержатся в эпителиальных тканях, они способны к фагоцитозу, не экспрессируют костимулятор В7 и играют значительную роль в обеспечении иммунного ответа организма.
Механизм их функционирования состоит в следующем. Клетки Лангерганса мигрируют по лимфатическим сосудам в ближайшие лимфоузлы, где преобразуются в стандартные дендритные клетки, обладающие поверхностными корецепторами В7. Это способствует созданию условий для включения иммунных ответов клеток типов CD8 T и CD4 T в случае проникновения патогенов через поврежденные участки кожного покрова и обеспечивает реакцию изоляции микроорганизмов. Клетки Лангерганса участвуют в обеспечении иммунного ответа и при наличии контактной гиперчувствительности кожного покрова. Кроме того, они в состоянии в течение продолжительного времени удерживать антигены, перемещать их в лимфоузлы, сохранять иммунологическую память.
Клеткам Лангерганса присуща эндокринная функция, обеспечивающая секрецию множества требуемых для жизнедеятельности эпидермиса веществ (в частности, простагландинов, гамма-интерферона, интерлейкина-1, а также элементов, регулирующих деление клеток и синтез белков). Имеются научные данные об особом антивирусном воздействии клеток Лангерганса и об их участии в разрушении папиллом.
Установлено, что в процессе хронических заболеваний, старения организма, UV-облучения, а также при интоксикациях число клеток Лангерганса существенно снижается.
Аналитика рынка
- Мировой рынок косметической упаковки – ориентация на цифровой мир и устойчивость
- Обзор мирового рынка косметики в 2018 г. Лучший год в истории мирового рынка красоты за последние 20 лет
- Косметические новинки 2018 года или индустрия красоты в новом формате
Салоны красоты Екатеринбурга Салоны красоты Новосибирска
Последние посты в блогах на нашем сайте
- Naturecream / Масло облепихи - "жидкое золото" для лица
- Naturecream / Суперфуд для кожи из Наварры
- Naturecream /
Марголина А.А. к.б.н., Эрнандес Е.И. к.б.н.
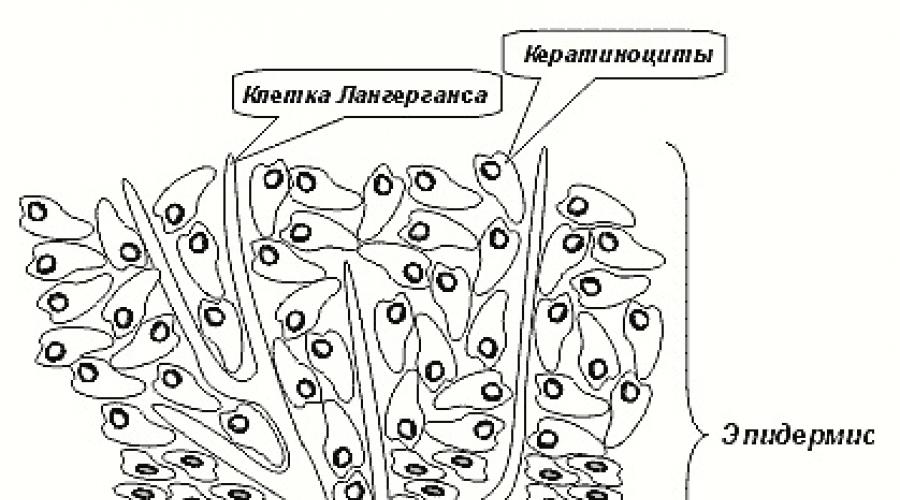
Эпидермис - это верхний, постоянно обновляющийся слой кожи. С дермой его связывает особая структура - базальная мембрана. Базальная мембрана - очень важное образование. Она служит фильтром, который не пропускает крупные заряженные молекулы, а также выполняет роль связующей среды между дермой и эпидермисом. Ученые считают, что через базальную мембрану эпидермис может влиять на клетки дермы, заставляя их усиливать или замедлять синтез различных веществ. Эта идея используется при разработке некоторых косметических средств, в которые вводятся особые молекулы - биорегуляторы, запускающие процесс дермо-эпидермального взаимодействия. На базальной мембране находится слой зародышевых клеток, которые непрестанно делятся, обеспечивая обновление кожи. Среди зародышевых клеток располагаются крупные отросчатые клетки - меланоциты и клетки Лангерганса. Меланоциты производят гранулы пигмента меланина, который придает коже определенный оттенок, от золотистого до темного или даже черного.

Клетки Лангерганса происходят из семейства макрофагов. Подобно макрофагам дермы они исполняют роль стражей порядка, то есть защищают кожу от внешнего вторжения и управляют деятельностью других клеток с помощью регуляторных молекул. Отростки клеток Лангерганса пронизывают все слои эпидермиса, достигая уровня рогового слоя. Считается, что клетки Лангерганса могут уходить в дерму, проникать в лимфатические узлы и превращаться в макрофаги. Это привлекает к ним большое внимание ученых, как к связующему звену между всеми слоями кожи. Есть мнение, что клетки Лангерганса регулируют скорость размножения клеток базального слоя, поддерживая его на оптимально низком уровне. При стрессовых воздействиях, когда на поверхность кожи действуют химические или физические травмирующие факторы, клетки Лангерганса дают базальным клеткам эпидермиса сигнал к усиленному делению.

Основными клетками эпидермиса являются кератиноциты, которые повторяют в миниатюре путь каждого живущего на земле организма. Они рождаются, проходят определенный путь развития и в конце концов умирают. Смерть кератиноцитов - запрограммированный процесс, который является логическим завершением их жизненного пути. Оторвавшись от базальной мембраны, они вступают на путь неизбежной гибели и, постепенно продвигаясь к поверхности кожи, превращаются в мертвую клетку - корнеоцит (роговая клетка). Этот процесс так хорошо организован, что мы можем разделить эпидермис на слои - в каждом слое находятся клетки на определенной стадии развития (или, как говорят ученые, дифференцировки). На базальной мембране сидят зародышевые клетки. Их отличительной особенностью является способность к бесконечному (или почти бесконечному) делению. Считается, что популяция активно делящихся клеток расположена в тех участках базальной мембраны, где эпидермис углублен в дерму. К старости эти углубления сглаживаются, что считается признаком истощения зародышевой популяции клеток кожи. Клетки базального слоя кожи делятся, порождая потомков, похожих на материнские клетки как две капли воды. Но рано или поздно некоторые из дочерних клеток отрываются от базальной мембраны и вступают на путь взросления, ведущий к гибели. Отрыв от базальной мембраны служит пусковым сигналом для синтеза белка кератина, который по мере продвижения клетки вверх заполняет всю цитоплазму и постепенно вытесняет клеточные органеллы. В конце концов кератиноцит теряет ядро и превращается в корнеоцит - плоскую чешуйку, набитую кератиновыми гранулами, придающими ей жесткость и прочность. Это происходит в самом верхнем слое кожи, который называют роговым. Роговой слой, состоящий из мертвых клеток, является основой эпидермального барьера нашей кожи.
Согласно современным взглядам, роговой слой состоит из плоских кератиновых чешуек, которые как кирпичи зацементированы липидной (жировой) прослойкой. Липидная прослойка образована особыми молекулами - так называемыми полярными липидами. Эти липиды отличаются от неполярных липидов тем, что они состоят из гидрофильной головы и гидрофобного хвоста. В воде молекулы полярных липидов самостоятельно группируются таким образом, чтобы гидрофобные хвосты были спрятаны от воды, а гидрофильные головы, напротив, были обращены в водную среду. Если таких липидов мало (или если смесь липидов и воды хорошо встряхнуть), то образуются шарики. Если молекул много, то они образуют протяженные двухслойные пласты.
Эпидермальный барьер

Липидные пласты рогового слоя построены из липидов, которые относятся к классу сфинголипидов, или церамидов. Впервые сфинголипиды были выделены из мозговой ткани. Свое второе название - церамиды - они получили от латинского слова cerebrum (мозг). Позже было найдено, что церамиды участвуют в построении эпидермального барьера, формируя липидную прослойку между роговыми чешуйками. Церамиды состоят из жирного спирта сфингозина (образует голову) и одной жирной кислоты (хвост). Если в жирной кислоте имеются двойные связи, то она называется ненасыщенной, если двойных связей нет, то говорят, что кислота насыщенная. В зависимости от того, какая жирная кислота прикреплена к голове церамида, липидные пласты, построенные из них, получаются более или менее жидкими. Самые твердые (кристаллические) липидные пласты образованы церамидами с насыщенными хвостами. Чем длиннее хвост церамида и чем больше в нем двойных связей, тем более жидкими получаются липидные структуры. 
Среди церамидов особо выделяются длинноцепочечные церамиды. Их хвосты представлены жирными кислотами, имеющими в своей цепочке более 20 атомов углерода. Длинноцепочечные церамиды выполняют роль заклепок, скрепляя соседние липидные пласты. Благодаря им многослойная липидная прослойка не расслаивается и представляет собой целостную структуру. Церамиды в последнее время стали очень популярными ингредиентами в косметике. Популярность церамидов объясняется той ролью, которую они играют в поддержании целостности эпидермального барьера. Благодаря наличию многослойной липидной прослойки между роговыми чешуйками, роговой слой способен эффективно защищать кожу не только от проникновения посторонних веществ извне, но и от обезвоживания. Как мы увидим, действие всех косметических средств надо оценивать прежде всего с точки зрения их воздействия на эпидермальный барьер, так как он довольно уязвим и легко разрушается. Нарушение целостности эпидермального барьера приводит к серьезным последствиям для кожи прежде всего вследствие нарушения водного баланса эпидермиса.
Кислотная мантия кожи
Поверхность нормальной кожи имеет кислую реакцию, и ее рН (мера кислотности) составляет 5,5 (нейтральный рН равен 7,0, а рН крови - 7,4). Практически все живые клетки (в том числе большая часть бактериальных) очень чувствительны к изменениям рН, и даже небольшое закисление для них губительно. Только кожа, покрытая слоем погибших ороговевших клеток, может себе позволить облечься в кислотную мантию (ее называют еще мантией Маркионини). Кислотная мантия кожи образована смесью кожного сала и пота, в которую добавлены органические кислоты - молочная, лимонная и другие. Эти кислоты образуются в результате биохимических процессов, протекающих в эпидермисе. Кислотная мантия кожи является первым звеном защиты от микроорганизмов, так как большинство микроорганизмов не любят кислую среду. И все-таки есть бактерии, которые постоянно живут на коже, например Staphylococcus epidermidis, лактобактерии. Они предпочитают жить именно в кислой среде и даже сами вырабатывают кислоты, внося свой вклад в формирование кислотной мантии кожи. Бактерии Staphylococcus epidermidis не только не приносят вреда коже, но даже выделяют токсины, которые обладают антибиотикоподобным действием и угнетают жизнедеятельность патогенной микрофлоры. Частое умывание с щелочным мылом может разрушить кислотную мантию. Тогда "хорошие" кислотолюбивые бактерии окажутся в непривычных условиях, а "плохие", кислоточувствительные бактерии получат преимущество. К счастью, кислотная мантия здоровой кожи достаточно быстро восстанавливается.
Кислотность кожи нарушается при некоторых кожных заболеваниях. Например, при грибковых заболеваниях рН возрастает до 6 (слабо кислая реакция), при экземе до 6,5 (почти нейтральная реакция), при угревой болезни до 7 (нейтральная). Надо отметить, что на уровне базального слоя эпидермиса, где располагаются зародышевые клетки, рН кожи становится равным рН крови - 7,4.
Дерма
Дерма играет роль каркаса, который обеспечивает механические свойства кожи - ее упругость, прочность и растяжимость. Она напоминает комбинацию водного и пружинного матраца, где роль пружин играют волокна коллагена и эластина, все пространство между которыми заполнено водным гелем, состоящим из мукополисахаридов (гликозаминогликанов). Молекулы коллагена на самом деле напоминают пружины, т. к. в них белковые нити скручены наподобие спиралей. Гликозаминогликаны - это большие полисахаридные молекулы, которые в воде не растворяются, а превращаются в сеточку, ячейки которой захватывают большое количество воды - образуется вязкий гель. Вблизи базальной мембраны дерма содержит больше гликозаминогликанов, а ее "пружины" более мягкие. Это так называемый сосочковый слой дермы. Он образует мягкую подушку непосредственно под эпидермисом. Под сосочковым слоем располагается сетчатый слой, в котором коллагеновые и эластиновые волокна формируют жесткую опорную сетку. Эта сетка также пропитана гликозаминогликанами. Главным гликозаминогликаном дермы является гиалуроновая кислота, которая имеет самую большую молекулярную массу и связывает больше всего воды.
Состояние дермы, этого матраца, на котором покоится эпидермис, его упругость и устойчивость к механическим нагрузкам определяются как состоянием "пружин" - волокон коллагена и эластина, так и качеством водного геля, образованного гликозаминогликанами. Если матрац не в порядке - ослабли пружины, или гель не держит влагу - кожа начинает обвисать под действием силы тяжести, смещаться и растягиваться во время сна, смеха и плача, сморщиваться и терять упругость. В молодой коже и коллагеновые волокна, и гликозаминогликановый гель постоянно обновляется. С возрастом обновление межклеточного вещества дермы идет все медленнее, накапливаются поврежденные волокна, а количество гликозаминогликанов неуклонно уменьшается. Найти способы воздействия на дерму - заветная мечта косметологов, т. к. это позволило бы реально устранять морщины. К сожалению, на деле добиться достоверного эффекта пока удается лишь пластическим хирургам.
Кроме коллагена, эластина и гликозаминогликанов (межклеточного вещества) дерма содержит клеточные элементы, кровеносные сосуды и железы (потовые и сальные) Основная задача клеток дермы - синтезировать и разрушать межклеточное вещество. В основном, этим занимаются фибробласты. Фибробласты производят многочисленные ферменты, с помощью которых они разрушают коллаген и гиалуроновую кислоту, а также синтезируют эти молекулы заново. Этот процесс происходит непрерывно, и благодаря ему межклеточное вещество постоянно обновляется. Особенно быстро протекает метаболизм гиалуроновой кислоты. В стареющей коже активность фибробластов снижается, и они все хуже справляются со своими обязанностями. Особенно быстро утрачивается способность к синтезу межклеточного вещества. А вот разрушительные способности долгое время остаются на прежнем уровне (ломать - не строить!). Поэтому в стареющей коже толщина дермы уменьшается, содержание влаги в ней падает, в результате кожа теряет ее упругость и эластичность.
Кроме фибробластов важными клетками дермы являются макрофаги. Они играют роль стражей порядка и следят за тем, чтобы чужеродные вещества не попадали в кожу. Макрофаги не обладают специфической памятью, поэтому их борьба с нарушителями порядка не приводит к развитию аллергической реакции. Все макрофаги наделены полномочиями отдавать приказы окружающим клеткам. Для этого они производят большое количество регуляторных молекул - цитокинов. Так же, как и фибробласты, макрофаги становятся менее активны с течением времени. Это приводит к снижению защитных свойств кожи и к неправильному поведению других клеток, которые ждут сигналов от макрофагов. В этом случае кожа напоминает страну при слабом правителе - падает боеготовность армии, ослабевает дисциплина, разрушается экономика. Чтобы как-то компенсировать это, в некоторые косметические средства и пищевые добавки включают вещества, стимулирующие макрофаги и заставляющие их активнее исполнять свои функции.

Вся дерма пронизана тончайшими кровеносными и лимфатическими сосудами. Кровь, протекающая по сосудам, просвечивает сквозь эпидермис и придает коже розовый оттенок. Из кровеносных сосудов в дерму поступает влага и питательные вещества. Влага захватывается гигроскопичными (связывающими и удерживающими влагу) молекулами - белками и гликозаминогликанами, которые при этом переходят в гелевую форму. Часть влаги поднимается выше, проникает в эпидермис и потом испаряется с поверхности кожи. Кровеносных сосудов в эпидермисе нет, поэтому влага и питательные вещества медленно просачиваются в эпидермис из дермы. При уменьшении интенсивности кровотока в сосудах дермы в первую очередь страдает эпидермис. В этом случае кожа напоминает дерево, которое начинает засыхать с верхушки. Поэтому внешний вид кожи во многом зависит от состояния ее кровеносных сосудов. Сосудистая гимнастика, массаж, микротоковая стимуляция и препараты, укрепляющие стенки сосудов и улучшающие микроциркуляцию, будут благотворно сказываться на внешнем виде кожи. Впрочем, возможен и другой вариант, когда сухость эпидермиса объясняется слишком интенсивным испарением воды через роговой слой. В этом случае поступление воды из дермы может сохраняться на прежнем уровне.
Заключение
Большинство органов нашего тела состоит из живых клеток, поэтому эффект от любого (в том числе и лекарственного) воздействия на эти органы можно представить как сумму реакций отдельных клеток. С кожей ситуация несколько иная. Кожа - это совокупность живых клеток, межклеточного вещества (которое занимает довольно большой объем) и неживых клеток (роговых чешуек). Существенное изменение функционирования кожи может быть достигнуто только через изменения в живых клетках, причем процесс этот довольно длительный. Воздействуя на неживые клетки и на внеклеточное вещество можно добиться временного изменения внешнего вида кожи (например, насыщение внеклеточного вещества дермы влагой приведет к разглаживанию кожи и повышению ее упругости, а отшелушивание мертвых чешуек с поверхности кожи осветлит ее). Изменения состояния внеклеточного вещества и слоя неживых клеток могут в свою очередь сказаться на деятельности живых клеток. Тогда кроме временного эффекта, который можно наблюдать сразу после воздействия, в коже будут происходить медленные изменения, результат которых проявится спустя длительное время.
Нанося на кожу косметику, мы часто наблюдаем немедленный эффект. При этом отсроченные эффекты ускользают от нашего внимания. Проследить их самостоятельно практически невозможно. Во-первых, они могут проявляться спустя недели и даже месяцы. Во-вторых, количество веществ, которые мы за это время успеем нанести на кожу, слишком велико, чтобы связать изменения кожи с каким-то конкретным кремом или лосьоном. Поэтому очень важно знать основные объекты воздействия для косметических средств в коже и хорошо представлять, какие из наблюдаемых эффектов могут быть вызваны воздействием на живые клетки, а какие - на другие структуры кожи. Важно уметь не поддаваться иллюзиям и каждый раз задумываться над тем, что реально может косметика.
Наша кожа защищает нас от порезов, кислот, низких и высоких температур… пожалуй, это всё, что мы сможем услышать о свойствах кожи от случайно спрошенного человека. И как видим, тут речь идет о чисто механических функциях защиты. Кожа воспринимается нами чем-то наподобие био-чехла, механически нас защищающего.
Это несомненно так и есть. Но это далеко не всё, чем является наша кожа.
На самом деле, кожа является по сути отдельным органом нашего тела. Этой фразы достаточно, наверное, чтобы указать на то — насколько сложным объектом она является. И конечно, в одном посте мы не сможем даже близко описать все ее удивительные свойства, поэтому сейчас давай рассмотрим только один аспект.
Наша кожа выполняет иммунологические функции. Она выявляет патогенов и борется с ними. Как именно? В составе кожи есть особые клетки — КЛЕТКИ ЛАНГЕРГАНСА (не путать с островками Лангерганса в хвосте поджелудочной железы). Она является внутридермальным макрофагом. «Внутридермальный» — значит внутри дермы — среднего слоя кожи. «Макрофаг» — значит она охотится на патогенов и пожирает их.
Клетка Лангерганса ведет себя как настоящий сторож — она может мигрировать из дермы в эпидермис (самый верхний слой кожи) и обратно. По пути может заглядывать в лимфатические узлы. В общем — сторожит, бодрствует, на посту.
Иногда болезнетворная бактерия натыкается на клетку Лангерганса, если ей удалось пробраться через плотный слой КЕРАТИНОЦИТОВ (роговые чешуйки на самой поверхности кожи), скрепленных МЕЖКЛЕТОЧНЫМ ЦЕМЕНТОМ. И тогда клетка Лангерганса, будучи хорошо подготовленным макрофагом, пожирает бактерию и выставляет на своей наружной мембране её фрагменты.
Для чего? Таким образом она показывает фрагменты патогена Т-лимфоцитам, которые живут тут же, рядом, в эпидерме и лимфатических узлах. А дальше запускается обычная иммунная реакция с участие Т-хелперов, Т-киллеров и т.д.
Клеток Лангерганса в нашем эпидермисе (верхнем слое кожи) очень много, иногда до 8% от всего количества клеток! Так что армия стоит у нас на защите очень мощная, и кроме того у них есть и помощники — другие макрофаги — КЛЕТКИ ГРИНСТЕЙНА.
Вот так — рука об руку, копье к копью, так сказать:) клетки Лангерганса, клетки Гринстейна и Т-лимфоциты, живущие внутри нашей кожи, предохраняют нас от патогенов, достаточно сильных и хитрых, чтобы преодолеть первый, механический барьер на своем пути. И поскольку бактерий вокруг очень много, работы нашим защитникам хватает, и они постоянно выделяют биоактивные вещества, которые убийственно действуют на врага. И поэтому нашей коже нужна защита от этих наших собственных химикатов, чтобы они не повредили лежащие ниже собственные наши клетки. И этим занимаются другие клетки кожи с помощью особых белков.